SARS-CoV-2に対する免疫低下の豊富なダイナミクスとデータ解析
The global pandemic of SARS-CoV-2 has constituted a serious threat to public health.
背景と学術的系譜
起源と学術的系譜
本問題の正確な起源は、世界的なSARS-CoV-2パンデミックとそれに続く広範なワクチン接種努力に直接由来する。パンデミックが進行するにつれて、自然感染およびワクチン接種の両方が免疫保護を提供することが明らかになったが、この保護は永続的ではなく、決定的に、一定または線形の速度で減衰するものではなかった(13-15行)。この観察は、流行の長期的な軌跡を正確にモデル化し、効果的な公衆衛生介入を設計する上で、重大な課題を生み出した。歴史的文脈は、SARS-CoV-2に対する免疫が時間とともにどのように減衰し、ブレークスルー感染を引き起こし、ワクチンの長期的な保護効果を損なうかを理解する必要性に根差している(45-47行)。
先行アプローチの根本的な限界、すなわち「ペインポイント」は二重であった。第一に、初期のモデルは免疫減衰を単純化しすぎている(例:一定または線形減衰)か、観察された複雑さを捉えようとすると「非常に複雑になり、系統的な理論的分析を困難にする」ものとなっていた(112-114行)。これらの複雑なモデルは、制御戦略の探索や、孤立した条件下での分岐現象の検討のために、しばしば数値シミュレーションに大きく依存していた(114-116行)。系統的な理論的分析ではなく、数値的手法へのこの依存は、根本的なダイナミクスを包括的かつ扱いやすい形で理解することを妨げた。したがって、著者らは、これらの分析的課題を克服し、免疫減衰とその疾患伝播への影響を研究するための、より扱いやすいフレームワークを提供するために、「免疫減衰に起因する非線形ダイナミクスを捉える、比較的単純でありながら生物学的に意味のあるモデル」を開発する必要に迫られたのである(116-118行)。
直感的ドメイン用語
- 免疫減衰 (Immune Waning): 過去の感染またはワクチンによって獲得された疾患に対する人の免疫保護が、時間とともに徐々に低下することを指す。
- アナロジー: 満充電された後、スマートフォンのバッテリーがゆっくりと充電を失っていく様子を想像してほしい。体の保護は単にオフになるのではなく、ゆっくりと色褪せ、再び感染しやすくなる。
- 後方分岐 (Backward Bifurcation): 疾患モデリングにおいて、これは、基本再生産数 ($R_0$) が1未満であっても、疾患が持続し、風土病となる可能性があるという特異な状況である。通常、$R_0 < 1$ は疾患が自然に終息することを意味する。
- アナロジー: やや傾斜した表面にある重いボールを考えてほしい。小さなプッシュをすると、元の場所に戻るかもしれない。しかし、十分な初期プッシュをすると、小さなこぶを乗り越えて、傾斜全体が戻るべきだと示唆しているにもかかわらず、さらに下のくぼみに引っかかってしまうかもしれない。この現象は他の分野でも発生している。初期の「勢い」(感染者数)が、疾患が風土病状態に「閉じ込められる」かどうかを決定する可能性がある。
- 基本再生産数 ($R_0$) (Basic Reproduction Number): これは、完全に感受性のある集団において、1人の感染者から引き起こされる新規感染者の平均数を表す重要な数値である。
- アナロジー: 新しいバイラルダンスの流行を考えてほしい。1人が平均して1人以上の新しい人に教える ($R_0 > 1$) なら、ダンスは広がる。1人未満の新しい人に教える ($R_0 < 1$) なら、流行は最終的に消滅する。
- 風土病均衡 (Endemic Equilibrium): これは、流行において疾患が集団内で一貫して存在する安定した状態を指し、感染者数は時間とともに比較的一定に保たれ、急速に増加も消滅もしない。
- アナロジー: 安定した流れを持つ川を思い浮かべてほしい。水は常に動いているが、全体的な水位と流れの速さは同じままである。疾患は常に存在するが、その存在は突然の急増や完全な不在ではなく、予測可能で安定している。
記法表
| 記法 | 説明 (単位) |
|---|---|
問題定義と制約
コア問題の定式化とジレンマ
本稿が取り組むコア問題は、SARS-CoV-2に対する免疫減衰の複雑かつ非線形な性質に起因する。
入力/現状:
初期段階では、自然感染またはワクチン接種により、SARS-CoV-2に対するある程度の免疫保護を獲得した個人が存在する。しかしながら、この免疫の現在の理解とモデリングは、いくつかの重要な側面において不十分である。
1. 非線形な減衰: 免疫の効果は一定または線形な速度で低下するわけではない。むしろ、時間とともに、より複雑で非線形な様式で減衰する(Abstract, 14-15行)。
2. モデルの複雑性と現実性のトレードオフ: 免疫減衰を捉えようとする既存の疫学モデルは、しばしば二つの極端に陥る。すなわち、単純すぎる(例:線形減衰を仮定する)か、あるいは非常に複雑である(例:年齢構造モデル、個人固有の減衰率を持つモデル、あるいはワクチン接種者/回復者に対する別個のコンパートメント)。この複雑さにより、分岐ダイナミクス(bifurcation dynamics)の理解のような系統的な理論解析が極めて困難になり、しばしば孤立した条件下での数値シミュレーションへの依存を余儀なくされる(Introduction, 65-78行, 112-116行, 445-447行)。
3. 不完全な動的特性評価: 過去のモデルは、特に後方分岐(backward bifurcation)のような現象、すなわち基本再生産数 ($R_0$) が1未満であっても疾患が持続する可能性といった、免疫の動的プロセスを完全に特性評価するのに苦労している(Introduction, 90-91行, 96-102行)。これは、単に $R_0$ を1未満にしても、疾患を根絶するには十分ではない可能性があり、公衆衛生戦略にとって重大な課題を提起する。
望ましい終点(出力/目標状態):
本稿は、以下のことが可能な新しい数学的モデルの開発を目指す。
1. 二段階減衰の捕捉: より生物学的に現実的な「二段階免疫減衰メカニズム」(Abstract, 15-16行; Introduction, 120-122行)を組み込むことにより、免疫の動的プロセスを正確に特性評価する。これは、初期の強力な免疫期間とその後のより急速な低下をモデル化することを意味する。
2. 単純性と扱いやすさの達成: 「比較的単純でありながら生物学的に意味のある」(Introduction, 116-118行)ものであり、「数学的な扱いやすさ」(Discussion, 449-450行)を維持する。このバランスは、包括的な分岐解析を含む厳密な理論解析を可能にする上で極めて重要である。
3. 公衆衛生戦略への貢献: SARS-CoV-2感染の根底にある免疫学的メカニズムと制御措置の影響を調査することにより、より効果的な公衆衛生戦略と政策の開発のための科学的根拠を提供する(Introduction, 48-51行, 118-119行)。
欠落しているリンク/数学的ギャップ:
正確に欠落しているリンクは、SARS-CoV-2に対する非線形な二段階免疫減衰メカニズムを明示的に組み込み、複雑な動的挙動(分岐や二安定性など)の厳密な理論解析と、現実世界の疫学データを用いた堅牢なパラメータ推定を可能にする、数学的に扱いやすいコンパートメントモデルである。過去のモデルは、減衰プロセスを単純化しすぎるか、あるいは包括的な理論解析には複雑になりすぎたため、免疫減衰の完全な動的影響の理解にギャップを残していた。
ジレンマ:
過去の研究者を悩ませてきた中心的なジレンマは、生物学的現実性と数学的扱いやすさとの間のトレードオフである。免疫減衰のニュアンス(例:個体間の異質性、年齢構造、非線形減衰)を正確に表現するためには、モデルは非常に複雑になりがちである。しかし、この複雑さはしばしば解析的に扱いにくくさせ、研究者は特定のシナリオに対して数値シミュレーションのみに頼らざるを得なくなる。本稿は、生物学的に意味がありながらも、基本再生産数の導出や包括的な分岐解析を含む厳密な数学的解析を可能にするのに十分単純な、特定の二段階減衰メカニズムを導入することにより、このギャップを埋めようと試みる(Discussion, 448-450行)。
制約と失敗モード
SARS-CoV-2における免疫減衰のモデリング問題は、著者が直面するいくつかの厳しい現実的な壁により、非常に困難である。
- 非線形かつ異質な免疫減衰: 免疫の効果は一定または線形な速度で低下するわけではない(Abstract, 14-15行)。むしろ、免疫は時間とともに減衰し、再感染に対する感受性の異質性を引き起こす。個人は通常、初期期間は高い保護を維持するが、その後、抗体レベルと保護効果は著しく低下し、最終的には消失に近づく(Introduction, 105-111行)。この複雑な生物学的プロセスを正確に表現する必要がある。
- 免疫回避メカニズムの出現: ウイルスは進化し、免疫回避メカニズムが出現し、ワクチンや自然免疫の長期的な保護効果を損なう(Introduction, 46-47行)。これはメカニズムとして明示的にモデル化されていないが、この生物学的な現実は、変化する免疫ランドスケープに適応できる動的モデルの必要性を強調している。
- 時間変動する疫学パラメータ: 伝播率 ($\beta(t)$) やワクチン接種率 ($\alpha(t)$) のような主要なパラメータは一定ではなく、時間とともに大きく変動する。これらの変動は、新しい変異株(例:Delta, Omicron)の出現、行動の変化、非医薬品介入(Discussion, 491-493行)など、複数の外部要因の影響を受ける。これにより、静的なパラメータモデルは不十分となり、時間依存パラメータを推定するための手法が必要となる。
- データ駆動型パラメータ推定の課題: モデルは、長期間(例:米国における2020年12月から2022年6月まで)にわたる現実世界のノイズの多い疫学データ(例:日々の新規確認COVID-19症例数、日々の新規ワクチン接種回数)に適合させる必要がある(Abstract, 23-25行; Discussion, 471-473行)。これには、時間変動する性質とデータの固有の不確実性を処理するために、マルコフ連鎖モンテカルロ法(MCMC)と区分的3次スプライン関数を組み合わせた堅牢な統計的手法が必要となる(Abstract, 25-26行; Discussion, 473-474行)。
- 分岐解析のための数学的扱いやすさ: 基本再生産数の導出や包括的な分岐解析を含む厳密な理論解析を実行し、前方分岐や後方分岐、複数の定常平衡の共存といった複雑な動的挙動を理解することが目標である(Abstract, 16-22行; Discussion, 449-450行)。これは、過度に複雑なモデルは解析的に扱いにくくなるため、モデルの複雑さに厳格な制約を課す。
- モデルの安定性と現実性の確保: モデルは、人口コンパートメントが有界かつ非負に保たれることを保証しなければならない。これは、あらゆる現実的な疫学モデルの基本的な要件である(Model derivation, 144-145行; Invariant regions, Lemma 1, 184-187行)。この数学的な制約は、モデルの出力が生物学的に妥当であることを保証する。
- 複雑な分岐現象の解釈: モデルは、鞍結点分岐(saddle-node bifurcations)や二安定性(bistability)のような複雑な動的挙動を明らかにする。これは、複数の安定な定常平衡が共存しうることを意味する。すなわち、$R_0 < 1$ の場合でも疾患が持続する可能性があり、これは従来の公衆衛生戦略に挑戦する重要な発見であり、慎重な解釈を必要とする(Abstract, 19-22行; Discussion, 461-467行)。これらの現象を理解するには、厳密な数学的証明と数値的検証が必要である。
このアプローチの理由
選択の必然性
著者らが新規の二段階免疫減衰モデルを開発するという決定は、恣意的なものではなく、SARS-CoV-2免疫の複雑な動態に直面した際の従来の疫学モデルの固有の限界に対する直接的な応答であった。標準的な「SOTA」(State-of-the-Art)疫学手法が不十分であるという認識は、ウイルスとヒトの免疫応答に関するいくつかの重要な観察から生じた。
第一に、自然感染またはワクチン接種による免疫保護が「一定または線形な速度で低下しない」ことが明らかになった(Abstract, lines 14-15)。これは、免疫の単純かつ連続的な減衰を仮定することが多い基本的なSIRS(Susceptible-Infected-Recovered-Susceptible)モデルを、ニュアンスのある生物学的プロセスを捉えるには不十分なものとした。免疫回避メカニズムの「出現[8]」と「短期間でのブレークスルー感染[7]」の現実は(Introduction, lines 45-48)、より動的で多面的な免疫減衰の表現の必要性をさらに強調した。
第二に、決定的な洞察は後方分岐現象であり、「$R_0 < 1$であっても必ずしも疾患の根絶を保証しない」(Introduction, lines 91-92)というものであった。従来のモデルは、基本再生産数($R_0$)が1を下回れば、流行は自然に終息すると根本的に仮定している。しかし、$R_0$がこの閾値を下回るシナリオでもSARS-CoV-2の持続が観察されたことは、これらのより単純な枠組みにおける重大な欠陥を浮き彫りにした。著者らのモデルは、この複雑な動態を明示的に捉え、「基本再生産数$R_0 < 1$であっても流行が持続する」(Abstract, lines 21-22)ことを示しており、これはより単純なモデルでは説明できない特徴である。
最後に、既存の高度なモデルは免疫減衰の側面を組み込み始めていたものの(例:[17, 18, 19])、多くは「非常に複雑で、体系的な理論解析を困難にし」、しばしば「制御戦略の検討や、孤立した条件下での分岐現象の検討に数値シミュレーションに依存していた」(Introduction, lines 112-115)。著者らは、他のアプローチにおける過度の複雑さによってしばしば損なわれていた厳密な理論解析を可能にするために、「比較的単純でありながら生物学的に意味のある」モデルを求め、「これらの限界に対処する」ことを明確に目指した(Introduction, lines 115-117)。生物学的現実性と数学的扱いやすさのバランスというこの必要性が、彼らの特定の二段階コンパートメント構造の選択を確固たるものにした。
比較優位性
この二段階免疫減衰モデルの質的な優位性は、単なる性能指標を超えて、複雑な疫学的現実を捉えつつ分析的厳密性を維持することを可能にする構造的利点にある。
- 生物学的に現実的な免疫減衰: 最も重要な構造的利点は、「部分的に、さらに減衰した免疫を持つ」個人を表す二つの異なるコンパートメント、$S_1(t)$および$S_2(t)$の明示的な導入である(Introduction, lines 120-127)。これにより、モデルは単純な線形減衰を超え、免疫を「完全に免疫のある状態から部分的に免疫のある状態への非線形遷移」として特徴づけることができる(Discussion, lines 448-449)。この多段階アプローチは、保護が均一で連続的な低下ではなく、時間とともに徐々に、かつ異質に低下するという生物学的プロセスにより忠実な表現である。
- 堅牢な分岐解析と二安定性: モデルの設計は、前方および後方分岐の厳密な導出と解析を容易にする(Abstract, lines 17-18; Discussion, lines 454-455)。後方分岐を示す能力は、重要な質的飛躍であり、「$R_0 < 1$であっても必ずしも疾患の根絶を保証しない」(Introduction, lines 91-92)ことを説明する。これは、従来の指標が終息を示唆する場合でも、疾患が蔓延しうることを意味する。さらに、モデルは「複数の定常状態の共存」と「二安定性」を明らかにする(Abstract, lines 18-22; Discussion, lines 458-469)。これは、流行の長期的な軌跡が初期条件に非常に敏感である可能性を示唆しており、より単純なモデルでは達成できないレベルの動的複雑性である。
- 深い洞察のための数学的扱いやすさ: 「非常に複雑で、しばしば数値シミュレーションに依存する」多くの既存モデルとは異なり(Introduction, lines 112-113)、この二段階モデルは「比較的単純でありながら生物学的に意味のある」ように設計されている(Introduction, lines 115-117)。この構造的な選択により、「基本再生産数の厳密な導出と包括的な分岐解析」が可能になる(Discussion, lines 449-451)。このバランスは、記述的なシミュレーションだけでなく、流行の動態を駆動するメカニズムに関する深い理論的洞察を提供するという点で、重要な利点である。
- 時間変動する実世界データの統合: モデルは、区分的多項式スプライン関数とMCMCアルゴリズムを使用して推定された時間変動する伝播率$\beta(t)$およびワクチン接種率$\alpha(t)$を組み込んでいる(Discussion, lines 470-473)。これにより、モデルは現実世界の疫学的データや変化する介入戦略に適応でき、静的パラメータに依存するモデルよりも動的で適用可能なフレームワークを提供する。
本論文は、機械学習アルゴリズムの文脈における$O(N^2)$から$O(N)$へのメモリ削減や高次元ノイズの処理といった計算複雑性については論じていない。その優位性は、むしろ疫学的現実性の向上と疾患伝播理解のための分析能力に根差している。
制約との整合性
選択された二段階免疫減衰モデルは、問題定義から導き出される暗黙の制約と完全に整合しており、SARS-CoV-2の動態の課題と解の独自の特性との間に強力な「結婚」を生み出している。
- 制約:免疫低下の正確な表現: 問題は、「免疫の効果が一定または線形な速度で低下しない」こと、そして免疫が「時間とともに減衰する傾向があり、再感染に対する感受性の不均一性を引き起こす」(Abstract, lines 14-15; Introduction, lines 105-106)モデルを必要とする。解の独自の特性は、「二段階免疫減衰メカニズム」(Abstract, line 16)であり、「部分的に、さらに減衰した免疫」のためのコンパートメント($S_1(t)$および$S_2(t)$)(Introduction, lines 120-127)を明示的に導入する。これは、免疫減衰の非線形かつ異質な性質に直接対処し、より生物学的に正確でニュアンスのある表現を提供する。
- 制約:複雑な流行持続の説明: 重要な要件は、従来の指標が根絶を示唆する場合でも、SARS-CoV-2の観察された持続を説明することである。モデルの「前方および後方分岐」および「二安定性」を示す能力(Abstract, lines 17-22; Discussion, lines 454-469)は、完璧に適合する。特に後方分岐は、「$R_0 < 1$であっても必ずしも疾患の根絶を保証しない」(Introduction, lines 91-92)ことを示し、流行を持続させることを可能にする。これは、単純なモデルの予測と現実世界の観察との間の乖離を直接解決する。
- 制約:政策洞察のための数学的扱いやすさ: 公衆衛生戦略に情報を提供するためには、現実的かつ厳密な理論解析に適したモデルが必要である。多くの既存モデルは「非常に複雑で、体系的な理論解析を困難にしている」(Introduction, lines 112-113)が、この二段階モデルは「比較的単純でありながら生物学的に意味のある」ように設計されている(Introduction, lines 115-117)。これにより、「基本再生産数の厳密な導出と包括的な分岐解析」が可能になり(Discussion, lines 449-451)、過度に複雑で扱いにくいモデルでは不明瞭になる可能性のある、明確で実行可能な洞察を提供する。
- 制約:データ駆動型および動的なパラメータ化: 急速に進化するパンデミックの効果的なモデリングには、実世界データを取り込み、時間変動要因を考慮する能力が必要である。「COVID-19の米国からの疫学的データ」から時間変動する伝播率$\beta(t)$およびワクチン接種率$\alpha(t)$を推定するために「区分的多項式スプライン関数と組み合わせたMCMCアルゴリズム」を使用する(Abstract, lines 23-25; Discussion, lines 470-473)という解の利用は、この制約を完璧に満たす。この動的なパラメータ化は、モデルの関連性とリアルタイムの流行制御における予測力を高める。
このアプローチは、生物学的複雑性と分析的実現可能性の間のギャップを効果的に橋渡しし、SARS-CoV-2の理解と管理のための理想的なツールとなっている。
代替案の却下
本論文は、コンパートメント疫学モデリングに焦点を当てているため、GANや拡散モデルのような深層学習アプローチについては、その範囲外であるため議論または却下していない。しかし、他の疫学モデリングの代替案を暗黙のうちに却下またはその限界を強調している。
-
標準的なSIR/SIRSモデル: これらの基礎的なモデルは、SARS-CoV-2免疫の特定の複雑さを捉える能力がないため、暗黙のうちに不十分と見なされている。
- SIRモデル: これらは終生免疫を仮定する(Introduction, lines 53-54)が、SARS-CoV-2に対しては明らかに偽であり、免疫は減衰する。
- 基本的なSIRSモデル: 免疫減衰を考慮するものの、しばしばそれを「一定または線形な速度」(Abstract, lines 14-15)または単純で連続的な減衰(Discussion, lines 445-446)に単純化する。著者らの研究は、「二段階免疫減衰メカニズム」が「完全に免疫のある状態から部分的に免疫のある状態への非線形遷移」(Discussion, lines 448-449)を反映するために必要であることを示すことで、これを直接否定している。
- 後方分岐の説明失敗: これらのより単純なモデルを却下する重要な理由は、流行が基本再生産数$R_0 < 1$であっても持続するような後方分岐現象を説明できないことである(Abstract, lines 21-22; Discussion, lines 462-469)。標準的なSIRSモデルは、そのような条件下での根絶を予測するため、SARS-CoV-2には不十分である。
-
過度に複雑な既存の疫学モデル: 本論文は、より詳細を捉えようとしながらも分析的に扱いにくくなるモデルの却下も示唆している。著者らは、「既存のモデルのほとんどは非常に複雑で、体系的な理論解析を困難にしている。これらの研究は、しばしば制御戦略の検討や、孤立した条件下での分岐現象の検討に数値シミュレーションに依存している」(Introduction, lines 112-115)と述べている。これは、これらのモデル(例えば、連続的な減衰関数、個人固有の率、または多数の別個のコンパートメントを持つものなど、Discussion, lines 445-447で言及されている)が詳細な詳細を提供する可能性がある一方で、著者らが優先する厳密な理論解析と包括的な分岐研究を妨げる複雑さを持っていることを示唆している。対照的に、選択された二段階モデルは、「より単純で生物学的に解釈しやすいフレームワークを提供する」一方で、「基本再生産数の厳密な導出と包括的な分岐解析」を可能にする(Discussion, lines 448-451)。これは、過度に複雑で扱いにくい詳細のために分析的な深さを犠牲にするモデルを避けるという意図的な選択を強調している。
本質的に、著者らは、SARS-CoV-2の観察された非線形免疫動態と複雑な分岐現象を反映するには単純すぎたり、望ましいレベルの厳密な理論解析とメカニズムの理解を可能にするには複雑すぎたりする代替案を却下した。彼らの二段階モデルは、分析的に扱いにくくなることなく、十分な生物学的現実性を提供し、実用的なバランスを取っている。
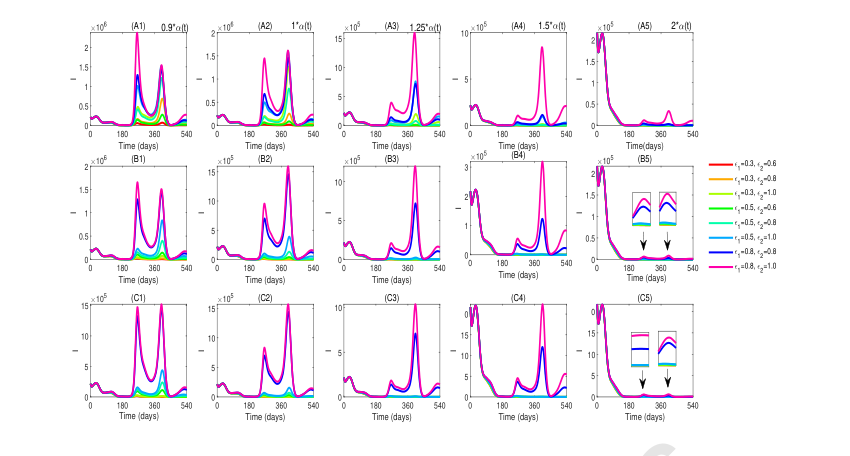 Figure 5. The impact of different vaccination rates, duration of secondary waning immunity, and two relative susceptibilities on disease transmission dynamics. By combining ε1 = 0.3, 0.5, 0.8 and ε2 = 0.6, 0.8, 1 in all possible pairwise combinations, we derive situations in which two relative suscep- tibilities change concurrently. (A1)-(C1), (A2)-(C2), (A3)-(C3), (A4)-(C4), and (A5)-(C5) correspond to multiples of the original vaccination rate of 0.9, 1, 1.25, 1.5, and 2, respectively. The figures are arranged into five columns based on different multiples of the original vaccination rate in the model and into three rows according to different immune waning durations. The durations of the secondary waning immunity 1 δV + 1 δS1 = 1 δR + 1 δS1 = 180, 365, 540 days, respectively, corresponds to (A1)-(A5),
Figure 5. The impact of different vaccination rates, duration of secondary waning immunity, and two relative susceptibilities on disease transmission dynamics. By combining ε1 = 0.3, 0.5, 0.8 and ε2 = 0.6, 0.8, 1 in all possible pairwise combinations, we derive situations in which two relative suscep- tibilities change concurrently. (A1)-(C1), (A2)-(C2), (A3)-(C3), (A4)-(C4), and (A5)-(C5) correspond to multiples of the original vaccination rate of 0.9, 1, 1.25, 1.5, and 2, respectively. The figures are arranged into five columns based on different multiples of the original vaccination rate in the model and into three rows according to different immune waning durations. The durations of the secondary waning immunity 1 δV + 1 δS1 = 1 δR + 1 δS1 = 180, 365, 540 days, respectively, corresponds to (A1)-(A5),
数学的・論理的メカニズム
マスター方程式
本論文の解析の中核をなすのは、人口における健康状態と免疫状態の異なる個体間の動的な流れを記述する、8つの連立常微分方程式(ODE)のシステムである。論文中で(2)とラベル付けされたこのシステムは、2段階の免疫減衰メカニズムを組み込み、SARS-CoV-2の蔓延と制御をシミュレートする数学的エンジンである。
$$ \begin{aligned} \frac{dS}{dt} &= \Lambda - \lambda(t)S - (\alpha + d)S \\ \frac{dV}{dt} &= \alpha(S + S_1 + S_2) - (\delta_V + d)V \\ \frac{dS_1}{dt} &= \delta_V V + \delta_R R - \epsilon_1\lambda(t)S_1 - (\alpha + \delta_{S_1} + d)S_1 \\ \frac{dS_2}{dt} &= \delta_{S_1} S_1 - \epsilon_2\lambda(t)S_2 - (\alpha + d)S_2 \\ \frac{dE}{dt} &= \lambda(t)S + \epsilon_1\lambda(t)S_1 + \epsilon_2\lambda(t)S_2 - (\sigma + d)E \\ \frac{dA}{dt} &= (1 - \rho)\sigma E - (\gamma_A + d)A \\ \frac{dI}{dt} &= \rho\sigma E - (\gamma_I + \mu + d)I \\ \frac{dR}{dt} &= \gamma_A A + \gamma_I I - (\delta_R + d)R \end{aligned} $$
決定的なのは、「感染力」として知られる個体が感染する速度、すなわち$\lambda(t)$は、それ自体が動的な要素であり、次のように定義されることである。
$$ \lambda(t) = \frac{\beta(\theta E + \epsilon A + I)}{N} $$
ここで、$N$は総人口を表し、8つのコンパートメントの全個体の合計である。$N(t) = S(t) + V(t) + S_1(t) + S_2(t) + E(t) + A(t) + I(t) + R(t)$。
項別解剖
これらの各方程式を詳細に検討し、各構成要素の意味と、それがなぜ存在するのかを理解しよう。これは、複雑な時計を分解して、各歯車とバネが全体の機能にどのように貢献しているかを見るようなものである。
コンパートメント変数(個体の「状態」)
- $S(t)$: 時間 $t$ における完全に感受性のある個体の数を示す。
- 数学的定義: ODEシステムの状態変数。
- 物理的/論理的役割: SARS-CoV-2に対する免疫がなく、感染しうる個体である。
- 変数である理由: 人々が出生、ワクチン接種、または感染するにつれて、その値は時間とともに変化する。
- $V(t)$: ワクチン接種を受け、完全に免疫のある個体の数である。
- 数学的定義: 状態変数。
- 物理的/論理的役割: ワクチンを接種し、現在保護されている個体である。
- $S_1(t)$: 免疫が初めて減衰した個体を示す。
- 数学的定義: 状態変数。
- 物理的/論理的役割: 一部の保護を失い、再び部分的に感受性を持つようになる。これは免疫減衰の第一段階である。
- 変数である理由: 人々が出生、ワクチン接種、または感染するにつれて、その値は時間とともに変化する。
- $S_2(t)$: 免疫がさらに減衰し、病原体と戦う能力が著しく低下した個体を表す。
- 数学的定義: 状態変数。
- 物理的/論理的役割: これらの個体は免疫力が非常に低く、感染しやすくなっている。これは免疫減衰の第二段階であり、より重度である。
- $E(t)$: 感染力を持つ曝露された個体の数である。
- 数学的定義: 状態変数。
- 物理的/論理的役割: 感染しているが、まだ自身が感染力を持たない個体(潜伏期間)。
- $A(t)$: 無症候性の感染個体を示す。
- 数学的定義: 状態変数。
- 物理的/論理的役割: 症状を示さないが、ウイルスを伝播させることができる感染個体である。
- $I(t)$: 症候性の感染個体の数である。
- 数学的定義: 状態変数。
- 物理的/論理的役割: 症状を示し、通常は感染力が高い感染個体である。
- $R(t)$: 回復し、完全に免疫のある個体の数を示す。
- 数学的定義: 状態変数。
- 物理的/論理的役割: 感染から回復し、一時的に完全な免疫を持つ個体である。
- $N(t)$: 時間 $t$ における総人口である。
- 数学的定義: 他のすべてのコンパートメント変数の合計。
- 物理的/論理的役割: 感染力の正規化に使用され、接触率が密度依存であることを示唆する。
- 合計である理由: システム内のすべての個体を集計する。
パラメータと係数(システムの「ルール」)
- $\Lambda$: 感受性のある個体の募集率(人/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: 感受性のある集団への新規参入を表す。通常は出生または移住である。
- 加算である理由: ソース項であり、$S$コンパートメントに個体を加える。
- $\beta$: 伝播率(1/日)。
- 数学的定義: 正の係数。時間変動する可能性もある($\beta(t)$)。
- 物理的/論理的役割: 感染性の人から感受性のある人へのウイルスの伝播の効率を決定する。
- 乗算である理由: 感染の全体的な速度をスケールし、伝播の「強度」係数として機能する。
- $\alpha$: ワクチン接種を受けた個体の割合(1/日)。
- 数学的定義: 正の係数。時間変動する可能性もある($\alpha(t)$)。
- 物理的/論理的役割: 感受性のある、$S_1$、および$S_2$の個体がワクチンを受け、$V$コンパートメントに移行する速度を表す。
- 乗算である理由: ワクチン接種コンパートメントへの個体の流れをスケールする。
- $d$: 人口の自然死亡率(1/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: 病気自体以外のすべての原因による死亡を表す。すべてのコンパートメントに適用される。
- 減算である理由: 各コンパートメントの人口を減少させる除去項である。
- $\mu$: 症候性の感染個体中の死亡率(1/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: これは、特に症候性の個体($I$)に影響を与える、病気による追加の死亡率である。
- 減算である理由: $I$コンパートメントからの追加の除去項である。
- $\delta_V$: $V$から$S_1$へのワクチン誘発性免疫減衰率(1/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: ワクチン接種を受けた個体が完全な免疫を失い、減衰した免疫の第一段階($S_1$)に移行する速度。
- 加算/減算である理由: コンパートメント間の個体の流れを決定する。
- $\delta_{S_1}$: $S_1$から$S_2$への免疫減衰率(1/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: $S_1$の個体がさらに免疫を失い、減衰した免疫の第二段階($S_2$)に移行する速度。
- 加算/減算である理由: コンパートメント間の個体の流れを決定する。
- $\delta_R$: $R$から$S_1$への自然免疫減衰率(1/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: 自然に回復した個体が完全な免疫を失い、$S_1$に移行する速度。
- 加算/減算である理由: コンパートメント間の個体の流れを決定する。
- $\epsilon_1$: $S_1$内の個体の感染に対する相対感受性(無次元)。
- 数学的定義: 正の定数係数、$0 \le \epsilon_1 \le 1$。
- 物理的/論理的役割: $S_1$個体の感染率を修正する。$\epsilon_1 < 1$の場合、完全に感受性のある個体よりも感受性が低い。
- 乗算である理由: $S_1$個体の感染力に対するスケール係数として機能する。
- $\epsilon_2$: $S_2$内の個体の感染に対する相対感受性(無次元)。
- 数学的定義: 正の定数係数、$0 \le \epsilon_2 \le 1$。
- 物理的/論理的役割: $\epsilon_1$と同様だが、$S_2$個体に対して。しばしば$\epsilon_2 > \epsilon_1$または$\epsilon_2 = 1$となり、より高い感受性を反映する。
- 乗算である理由: $S_2$個体の感染力に対するスケール係数として機能する。
- $\theta$: $E$の伝播確率の低下係数(無次元)。
- 数学的定義: 正の定数係数、$0 \le \theta \le 1$。
- 物理的/論理的役割: 症候性の個体よりも感染力が低い可能性があることを反映し、曝露された個体($E$)の感染力への寄与をスケールする。
- 乗算である理由: $E$の感染性寄与をスケールする。
- $\epsilon$: $A$の伝播確率の低下係数(無次元)。
- 数学的定義: 正の定数係数、$0 \le \epsilon \le 1$。
- 物理的/論理的役割: 無症候性の個体($A$)の感染力への寄与をスケールする。
- 乗算である理由: $A$の感染性寄与をスケールする。
- $\sigma$: $E$から感染個体への進行率(1/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: 曝露された個体が潜伏期間を完了し、感染力を持つようになる速度(無症候性または症候性)。
- 乗算である理由: $E$からの個体の流れをスケールする。
- $\rho$: 症候性の感染個体の割合(無次元)。
- 数学的定義: 正の定数係数、$0 \le \rho \le 1$。
- 物理的/論理的役割: $E$コンパートメントから離れる個体のうち、症候性($I$)になる割合を決定する。残りの割合($1-\rho$)が無症候性($A$)になる。
- 乗算である理由: $E$からの流れの分割係数として機能する。
- $\gamma_A$: 無症候性の感染個体の回復率(1/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: 無症候性の個体が回復し、免疫を獲得する速度。
- 乗算である理由: $A$からの個体の流れをスケールする。
- $\gamma_I$: 症候性の感染個体の回復率(1/日)。
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: 症候性の個体が回復し、免疫を獲得する速度。
- 乗算である理由: $I$からの個体の流れをスケールする。
数学演算子
- $d/dt$: 時間に関する微分。
- 数学的定義: 瞬時変化率を表す。
- 物理的/論理的役割: これらのODEでは、非常に短い時間間隔における各コンパートメントの個体数の変化を記述する。
- 微分である理由: モデルは人口サイズの連続的な変化を仮定しており、これは疫学的モデルにおける大規模人口の典型である。
- 加算($+$)と減算($-$):
- 数学的定義: 標準的な算術演算。
- 物理的/論理的役割: これらの演算子は、特定のコンパートメントへの個体の流れ(加算)またはからの流れ(減算)を表す。例えば、$\Lambda$は$S$に加算され、$\lambda(t)S$は$S$から減算される。
- 加算/減算である理由: これは、コンパートメントモデルにおける人口動態をモデル化し、増減を追跡するための基本的な方法である。
- 乗算($\times$または暗黙):
- 数学的定義: 標準的な算術演算。
- 物理的/論理的役割: 個体数の積に依存する率(例:感染率$\lambda(t)S$は感受性のある個体数と感染力の積に依存する)を計算したり、スケール係数を適用したりするために使用される(例:$\epsilon_1\lambda(t)S_1$)。
- 乗算である理由: これは「質量作用の原理」を反映しており、相互作用(感染など)の速度は相互作用する個体数の積に比例する。また、無次元のスケール係数を適用して率を修正する。
- 除算($/$):
- 数学的定義: 標準的な算術演算。
- 物理的/論理的役割: 感染力$\lambda(t)$において、$N$(総人口)で割ることは、感染性接触項を正規化する。
- 除算である理由: これは頻度依存性伝播を示唆しており、感染の確率は、感染性個体の絶対数ではなく、集団における感染性個体の割合に依存する。これは、大規模でよく混合された集団ではしばしばより現実的である。
ステップバイステップの流れ
単一の抽象的な個体、「データポイント」が、この複雑な免疫システムと疾患進行の機械的な組み立てラインを移動する様子を想像してみよう。
-
システムへの参入: 我々の個体は、感受性($S$)コンパートメントに「募集」されることから旅を始める。これは、新しい部品が工場に入ってくるようなものである。率$\Lambda$が毎日どれだけの新しい部品が到着するかを決定する。
-
初期選択($S$コンパートメント): $S$にいる間、我々の個体はいくつかの経路に直面する。
- ワクチン接種: 彼らは率$\alpha S$でワクチン接種を受ける可能性があり、これは直ちに彼らをワクチン接種済み($V$)コンパートメントに移動させ、完全な免疫を与える。
- 自然死: 彼らは非疾患原因で率$dS$で死亡し、システムから退出する可能性がある。
- 感染: 感染性の人($E$、$A$、または$I$から)に遭遇した場合、率$\lambda(t)S$で感染し、曝露($E$)コンパートメントに移動する。これが彼らがウイルスに「感染」した瞬間である。
-
潜伏($E$コンパートメント): $E$では、我々の個体はウイルスを潜伏させている。彼らは感染しているが、まだ効果的に広めることはできない。
- 進行: 潜伏期間の後、彼らは率$\sigma E$で感染状態に進行する。
- 自然死: 彼らは率$dE$で自然死する可能性もある。
-
感染力の獲得($A$または$I$コンパートメント): $E$から離れると、我々の個体は2つの感染経路のいずれかに「振り分け」られる。
- 無症候性($A$): 確率$(1-\rho)$で、彼らは無症候性になり、率$(1-\rho)\sigma E$で無症候性($A$)コンパートメントに移動する。ここでは、症状を示さずにウイルスを広めることができる。
- 症候性($I$): 確率$\rho$で、彼らは症候性になり、率$\rho\sigma E$で症候性($I$)コンパートメントに移動する。ここでは、症状を示し、通常はより感染力が高い。
-
感染期間と回復($A$および$I$コンパートメント):
- $A$から: 無症候性の個体は率$\gamma_A A$で回復し、回復済み($R$)コンパートメントに移動する。彼らはまた、率$dA$で自然死する可能性もある。
- $I$から: 症候性の個体は率$\gamma_I I$で回復し、これも$R$に移動する。しかし、彼らは追加のリスクに直面する。病気による死亡率$\mu I$、または自然死亡率$dI$である。
-
一時的な免疫($R$および$V$コンパートメント): $R$(回復済み)または$V$(ワクチン接種済み)に入ると、我々の個体は一時的な完全な免疫を楽しむ。しかし、この免疫は永遠ではない。
- $V$からの減衰: ワクチン接種を受けた個体は、率$\delta_V V$で免疫を失い、$S_1$(第一段階の減衰した免疫)コンパートメントに移行する。
- $R$からの減衰: 自然に回復した個体は、率$\delta_R R$で自然免疫を失い、これも$S_1$に移行する。
- 自然死: $V$または$R$の個体も、それぞれ率$dV$および$dR$で自然死する可能性がある。
-
免疫の低下($S_1$および$S_2$コンパートメント):
- $S_1$から: $S_1$の個体は部分的に減衰した免疫を持つ。彼らは次のことができる。
- 率$\alpha S_1$で再びワクチン接種を受け、$V$に戻る。
- 率$dS_1$で自然死する。
- 低下した率$\epsilon_1\lambda(t)S_1$で再感染し、$E$に戻る。
- 率$\delta_{S_1} S_1$でさらなる免疫減衰を経験し、$S_2$(第二段階の減衰した免疫)コンパートメントに移行する。
- $S_2$から: $S_2$の個体は著しく減衰した免疫を持つ。彼らは次のことができる。
- 率$\alpha S_2$で再びワクチン接種を受け、$V$に戻る。
- 率$dS_2$で自然死する。
- (潜在的に高い)低下した率$\epsilon_2\lambda(t)S_2$で再感染し、$E$に戻る。
- $S_1$から: $S_1$の個体は部分的に減衰した免疫を持つ。彼らは次のことができる。
これらの率に基づいて個体がコンパートメント間を移動するこの連続的な流れは、集団内の免疫と感染のライフサイクル全体を記述している。
最適化ダイナミクス
このモデルは、常微分方程式のシステムであるため、損失関数を最小化することによって機械学習アルゴリズムが行うのと同じ方法で「学習」したり「更新」したりしない。代わりに、その「ダイナミクス」とは、システムの状態が時間とともにどのように進化し、どのような安定または不安定なパターンに落ち着くかを指す。「最適化」とは、疾患が制御されるか持続する条件を理解することにある。
-
平衡状態への到達: システムの自然な傾向は、すべてのコンパートメントの変化率がゼロになる平衡点($dS/dt = 0, dV/dt = 0$など)に向かって進化することである。これらはシステムの「定常状態」である。
- 疾患フリー平衡(DFE): 曝露された、無症候性の、または症候性の個体が存在しない状態($E=A=I=0$)。疾患は消滅した。
- 風土病平衡(EE): 疾患が集団内に持続し、一定数(ゼロ以外)の感染個体が存在する状態である。
-
基本再生産数($R_0$): この単一の重要なパラメータは、システムの挙動の主要な「スイッチ」として機能する。これはモデルのパラメータから導出され、完全に感受性のある集団における1人の感染個体によって引き起こされる二次感染の平均数を示す。
- $R_0 < 1$の場合: 疾患フリー平衡は局所漸近安定である。これは、初期の感染個体数が十分に小さい場合、疾患は自然に消滅することを意味する。システムは疾患のない状態に「収束」する。
- $R_0 > 1$の場合: 疾患フリー平衡は不安定である。これは、疾患が広がり、風土病になる可能性があることを意味する。システムは疾患フリー状態から離れる。
-
分岐解析:システムの「相転移」: ここで、モデルの複雑なダイナミクスが真に輝く。分岐は、パラメータ(基本再生産数$R_0$に直接影響する伝播率$\beta$など)が変化するにつれて、システムの挙動の質的な変化を記述する。
- 前方分岐: 通常のシナリオでは、$R_0$が1を下から超えると、DFEは安定性を失い、安定な風土病平衡が出現する。これは、伝播が十分に高い場合、疾患が風土病になる「滑らかな」遷移である。
- 後方分岐: これはより複雑で懸念されるダイナミクスである。これは、$R_0 < 1$の場合でも、安定な風土病平衡が存在しうることを意味する。このような場合、基本再生産数が疾患が消滅すべきであることを示唆していても、疾患は持続する可能性がある。結果は初期の感染個体数に依存する(二安定性と呼ばれる現象)。これは公衆衛生にとって重要な洞察であり、初期感染レベルが高い場合、$R_0$を1未満に減らすだけでは疾患を根絶するには十分ではない可能性がある。
- 鞍節点分岐: これは、パラメータが変化するにつれて2つの平衡点(しばしば安定な風土病平衡と不安定な風土病平衡)が出現または消滅するときに発生する。論文では、これが前方分岐の拡張された枝に沿って発生する可能性があり、複雑な二安定ダイナミクスに寄与すると指摘している。
-
MCMCによるパラメータ推定: モデルのダイナミクスを現実世界のシナリオを反映させるために、著者は実際のCOVID-19データを使用してモデルを「トレーニング」または「適合」させる。彼らはマルコフ連鎖モンテカルロ(MCMC)アルゴリズムを採用して、時間変動する伝播率$\beta(t)$とワクチン接種率$\alpha(t)$を推定する。
- 仕組み: MCMCは確率分布からサンプルを生成する計算技術である。この文脈では、未知のパラメータ(様々な時点での$\beta(t)$と$\alpha(t)$、スプラインノードで表される)の新しい値を反復的に提案し、モデルの出力が観測された日々の新規確認症例とワクチン接種数にどれだけ適合するかに基づいてそれらを受け入れるか拒否する。
- データからの「学習」: 多くの反復を経て、MCMCアルゴリズムはパラメータ空間を探索し、最終的に観測データと最も一致するパラメータ値の分布に収束する。このプロセスにより、モデルは経験的証拠から基盤となる伝播とワクチン接種のダイナミクスを「学習」し、現実世界の疫病曲線を最もよく記述するようにパラメータを形成することができる。$\beta(t)$と$\alpha(t)$に区分的立方スプラインを使用することで、モデルは時間とともに非定常で進化する率に「学習」を適応させることができ、公衆衛生介入やウイルス変異株の変化の影響を捉えることができる。
本質的に、このモデルの「最適化ダイナミクス」は、単一の最適な解を見つけることではなく、可能な長期的な挙動(平衡状態)の範囲と、これらの挙動が主要なパラメータの変化とともにどのように変化するかを理解することであり、これは現実世界のデータへの適合によって情報が提供される。後方分岐と二安定性の存在は、疫病制御の複雑で時には直感に反する性質を強調している。
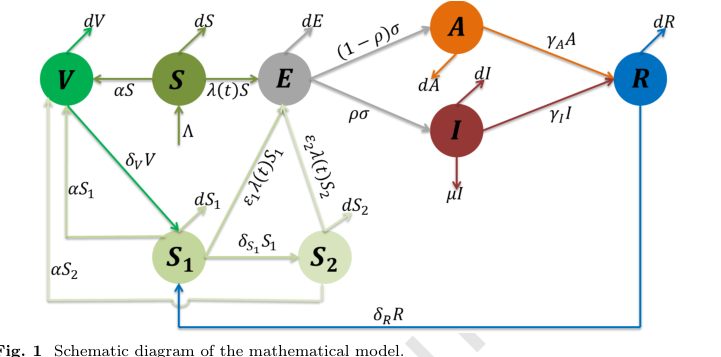 Figure 1. Schematic diagram of the mathematical model
Figure 1. Schematic diagram of the mathematical model
結果、限界、および結論
実験デザインとベースライン
著者らは、数学的主張を厳密に検証するため、提案された2段階免疫減衰モデル(システム(2))を実世界の疫学的データに適合させることに焦点を当てた実験を設計した。この文脈における主要な「犠牲者」あるいはベースラインは、直接的な比較対象となる代替モデルではなく、免疫低下の複雑で非線形な動態や時間変動する介入を捉えきれない、より単純な疫学的枠組みの固有の限界であった。モデルの有効性に関する決定的な証拠は、観察された流行傾向を正確に再現する能力にある。
実験設定では、2020年12月14日から2022年6月6日までの重要な期間を対象とした、米国からのCOVID-19サーベイランスデータを収集した。このデータセットには、日々の新規確認COVID-19症例数と日々の新規ワクチン接種者数が含まれていた。短期的な変動や周期的なパターンを軽減するため、生データに7日間移動平均を適用した。
設計の重要な側面は、主要パラメータの扱いである。感染率 $\beta(t)$ とワクチン接種率 $\alpha(t)$ は時間変動するものとみなされた。これらの動的なパラメータを推定するため、区分的多項式スプライン関数が用いられた。具体的には、$\beta(t)$ は18個のスプラインノードと30日間のノット間隔で近似され、$\alpha(t)$ はより急速な変動を考慮するため、36個のスプラインノードと短い15日間のノット間隔で近似された。その後、マルコフ連鎖モンテカルロ(MCMC)アルゴリズムを用いてパラメータ推定を行い、これらの時間変動パラメータや表4にリストされた他のパラメータの最適値を得た。このアプローチにより、モデルは新たな変異株や行動変容などの要因を間接的に考慮しながら、進化するパンデミックの状況に適応することができた。
証拠が示すもの
この証拠は、免疫低下の豊かな動態とそのSARS-CoV-2感染への影響を捉えるモデルの能力を強く支持している。最も説得力のある証明は、モデルのシミュレーションデータ(日々の新規確認症例数とワクチン接種者数)と、米国からの実際の観測データとの間の緊密な一致であり、これは図3に視覚的に示されている。この成功した適合は、2段階免疫減衰プロセスという中心的なメカニズムが、時間変動する感染率とワクチン接種率と組み合わさることで、現実世界で効果的に機能するという明白な証拠を提供する。
単なるデータ適合を超えて、数値シミュレーションは分岐ダイナミクスに関する理論的予測を厳密に検証した。
- 前方分岐と後方分岐: モデルは、$R_0 = 1$ において一貫して前方分岐と後方分岐の両方を示す。前方分岐は $R_0 > 1$ の場合に流行が安定化することを示唆するが、後方分岐の発生は重要な発見である。これは、特定のパラメータ条件下では、基本再生産数 $R_0 < 1$ の場合でも安定な定常状態が存在しうることを決定的に証明する。これは、 $R_0$ を1未満にしても、単純なモデルが示唆するよりも複雑な現実を浮き彫りにし、必ずしも疾患の根絶を保証するわけではないことを意味する。
- 二安定性と多安定性: 解析により、パラメータ値に応じて、ゼロ、1つ、2つ、あるいは3つの定常状態が共存しうる、二安定性または多安定性をシステムが示すことが明らかになった。これは、流行の長期的な結果(根絶か持続か)が、特に $R_0$ の特定の範囲内において、初期条件に非常に敏感である可能性を示唆している。
- 鞍点分岐: 数値シミュレーションはさらに、転換分岐の拡張された枝に沿って鞍点分岐が発生しうることを示した。この現象は2つの安定な定常状態の共存をもたらし、二安定性の概念を強化し、流行の軌跡が初期条件に基づいて異なる安定状態に収束しうることを示唆している。
さらに、主要パラメータの感度分析は、効果的な制御策に関する明確な洞察を提供した。
- 免疫減衰期間: 証拠は、二次的な免疫減衰(自然免疫およびワクチン誘発免疫の両方)の期間を延長することが、症候性感染者数を大幅に減らし、全体的な感染リスクを低下させることを明確に示している。
- ワクチン接種率: より高いワクチン接種率が、感染ピークを大幅に緩和し、全体的な感染リスクを低減させることが証明された。
- 相対的感受性: 相対的感受性(すなわち、より強い免疫)が低いほど、より有利な感染動態につながる。本研究では、相対的感受性 ($\epsilon_1$ および $\epsilon_2$) が高い場合、流行ピークはより早く、より重篤になる可能性があることが示された。逆に、中程度の値はピークを遅らせ、介入のための貴重な時間を提供することができる。ワクチン接種率の増加と相対的感受性の調整の組み合わせ効果は、感染ピークを低減させることが示された。
総じて、この証拠は、提案された2段階免疫減衰モデルがSARS-CoV-2の動態について、より微妙で正確な理解を提供し、流行制御における持続的な免疫、高いワクチン接種率、および感受性の低下の重要な役割を強調していることを証明している。
限界と今後の方向性
本研究は、免疫低下とそのSARS-CoV-2感染への影響を理解するための厳密な枠組みを提供する一方で、その固有の限界を認識し、将来の開発の方向性を検討することが重要である。
一つの重要な限界は、モデルの時間変動する感染率とワクチン接種率が、実世界のデータへの適合において効果的であるにもかかわらず、新たなウイルス変異株(例:デルタ株、オミクロン株)の出現、人間の行動の変化、非医薬品介入の実施といった複数の外部要因の影響を暗黙的に捉えていることである。しかし、モデルはこれらの要因の個々の寄与を区別することはできない。これは、何が起こったかはわかるが、特定の外部ドライバーの観点からなぜ起こったのかを正確にはわからないことを意味する。
さらに、現在のモデルは、様々なワクチンタイプやその異なる有効性を区別していない。また、集団内の行動の不均一性や感染伝播の空間構造も明示的に考慮していない。これらの単純化は、数学的な扱いやすさを助ける一方で、現実の疫学的シナリオの完全な複雑さを反映する上でのモデルの粒度を制限する。
今後、これらの発見をさらに発展させ、進化させるためのいくつかの議論のテーマが現れる。
- 外部要因の解明: 将来の研究では、特定のウイルス変異株、行動の変化、または非医薬品介入が感染率とワクチン接種率に与える影響を明示的にモデル化するために、サブモデルを開発したり、追加のデータストリームを組み込んだりすることに焦点を当てることができる。これにより、流行動態への個々の寄与をより詳細に理解することが可能になる。
- ワクチンの不均一性と有効性: 様々なワクチンプラットフォーム(例:mRNA、ウイルスベクター)とそれらの特定の減衰プロファイルおよび有効性を区別するようにモデルを進化させることは、個別化されたワクチン接種戦略のための生物学的現実性と予測力を大幅に向上させるだろう。
- 空間的および社会的動態: 空間的要素と行動の不均一性(例:公衆衛生措置への遵守のばらつき、社会ネットワーク構造)をモデルに統合することは、局所的なアウトブレイク、スーパー・スプレッディング・イベント、および地理的に標的化された介入の効果に関する洞察を提供する可能性がある。
- 長期的な免疫刷り込み: ワクチン誘発保護の長期化と集団レベルのカバレッジの重要性に関する本研究の発見は、免疫刷り込み効果のさらなる調査の必要性を強調している。進化する病原体に対して免疫応答の幅と持続性を最大化するワクチン接種スケジュールやブースター戦略をどのように設計できるか?
- 後方分岐と二安定性の政策的含意: $R_0 < 1$ でも流行が持続しうる(後方分岐による)こと、および結果が初期条件に依存しうる(二安定性)ことの証明は、公衆衛生政策にとって重大な課題を提示する。これは、$R_0$ を1未満に下げることへの単一の焦点から、初期条件、集団免疫の状況、および制御されているように見える環境でさえ再燃する可能性を考慮した、より動的で適応的な戦略への移行を必要とする。このような複雑なシステムを導くために、どのような新しい指標や閾値が必要か?
- 免疫減衰の経済的および社会的コスト: さらなる研究では、異なる免疫減衰率とワクチン接種戦略に関連する経済的および社会的コストを統合することができる。これにより、公衆衛生上の決定(より持続的なワクチンへの投資対頻繁なブースターキャンペーンなど)に関わるトレードオフについて、より包括的な理解が得られるだろう。
本分析から得られた洞察は、ワクチン接種戦略の最適化と、より持続的で効果的なワクチンの開発にとって極めて重要である。特に後方分岐と二安定性によって明らかになった複雑な動態は、流行制御が単純な線形問題ではなく、継続的な適応と免疫学的および疫学的相互作用の深い理解を必要とする多面的な課題であることを強調している。
他の体との同型
構造的骨格
中心的なメカニズムは、状態間のエンティティの流れと変換をモデル化するマルチコンパートメント動的システムであり、主要なレートパラメータに基づいた分岐や二安定性のような複雑な非線形挙動を示す。
