Богатая динамика и анализ данных иммунного спада против SARS-CoV-2
Точное происхождение данной проблемы напрямую связано с глобальной пандемией SARS CoV 2 и последующими широкомасштабными усилиями по вакцинации.
Предпосылки и академическая преемственность
Происхождение и академическая преемственность
Точное происхождение данной проблемы напрямую связано с глобальной пандемией SARS-CoV-2 и последующими широкомасштабными усилиями по вакцинации. По мере развития пандемии стало ясно, что как естественное заражение, так и вакцинация обеспечивают иммунную защиту, но эта защита не была постоянной и, что особенно важно, не снижалась с постоянной или линейной скоростью (строки 13-15). Это наблюдение создало значительную проблему для точного моделирования долгосрочной траектории эпидемии и для разработки эффективных мер общественного здравоохранения. Исторический контекст коренится в необходимости понять, как иммунитет к SARS-CoV-2 ослабевал со временем, приводя к прорывным инфекциям и компрометируя долгосрочную защитную эффективность вакцин (строки 45-47).
Фундаментальное ограничение или «болевая точка» предыдущих подходов была двоякой. Во-первых, более ранние модели либо чрезмерно упрощали ослабление иммунитета (например, постоянный или линейный спад), либо, пытаясь уловить наблюдаемую сложность, становились «чрезвычайно сложными, что затрудняло систематический теоретический анализ» (строки 112-114). Эти сложные модели часто сильно полагались на численные симуляции для изучения стратегий контроля или исследования явлений бифуркации в изолированных условиях (строки 114-116). Эта зависимость от численных методов, а не от систематического теоретического анализа, препятствовала всестороннему и управляемому пониманию лежащей в основе динамики. Таким образом, авторы были вынуждены разработать «относительно простую, но биологически значимую модель, которая улавливает нелинейную динамику, возникающую из-за ослабления иммунитета» (строки 116-118), чтобы преодолеть эти аналитические проблемы и предоставить более управляемую основу для изучения иммунного спада и его влияния на передачу заболеваний.
Интуитивные термины предметной области
- Ослабление иммунитета (Immune Waning): Это относится к постепенному снижению защитного иммунитета человека к заболеванию с течением времени, независимо от того, был ли этот иммунитет приобретен в результате прошлой инфекции или вакцины.
- Аналогия: Представьте, что батарея вашего телефона медленно теряет заряд после полной зарядки. Защита вашего организма не просто отключается; она медленно угасает, делая вас снова более уязвимым для инфекции.
- Обратная бифуркация (Backward Bifurcation): В моделировании заболеваний это своеобразная ситуация, когда заболевание может сохраняться и становиться эндемическим, даже когда базовое репродуктивное число ($R_0$) меньше 1. Обычно $R_0 < 1$ означает, что заболевание должно естественным образом исчезнуть.
- Аналогия: Представьте тяжелый шар на слегка наклонной поверхности. Если вы дадите ему небольшой толчок, он может откатиться туда, откуда начал. Но если вы дадите ему достаточно сильный начальный толчок, он может перекатиться через небольшой выступ и застрять в углублении дальше по склону, даже несмотря на то, что общий наклон предполагает, что он должен был откатиться назад. Это явление также встречалось и в других областях. Начальный «импульс» (количество инфицированных людей) может определить, «застрянет» ли болезнь в эндемическом состоянии.
- Базовое репродуктивное число ($R_0$) (Basic Reproduction Number): Это критически важное число, представляющее собой среднее количество новых инфекций, вызванных одним инфицированным человеком в полностью восприимчивой популяции.
- Аналогия: Рассмотрите новый вирусный танцевальный тренд. Если один человек обучает ему, в среднем, более одного нового человека ($R_0 > 1$), танец распространяется. Если он обучает менее одного нового человека ($R_0 < 1$), тренд в конечном итоге угасает.
- Эндемическое равновесие (Endemic Equilibrium): Это относится к стабильному состоянию в эпидемии, когда заболевание постоянно присутствует в популяции, но количество инфицированных людей остается относительно постоянным с течением времени, не увеличиваясь быстро и не исчезая.
- Аналогия: Представьте реку с постоянным течением. Вода всегда движется, но общий уровень воды и скорость течения остаются прежними. Болезнь всегда присутствует, но ее проявление предсказуемо и стабильно, а не внезапный всплеск или полное отсутствие.
Таблица обозначений
| Обозначение | Описание (Единицы измерения) |
|---|---|
| $S(t)$ | Число полностью восприимчивых индивидов (чел.) |
| $V(t)$ | Число вакцинированных и полностью иммунных индивидов (чел.) |
| $S_1(t)$ | Число индивидов с ослабленным иммунитетом первой стадии (чел.) |
| $S_2(t)$ | Число индивидов с ослабленным иммунитетом второй стадии (чел.) |
| $E(t)$ | Число инкубационных индивидов (чел.) |
| $A(t)$ | Число бессимптомных инфицированных индивидов (чел.) |
| $I(t)$ | Число симптоматических инфицированных индивидов (чел.) |
| $R(t)$ | Число выздоровевших и полностью иммунных индивидов (чел.) |
| $N(t)$ | Общая численность населения (чел.) |
| $\Lambda$ | Скорость притока восприимчивых индивидов (чел./день) |
| $\beta$ | Коэффициент передачи (1/день) |
| $\alpha$ | Скорость вакцинации (1/день) |
| $d$ | Скорость естественной смертности (1/день) |
| $\mu$ | Скорость смертности от заболевания у симптоматических инфицированных (1/день) |
| $\delta_V$ | Скорость ослабления вакцинального иммунитета ($V \to S_1$) (1/день) |
| $\delta_{S_1}$ | Скорость ослабления иммунитета ($S_1 \to S_2$) (1/день) |
| $\delta_R$ | Скорость ослабления естественного иммунитета ($R \to S_1$) (1/день) |
| $\epsilon_1$ | Относительная восприимчивость индивидов в $S_1$ (безразмерная) |
| $\epsilon_2$ | Относительная восприимчивость индивидов в $S_2$ (безразмерная) |
| $\theta$ | Коэффициент снижения передачи инфекции индивидами в $E$ (безразмерный) |
| $\epsilon$ | Коэффициент снижения передачи инфекции индивидами в $A$ (безразмерный) |
| $\sigma$ | Скорость перехода из $E$ в инфицированное состояние (1/день) |
| $\rho$ | Доля симптоматических инфицированных индивидов (безразмерная) |
| $\gamma_A$ | Скорость выздоровления бессимптомных инфицированных (1/день) |
| $\gamma_I$ | Скорость выздоровления симптоматических инфицированных (1/день) |
Определение проблемы и ограничения
Формулировка основной проблемы и дилемма
Основная проблема, рассматриваемая в данной статье, вытекает из сложного и нелинейного характера ослабления иммунитета против SARS-CoV-2.
Входные данные/Текущее состояние:
В начале мы имеем индивидов, которые приобрели определенный уровень иммунной защиты от SARS-CoV-2, будь то в результате естественного заражения или вакцинации. Однако текущее понимание и моделирование этого иммунитета недостаточны в нескольких ключевых аспектах:
1. Нелинейное ослабление: Эффективность иммунитета не снижается с постоянной или линейной скоростью. Вместо этого иммунитет ослабевает со временем более сложным, нелинейным образом (резюме, строки 14-15).
2. Сложность модели против реализма: Существующие эпидемиологические модели, пытающиеся уловить ослабление иммунитета, часто впадают в две крайности: либо они слишком упрощены (например, предполагают линейный спад), либо они чрезвычайно сложны (например, модели с учетом возраста, модели с индивидуальными скоростями ослабления или отдельные отсеки для вакцинированных/выздоровевших). Эта сложность делает систематический теоретический анализ, такой как понимание динамики бифуркации, чрезвычайно трудным и часто требует опоры на численные симуляции в изолированных условиях (введение, строки 65-78, 112-116, 445-447).
3. Неполная характеристика динамики: Предыдущие модели с трудом полностью характеризуют динамический процесс иммунитета, особенно такие явления, как обратная бифуркация, когда заболевание может сохраняться, даже если базовое репродуктивное число ($R_0$) меньше единицы (введение, строки 90-91, 96-102). Это означает, что простое снижение $R_0$ ниже 1 может быть недостаточно для искоренения заболевания, что создает серьезную проблему для стратегий общественного здравоохранения.
Желаемое конечное состояние (выход/цель):
Статья направлена на разработку новой математической модели, которая может:
1. Охватить двухэтапное ослабление: Точно охарактеризовать динамический процесс иммунитета, включая более биологически реалистичный «двухэтапный механизм ослабления иммунитета» (резюме, строки 15-16; введение, строки 120-122). Это означает моделирование начального периода сильного иммунитета, за которым следует более быстрый спад.
2. Достичь простоты и управляемости: Быть «относительно простой, но биологически значимой» (введение, строки 116-118) и сохранять «математическую управляемость» (обсуждение, строки 449-450). Этот баланс имеет решающее значение для обеспечения строгого теоретического анализа, включая всесторонний анализ бифуркации.
3. Информировать стратегии общественного здравоохранения: Предоставить научную основу для разработки более эффективных стратегий и политик общественного здравоохранения путем изучения иммунологических механизмов, лежащих в основе инфекции SARS-CoV-2, и влияния мер контроля (введение, строки 48-51, 118-119).
Упущенное звено/Математический пробел:
Точным упущенным звеном является математически управляемая компартментная модель, которая явно включает нелинейный, двухэтапный механизм ослабления иммунитета для SARS-CoV-2, позволяющий проводить строгий теоретический анализ сложных динамических поведений (таких как бифуркации и бистабильность) и надежную оценку параметров с использованием реальных эпидемиологических данных. Предыдущие модели либо чрезмерно упрощали процесс ослабления, либо становились слишком сложными для всестороннего теоретического анализа, оставляя пробел в понимании полных динамических последствий ослабления иммунитета.
Дилемма:
Центральная дилемма, которая поставила в тупик предыдущих исследователей, — это компромисс между биологической реалистичностью и математической управляемостью. Чтобы точно отразить нюансы ослабления иммунитета (например, индивидуальную гетерогенность, возрастную структуру, нелинейный спад), модели имеют тенденцию становиться чрезвычайно сложными. Однако эта сложность часто делает их аналитически неуправляемыми, вынуждая исследователей полагаться исключительно на численные симуляции для конкретных сценариев. Данная статья пытается устранить этот пробел, вводя специфический двухэтапный механизм ослабления, который является биологически значимым, но достаточно простым для строгого математического анализа, включая вывод базового репродуктивного числа и всесторонний анализ бифуркации (обсуждение, строки 448-450).
Ограничения и возможные сбои
Проблема моделирования ослабления иммунитета при SARS-CoV-2 невероятно сложна из-за нескольких жестких, реалистичных стен, с которыми сталкиваются авторы:
- Нелинейное и гетерогенное ослабление иммунитета: Эффективность иммунитета не снижается с постоянной или линейной скоростью (резюме, строки 14-15). Вместо этого иммунитет ослабевает со временем, приводя к гетерогенности восприимчивости к повторному заражению. Индивиды обычно сохраняют высокую защиту в течение начального периода, но затем уровни антител и защитная эффективность заметно снижаются, в конечном итоге приближаясь к исчезновению (введение, строки 105-111). Этот сложный биологический процесс должен быть точно представлен.
- Возникновение механизмов уклонения от иммунитета: Вирус эволюционирует, и возникают механизмы уклонения от иммунитета, что компрометирует долгосрочную защитную эффективность вакцин и естественного иммунитета (введение, строки 46-47). Хотя это явно не моделируется как механизм, эта биологическая реальность подчеркивает необходимость динамической модели, которая может адаптироваться к меняющимся иммунным ландшафтам.
- Эпидемиологические параметры, изменяющиеся во времени: Ключевые параметры, такие как коэффициент передачи ($\beta(t)$) и коэффициент вакцинации ($\alpha(t)$), не являются постоянными, а значительно меняются со временем. Эти изменения зависят от множества внешних факторов, включая появление новых вариантов (например, Дельта, Омикрон), изменения в поведении и применение немедикаментозных мер вмешательства (обсуждение, строки 491-493). Это делает модели со статическими параметрами недостаточными и требует методов оценки зависящих от времени параметров.
- Проблемы оценки параметров на основе данных: Модель должна быть подогнана к реальным, зашумленным эпидемиологическим данным (например, ежедневные новые подтвержденные случаи COVID-19, ежедневные новые дозы вакцин) в течение длительных периодов (например, с декабря 2020 г. по июнь 2022 г. в США). Это требует надежных статистических методов, таких как Марковские цепи Монте-Карло (MCMC), в сочетании с кусочно-кубическими сплайновыми функциями для учета изменяющегося во времени характера и присущей неопределенности данных (резюме, строки 25-26; обсуждение, строки 473-474).
- Математическая управляемость для анализа бифуркации: Цель состоит в проведении строгого теоретического анализа, включая вывод базового репродуктивного числа и всесторонний анализ бифуркации, для понимания сложных динамических поведений, таких как прямые и обратные бифуркации, а также сосуществование нескольких эндемических равновесий (резюме, строки 17-22; обсуждение, строки 449-450). Это накладывает строгое ограничение на сложность модели, поскольку чрезмерно сложные модели быстро становятся аналитически неуправляемыми.
- Обеспечение стабильности и реалистичности модели: Модель должна гарантировать, что компартменты популяции остаются ограниченными и неотрицательными, что является фундаментальным требованием для любой реалистичной эпидемиологической модели (вывод модели, строки 144-145; инвариантные области, лемма 1, строки 184-187). Это математическое ограничение гарантирует, что выходные данные модели биологически осмысленны.
- Интерпретация сложных явлений бифуркации: Модель выявляет сложное динамическое поведение, такое как бифуркации седло-узла и бистабильность, когда несколько стабильных эндемических равновесий могут сосуществовать. Это означает, что заболевание может сохраняться даже при $R_0 < 1$, что является критическим выводом, бросающим вызов традиционным стратегиям общественного здравоохранения и требующим тщательной интерпретации (резюме, строки 19-22; обсуждение, строки 461-467). Понимание этих явлений требует строгого математического доказательства и численного подтверждения.
Почему этот подход
Неизбежность выбора
Решение авторов разработать новую модель двухэтапного ослабления иммунитета было не случайным, а прямым ответом на присущие ограничения традиционных эпидемиологических моделей при столкновении со сложной динамикой иммунитета к SARS-CoV-2. Осознание того, что стандартные «SOTA» (State-of-the-Art) эпидемиологические методы были недостаточны, вытекало из нескольких критических наблюдений относительно вируса и иммунных ответов человека:
Во-первых, стало ясно, что иммунная защита, будь то от естественного заражения или вакцинации, «не снижается с постоянной или линейной скоростью» (резюме, строки 14-15). Это немедленно сделало базовые модели SIRS (восприимчивый-инфицированный-выздоровевший-восприимчивый), которые часто предполагают простой, непрерывный спад иммунитета, неадекватными для улавливания тонкого биологического процесса. Реальность «прорывных инфекций в течение короткого периода [7]» и «возникновение механизмов уклонения от иммунитета [8]» (введение, строки 45-48) еще больше подчеркнула необходимость более динамичного и многогранного представления ослабления иммунитета.
Во-вторых, ключевым выводом стало явление обратной бифуркации, когда «$R_0 < 1$ не обязательно гарантирует искоренение заболевания» (введение, строки 91-92). Традиционные модели фундаментально предполагают, что если базовое репродуктивное число ($R_0$) падает ниже 1, эпидемия естественным образом вымрет. Однако наблюдаемое сохранение SARS-CoV-2, даже в сценариях, где $R_0$ может быть ниже этого порога, выявило критический недостаток в этих более простых рамках. Модель авторов явно улавливает эту сложную динамику, демонстрируя, что «эпидемия может сохраняться даже при базовом репродуктивном числе $R_0 < 1$» (резюме, строки 21-22), что более простые модели не могут объяснить.
Наконец, хотя существующие передовые модели начали включать аспекты ослабления иммунитета (например, [17, 18, 19]), многие были «чрезвычайно сложными, что затрудняло систематический теоретический анализ» и часто полагались «на численные симуляции для изучения стратегий контроля или исследования явлений бифуркации в изолированных условиях» (введение, строки 112-115). Авторы явно стремились «устранить эти ограничения», ища модель, которая была бы «относительно простой, но биологически значимой» (введение, строки 115-117), чтобы обеспечить строгий теоретический анализ, который часто компрометировался чрезмерной сложностью других подходов. Эта потребность в балансе между биологической реалистичностью и математической управляемостью укрепила выбор их специфической двухэтапной компартментной структуры.
Сравнительное превосходство
Качественное превосходство данной модели двухэтапного ослабления иммунитета, помимо простых метрик производительности, заключается в ее структурных преимуществах, которые позволяют ей улавливать сложные эпидемиологические реалии, сохраняя при этом аналитическую строгость.
- Биологически реалистичное ослабление иммунитета: Наиболее значительным структурным преимуществом является явное введение двух отдельных компартментов, $S_1(t)$ и $S_2(t)$, представляющих индивидов с «частично и далее ослабленным иммунитетом» (введение, строки 120-127). Это позволяет модели выйти за рамки упрощенного линейного спада, характеризуя иммунитет как «нелинейный переход от полностью иммунных к частично иммунным состояниям» (обсуждение, строки 448-449). Этот многоэтапный подход является более точным отражением биологического процесса, при котором защита постепенно и гетерогенно ослабевает со временем, а не равномерный, непрерывный спад.
- Надежный анализ бифуркации и бистабильность: Структура модели облегчает строгий вывод и анализ как прямых, так и обратных бифуркаций (резюме, строки 17-18; обсуждение, строки 454-455). Способность продемонстрировать обратную бифуркацию является критическим качественным скачком, поскольку она объясняет, почему «$R_0 < 1$ не обязательно гарантирует искоренение заболевания» (введение, строки 91-92). Это означает, что заболевание может стать эндемическим, даже когда традиционные метрики предполагают, что оно должно исчезнуть. Более того, модель выявляет «сосуществование нескольких эндемических равновесий» и «бистабильность» (резюме, строки 18-22; обсуждение, строки 458-469), что подразумевает, что долгосрочная траектория эпидемии может быть крайне чувствительна к начальным условиям, — уровень динамической сложности, который более простые модели не могут достичь.
- Математическая управляемость для глубоких выводов: В отличие от многих «чрезвычайно сложных» существующих моделей, которые «часто полагаются на численные симуляции» (введение, строки 112-113), эта двухэтапная модель разработана как «относительно простая, но биологически значимая» (введение, строки 115-117). Этот структурный выбор позволяет «строго вывести базовое репродуктивное число и провести всесторонний анализ бифуркации» (обсуждение, строки 449-451). Этот баланс является ключевым преимуществом, обеспечивая глубокие теоретические выводы о механизмах, лежащих в основе динамики эпидемий, а не просто описательные симуляции.
- Интеграция реальных данных, изменяющихся во времени: Модель включает изменяющиеся во времени коэффициенты передачи $\beta(t)$ и вакцинации $\alpha(t)$, оцененные с использованием кусочно-кубических сплайновых функций и алгоритма MCMC (обсуждение, строки 470-473). Это позволяет модели адаптироваться к реальным эпидемиологическим данным и меняющимся стратегиям вмешательства, предоставляя более динамичную и применимую основу, чем модели, основанные на статичных параметрах.
Статья не затрагивает вычислительные сложности, такие как сокращение памяти с $O(N^2)$ до $O(N)$ или обработка высокоразмерного шума в контексте алгоритмов машинного обучения. Ее превосходство, напротив, коренится в улучшенной эпидемиологической реалистичности и аналитической мощности для понимания распространения заболеваний.
Соответствие ограничениям
Выбранная модель двухэтапного ослабления иммунитета идеально соответствует неявным ограничениям, вытекающим из определения проблемы, создавая прочный «союз» между сложностями динамики SARS-CoV-2 и уникальными свойствами решения.
- Ограничение: Точное представление ослабления иммунитета: Проблема требует модели, которая признает, что «эффективность иммунитета не снижается с постоянной или линейной скоростью» и что иммунитет «имеет тенденцию ослабевать со временем, приводя к гетерогенности восприимчивости к повторному заражению» (резюме, строки 14-15; введение, строки 105-106). Уникальным свойством решения является «двухэтапный механизм ослабления иммунитета» (резюме, строка 16), который явно вводит компартменты для «частично и далее ослабленного иммунитета» ($S_1(t)$ и $S_2(t)$) (введение, строки 120-127). Это напрямую решает проблему нелинейного и гетерогенного характера ослабления иммунитета, обеспечивая более точное и нюансированное биологическое представление.
- Ограничение: Объяснение сложного сохранения эпидемии: Критическим требованием является объяснение наблюдаемого сохранения SARS-CoV-2, даже когда традиционные индикаторы предполагают искоренение. Способность модели демонстрировать «прямые и обратные бифуркации» и «бистабильность» (резюме, строки 17-22; обсуждение, строки 454-469) идеально подходит. Обратная бифуркация, в частности, показывает, что «$R_0 < 1$ не обязательно гарантирует искоренение заболевания» (введение, строки 91-92), позволяя эпидемии сохраняться. Это напрямую устраняет расхождение между простыми предсказаниями модели и реальными наблюдениями.
- Ограничение: Математическая управляемость для политических выводов: Необходимость модели, которая является одновременно реалистичной и поддающейся строгому теоретическому анализу, имеет первостепенное значение для информирования стратегий общественного здравоохранения. В то время как многие существующие модели «чрезвычайно сложны, что затрудняет систематический теоретический анализ» (введение, строки 112-113), эта двухэтапная модель разработана как «относительно простая, но биологически значимая» (введение, строки 115-117). Это позволяет «строго вывести базовое репродуктивное число и провести всесторонний анализ бифуркации» (обсуждение, строки 449-451), предоставляя четкие, действенные выводы, которые могут быть затуманены чрезмерно сложными, неуправляемыми моделями.
- Ограничение: Параметризация на основе данных и динамическая параметризация: Эффективное моделирование быстро развивающейся пандемии требует возможности включать реальные данные и учитывать изменяющиеся во времени факторы. Использование решения алгоритма «MCMC в сочетании с кусочно-кубическими сплайновыми функциями» для оценки изменяющихся во времени коэффициентов передачи $\beta(t)$ и вакцинации $\alpha(t)$ из «эпидемиологических данных по COVID-19 из США» (резюме, строки 23-25; обсуждение, строки 470-473) идеально соответствует этому ограничению. Эта динамическая параметризация повышает релевантность модели и ее предсказательную силу для контроля эпидемий в реальном времени.
Этот подход эффективно устраняет разрыв между биологической сложностью и аналитической осуществимостью, делая его идеальным инструментом для понимания и управления SARS-CoV-2.
Отклонение альтернатив
Статья, будучи сосредоточенной на компартментном эпидемиологическом моделировании, не обсуждает и не отвергает подходы глубокого обучения, такие как GANs или диффузионные модели, поскольку они выходят за рамки ее сферы. Однако она косвенно отвергает или подчеркивает ограничения других эпидемиологических альтернативных моделей:
-
Стандартные модели SIR/SIRS: Эти основополагающие модели косвенно считаются недостаточными из-за их неспособности уловить специфическую сложность иммунитета к SARS-CoV-2.
- Модели SIR: Они предполагают пожизненный иммунитет (введение, строки 53-54), что явно неверно для SARS-CoV-2, где иммунитет ослабевает.
- Базовые модели SIRS: Хотя они учитывают ослабление иммунитета, они часто упрощают его до «постоянной или линейной скорости» (резюме, строки 14-15) или простого, непрерывного спада (обсуждение, строки 445-446). Работа авторов напрямую противоречит этому, показывая, что «двухэтапный механизм ослабления иммунитета» необходим для отражения «нелинейного перехода от полностью иммунных к частично иммунным состояниям» (обсуждение, строки 448-449).
- Неспособность объяснить обратную бифуркацию: Критической причиной отказа от этих более простых моделей является их неспособность объяснить такие явления, как обратная бифуркация, когда эпидемия может сохраняться, даже если базовое репродуктивное число $R_0 < 1$ (резюме, строки 21-22; обсуждение, строки 462-469). Стандартные модели SIRS предсказывали бы искоренение в таких условиях, делая их неадекватными для SARS-CoV-2.
-
Чрезмерно сложные существующие эпидемиологические модели: Статья также подразумевает отказ от моделей, которые, пытаясь уловить больше деталей, становятся аналитически неуправляемыми. Авторы отмечают, что «большинство существующих моделей чрезвычайно сложны, что затрудняет систематический теоретический анализ. Эти исследования часто полагаются на численные симуляции для изучения стратегий контроля или исследования явлений бифуркации в изолированных условиях.» (введение, строки 112-115). Это предполагает, что, хотя эти модели (например, те, что с непрерывными функциями ослабления, индивидуальными скоростями или многочисленными отдельными компартментами, как указано в обсуждении, строки 445-447) могут предлагать детальную информацию, их сложность препятствует строгому теоретическому анализу и всесторонним исследованиям бифуркации, которые авторы ставят во главу угла. Выбранная двухэтапная модель, напротив, «обеспечивает более простую и биологически интерпретируемую основу», позволяя при этом «строго вывести базовое репродуктивное число и провести всесторонний анализ бифуркации» (обсуждение, строки 448-451). Это подчеркивает сознательный выбор избегать моделей, которые жертвуют аналитической глубиной ради чрезмерной, потенциально непроверяемой детализации.
По сути, авторы отвергли альтернативы, которые были либо слишком упрощены, чтобы отразить наблюдаемую нелинейную иммунную динамику и сложные явления бифуркации SARS-CoV-2, либо слишком сложны, чтобы допустить желаемый уровень строгого теоретического анализа и понимания механизмов. Их двухэтапная модель обеспечивает прагматичный баланс, предлагая достаточную биологическую реалистичность, не становясь аналитически неуправляемой.
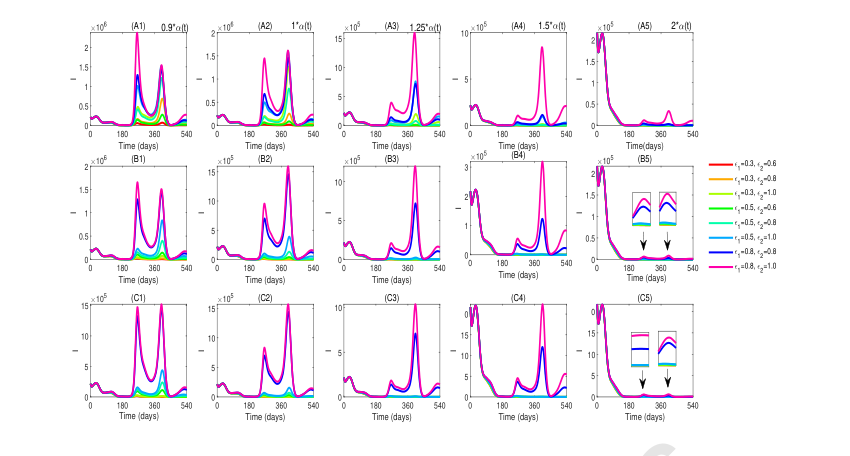 Figure 5. The impact of different vaccination rates, duration of secondary waning immunity, and two relative susceptibilities on disease transmission dynamics. By combining ε1 = 0.3, 0.5, 0.8 and ε2 = 0.6, 0.8, 1 in all possible pairwise combinations, we derive situations in which two relative suscep- tibilities change concurrently. (A1)-(C1), (A2)-(C2), (A3)-(C3), (A4)-(C4), and (A5)-(C5) correspond to multiples of the original vaccination rate of 0.9, 1, 1.25, 1.5, and 2, respectively. The figures are arranged into five columns based on different multiples of the original vaccination rate in the model and into three rows according to different immune waning durations. The durations of the secondary waning immunity 1 δV + 1 δS1 = 1 δR + 1 δS1 = 180, 365, 540 days, respectively, corresponds to (A1)-(A5),
Figure 5. The impact of different vaccination rates, duration of secondary waning immunity, and two relative susceptibilities on disease transmission dynamics. By combining ε1 = 0.3, 0.5, 0.8 and ε2 = 0.6, 0.8, 1 in all possible pairwise combinations, we derive situations in which two relative suscep- tibilities change concurrently. (A1)-(C1), (A2)-(C2), (A3)-(C3), (A4)-(C4), and (A5)-(C5) correspond to multiples of the original vaccination rate of 0.9, 1, 1.25, 1.5, and 2, respectively. The figures are arranged into five columns based on different multiples of the original vaccination rate in the model and into three rows according to different immune waning durations. The durations of the secondary waning immunity 1 δV + 1 δS1 = 1 δR + 1 δS1 = 180, 365, 540 days, respectively, corresponds to (A1)-(A5),
Математический и логический механизм
Основное уравнение
Ядром анализа данной статьи является система из восьми связанных обыкновенных дифференциальных уравнений (ОДУ), описывающих динамический поток индивидов между различными состояниями здоровья и иммунитета в популяции. Эта система, обозначенная как (2) в статье, является математическим двигателем, который моделирует распространение и контроль SARS-CoV-2, включая двухэтапный механизм ослабления иммунитета.
$$ \begin{aligned} \frac{dS}{dt} &= \Lambda - \lambda(t)S - (\alpha + d)S \\ \frac{dV}{dt} &= \alpha(S + S_1 + S_2) - (\delta_V + d)V \\ \frac{dS_1}{dt} &= \delta_V V + \delta_R R - \epsilon_1\lambda(t)S_1 - (\alpha + \delta_{S_1} + d)S_1 \\ \frac{dS_2}{dt} &= \delta_{S_1} S_1 - \epsilon_2\lambda(t)S_2 - (\alpha + d)S_2 \\ \frac{dE}{dt} &= \lambda(t)S + \epsilon_1\lambda(t)S_1 + \epsilon_2\lambda(t)S_2 - (\sigma + d)E \\ \frac{dA}{dt} &= (1 - \rho)\sigma E - (\gamma_A + d)A \\ \frac{dI}{dt} &= \rho\sigma E - (\gamma_I + \mu + d)I \\ \frac{dR}{dt} &= \gamma_A A + \gamma_I I - (\delta_R + d)R \end{aligned} $$
Важно отметить, что скорость, с которой индивиды заражаются, известная как «сила инфекции», $\lambda(t)$, сама по себе является динамическим компонентом, определяемым как:
$$ \lambda(t) = \frac{\beta(\theta E + \epsilon A + I)}{N} $$
Здесь $N$ представляет собой общую численность населения, которая является суммой всех индивидов во всех восьми компартментах: $N(t) = S(t) + V(t) + S_1(t) + S_2(t) + E(t) + A(t) + I(t) + R(t)$.
Покомпонентный анализ
Давайте разберем эти уравнения по частям, чтобы понять, что означает каждый компонент и почему он там находится. Представьте это как разборку сложного часового механизма, чтобы увидеть, как каждая шестеренка и пружина способствует его общей работе.
Переменные компартментов («Состояния» индивидов)
- $S(t)$: Это представляет собой количество полностью восприимчивых индивидов в момент времени $t$.
- Математическое определение: Переменная состояния в системе ОДУ.
- Физическая/логическая роль: Это индивиды, не имеющие иммунитета к SARS-CoV-2 и способные заразиться.
- Почему это переменная: Ее значение меняется со временем по мере рождения, вакцинации или заражения людей.
- $V(t)$: Это количество вакцинированных и полностью иммунных индивидов.
- Математическое определение: Переменная состояния.
- Физическая/логическая роль: Индивиды, получившие вакцину и в настоящее время защищенные.
- $S_1(t)$: Это обозначает индивидов, чей иммунитет ослаб впервые.
- Математическое определение: Переменная состояния.
- Физическая/логическая роль: Они потеряли некоторую защиту, что снова сделало их частично восприимчивыми. Это первая стадия ослабления иммунитета.
- $S_2(t)$: Это представляет собой количество индивидов, чей иммунитет ослаб еще сильнее, что привело к заметному снижению их способности бороться с патогенами.
- Математическое определение: Переменная состояния.
- Физическая/логическая роль: Эти индивиды имеют очень низкий иммунитет, что делает их очень восприимчивыми. Это вторая, более тяжелая стадия ослабления иммунитета.
- $E(t)$: Это количество инкубационных индивидов с инфекционным потенциалом.
- Математическое определение: Переменная состояния.
- Физическая/логическая роль: Индивиды, которые были инфицированы, но еще не стали заразными сами (инкубационный период).
- $A(t)$: Это обозначает количество бессимптомных инфицированных индивидов.
- Математическое определение: Переменная состояния.
- Физическая/логическая роль: Инфицированные индивиды, у которых нет симптомов, но они все еще могут передавать вирус.
- $I(t)$: Это количество симптоматических инфицированных индивидов.
- Математическое определение: Переменная состояния.
- Физическая/логическая роль: Инфицированные индивиды, у которых проявляются симптомы и которые обычно очень заразны.
- $R(t)$: Это представляет собой количество выздоровевших и полностью иммунных индивидов.
- Математическое определение: Переменная состояния.
- Физическая/логическая роль: Индивиды, которые выздоровели после инфекции и имеют временный полный иммунитет.
- $N(t)$: Это общая численность населения в момент времени $t$.
- Математическое определение: Сумма всех других переменных компартментов.
- Физическая/логическая роль: Используется для нормализации силы инфекции, подразумевая, что коэффициенты контакта зависят от плотности.
- Почему суммирование: Оно агрегирует всех индивидов в системе.
Параметры и коэффициенты («Правила» системы)
- $\Lambda$: Скорость притока восприимчивых индивидов (чел./день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Представляет новые поступления в восприимчивую популяцию, обычно роды или иммиграцию.
- Почему сложение: Это источник, добавляющий индивидов в компартмент $S$.
- $\beta$: Коэффициент передачи (1/день).
- Математическое определение: Положительный коэффициент, потенциально зависящий от времени ($\beta(t)$).
- Физическая/логическая роль: Определяет, насколько эффективно вирус распространяется от инфицированного человека к восприимчивому.
- Почему умножение: Он масштабирует общую скорость заражения, действуя как фактор «силы» передачи.
- $\alpha$: Доля вакцинированных индивидов (1/день).
- Математическое определение: Положительный коэффициент, потенциально зависящий от времени ($\alpha(t)$).
- Физическая/логическая роль: Представляет скорость, с которой восприимчивые индивиды, $S_1$ и $S_2$ получают вакцины и переходят в компартмент $V$.
- Почему умножение: Он масштабирует поток индивидов в вакцинированный компартмент.
- $d$: Скорость естественной смертности населения (1/день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Представляет смерти от всех причин, кроме самой болезни. Он применяется ко всем компартментам.
- Почему вычитание: Это член удаления, уменьшающий популяцию в каждом компартменте.
- $\mu$: Скорость смертности среди симптоматических инфицированных индивидов (1/день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Это дополнительная скорость смертности, специфичная для заболевания, влияющая только на симптоматических индивидов ($I$).
- Почему вычитание: Это дополнительный член удаления из компартмента $I$.
- $\delta_V$: Скорость ослабления вакцинально-индуцированного иммунитета от $V$ к $S_1$ (1/день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Скорость, с которой вакцинированные индивиды теряют полный иммунитет и переходят в первую стадию ослабленного иммунитета ($S_1$).
- Почему сложение/вычитание: Он определяет поток индивидов между компартментами.
- $\delta_{S_1}$: Скорость ослабления иммунитета от $S_1$ к $S_2$ (1/день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Скорость, с которой индивиды в $S_1$ далее теряют иммунитет и переходят во вторую стадию ослабленного иммунитета ($S_2$).
- Почему сложение/вычитание: Он определяет поток индивидов между компартментами.
- $\delta_R$: Скорость ослабления естественного иммунитета от $R$ к $S_1$ (1/день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Скорость, с которой естественно выздоровевшие индивиды теряют полный иммунитет и переходят в $S_1$.
- Почему сложение/вычитание: Он определяет поток индивидов между компартментами.
- $\epsilon_1$: Относительная восприимчивость к инфекции индивидов в $S_1$ (безразмерная).
- Математическое определение: Постоянный положительный коэффициент, $0 \le \epsilon_1 \le 1$.
- Физическая/логическая роль: Модифицирует скорость заражения для индивидов $S_1$. Если $\epsilon_1 < 1$, они менее восприимчивы, чем полностью восприимчивые индивиды.
- Почему умножение: Он действует как масштабирующий коэффициент для силы инфекции для индивидов $S_1$.
- $\epsilon_2$: Относительная восприимчивость к инфекции индивидов в $S_2$ (безразмерная).
- Математическое определение: Постоянный положительный коэффициент, $0 \le \epsilon_2 \le 1$.
- Физическая/логическая роль: Аналогично $\epsilon_1$, но для индивидов $S_2$. Часто $\epsilon_2 > \epsilon_1$ или $\epsilon_2 = 1$, чтобы отразить большую восприимчивость.
- Почему умножение: Он действует как масштабирующий коэффициент для силы инфекции для индивидов $S_2$.
- $\theta$: Коэффициент снижения вероятности передачи инфекции от $E$ (безразмерный).
- Математическое определение: Постоянный положительный коэффициент, $0 \le \theta \le 1$.
- Физическая/логическая роль: Снижает вклад инкубационных индивидов ($E$) в силу инфекции, отражая, что они могут быть менее заразными, чем симптоматические индивиды.
- Почему умножение: Он масштабирует инфекционный вклад $E$.
- $\epsilon$: Коэффициент снижения вероятности передачи инфекции от $A$ (безразмерный).
- Математическое определение: Постоянный положительный коэффициент, $0 \le \epsilon \le 1$.
- Физическая/логическая роль: Снижает вклад бессимптомных индивидов ($A$) в силу инфекции.
- Почему умножение: Он масштабирует инфекционный вклад $A$.
- $\sigma$: Скорость прогрессирования от $E$ к инфицированным индивидам (1/день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Скорость, с которой инкубационные индивиды завершают свой инкубационный период и становятся заразными (либо бессимптомными, либо симптоматическими).
- Почему умножение: Он масштабирует поток индивидов из $E$.
- $\rho$: Доля симптоматических инфицированных индивидов (безразмерная).
- Математическое определение: Постоянный положительный коэффициент, $0 \le \rho \le 1$.
- Физическая/логическая роль: Определяет долю индивидов, покидающих инкубационный компартмент ($E$), которые становятся симптоматическими ($I$). Оставшаяся доля $(1-\rho)$ становится бессимптомной ($A$).
- Почему умножение: Он действует как фактор разделения для потока из $E$.
- $\gamma_A$: Скорость выздоровления бессимптомных инфицированных индивидов (1/день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Скорость, с которой бессимптомные индивиды выздоравливают и приобретают иммунитет.
- Почему умножение: Он масштабирует поток индивидов из $A$.
- $\gamma_I$: Скорость выздоровления симптоматических инфицированных индивидов (1/день).
- Математическое определение: Постоянный положительный коэффициент.
- Физическая/логическая роль: Скорость, с которой симптоматические индивиды выздоравливают и приобретают иммунитет.
- Почему умножение: Он масштабирует поток индивидов из $I$.
Математические операторы
- $d/dt$: Производная по времени.
- Математическое определение: Представляет мгновенную скорость изменения.
- Физическая/логическая роль: В этих ОДУ он описывает, как количество индивидов в каждом компартменте изменяется за очень малый интервал времени.
- Почему производная: Модель предполагает непрерывные изменения численности популяций, что типично для больших популяций в эпидемиологических моделях.
- Сложение ($+$) и вычитание ($-$):
- Математическое определение: Стандартные арифметические операции.
- Физическая/логическая роль: Эти операторы представляют поток индивидов в (сложение) или из (вычитание) определенного компартмента. Например, $\Lambda$ добавляется к $S$, а $\lambda(t)S$ вычитается из $S$.
- Почему сложение/вычитание: Это фундаментальный способ моделирования динамики популяций в компартментных моделях, отслеживая прирост и потери.
- Умножение ($\times$ или подразумеваемое):
- Математическое определение: Стандартная арифметическая операция.
- Физическая/логическая роль: Используется для расчета скоростей, зависящих от произведения популяций (например, скорость заражения $\lambda(t)S$ зависит от количества восприимчивых индивидов и силы инфекции) или для применения масштабирующих коэффициентов (например, $\epsilon_1\lambda(t)S_1$).
- Почему умножение: Это отражает принцип «массового действия», где скорость взаимодействия (например, заражения) пропорциональна произведению взаимодействующих популяций. Он также применяет безразмерные масштабирующие коэффициенты для модификации скоростей.
- Деление ($/$):
- Математическое определение: Стандартная арифметическая операция.
- Физическая/логическая роль: В силе инфекции $\lambda(t)$ деление на $N$ (общую численность населения) нормализует член инфекционного контакта.
- Почему деление: Это подразумевает частотно-зависимую передачу, означая, что вероятность заражения зависит от доли инфицированных индивидов в популяции, а не от их абсолютного числа. Это часто более реалистично для больших, хорошо перемешанных популяций.
Пошаговый поток
Представьте себе одного, абстрактного индивида, «точку данных», движущуюся через этот сложный механический конвейер иммунной системы и прогрессирования заболевания.
-
Вход в систему: Наш индивид начинает свой путь, будучи «привлеченным» в компартмент Восприимчивые ($S$). Это похоже на поступление новой детали на заводской пол. Скорость $\Lambda$ определяет, сколько новых деталей прибывает каждый день.
-
Первоначальный выбор (компартмент S): Находясь в $S$, наш индивид сталкивается с несколькими путями:
- Вакцинация: Он может быть вакцинирован со скоростью $\alpha S$, что немедленно перемещает его в компартмент Вакцинированные ($V$), предоставляя ему полный иммунитет.
- Естественная смерть: Он может умереть от причин, не связанных с болезнью, со скоростью $dS$, покидая систему.
- Инфекция: Если он сталкивается с инфицированным человеком (из $E$, $A$ или $I$), он заражается со скоростью $\lambda(t)S$ и переходит в компартмент Инкубационные ($E$). Это момент, когда он «подхватывает» вирус.
-
Инкубация (компартмент E): В $E$ наш индивид инкубирует вирус. Он инфицирован, но еще не способен эффективно его распространять.
- Прогрессирование: После инкубационного периода он переходит в инфекционное состояние со скоростью $\sigma E$.
- Естественная смерть: Он также может умереть естественным образом со скоростью $dE$.
-
Становление заразным (компартмент A или I): Покидая $E$, наш индивид «сортируется» по одному из двух инфекционных путей:
- Бессимптомный ($A$): С вероятностью $(1-\rho)$ он становится бессимптомным, переходя в компартмент Бессимптомные ($A$) со скоростью $(1-\rho)\sigma E$. Здесь он может распространять вирус, не проявляя симптомов.
- Симптоматический ($I$): С вероятностью $\rho$ он становится симптоматическим, переходя в компартмент Симптоматические ($I$) со скоростью $\rho\sigma E$. Здесь он проявляет симптомы и обычно более заразен.
-
Инфекционный период и выздоровление (компартменты A и I):
- Из A: Наш бессимптомный индивид может выздороветь со скоростью $\gamma_A A$, переходя в компартмент Выздоровевшие ($R$). Он также может умереть естественным образом со скоростью $dA$.
- Из I: Наш симптоматический индивид может выздороветь со скоростью $\gamma_I I$, также переходя в $R$. Однако он сталкивается с дополнительным риском: смертью от заболевания со скоростью $\mu I$ или естественной смертью со скоростью $dI$.
-
Временный иммунитет (компартменты R и V): Попав в $R$ (выздоровевшие) или $V$ (вакцинированные), наш индивид наслаждается периодом полного иммунитета. Но этот иммунитет не вечен.
- Ослабление от V: Вакцинированные индивиды теряют иммунитет со скоростью $\delta_V V$, переходя в компартмент $S_1$ (ослабленный иммунитет первой стадии).
- Ослабление от R: Естественно выздоровевшие индивиды теряют иммунитет со скоростью $\delta_R R$, также переходя в $S_1$.
- Естественная смерть: Индивиды в $V$ или $R$ также могут умереть естественным образом со скоростями $dV$ и $dR$ соответственно.
-
Спад иммунитета (компартменты S1 и S2):
- Из S1: Индивиды в $S_1$ имеют частично ослабленный иммунитет. Они могут:
- Быть вакцинированы снова со скоростью $\alpha S_1$, возвращаясь в $V$.
- Умереть естественным образом со скоростью $dS_1$.
- Быть повторно инфицированы со сниженной скоростью $\epsilon_1\lambda(t)S_1$, возвращаясь в $E$.
- Испытать дальнейшее ослабление иммунитета со скоростью $\delta_{S_1} S_1$, переходя в компартмент $S_2$ (ослабленный иммунитет второй стадии).
- Из S2: Индивиды в $S_2$ имеют значительно ослабленный иммунитет. Они могут:
- Быть вакцинированы снова со скоростью $\alpha S_2$, возвращаясь в $V$.
- Умереть естественным образом со скоростью $dS_2$.
- Быть повторно инфицированы со (потенциально более высокой) сниженной скоростью $\epsilon_2\lambda(t)S_2$, возвращаясь в $E$.
- Из S1: Индивиды в $S_1$ имеют частично ослабленный иммунитет. Они могут:
Этот непрерывный поток, когда индивиды перемещаются между компартментами на основе этих скоростей, описывает весь жизненный цикл иммунитета и инфекции в популяции.
Динамика оптимизации
Эта модель, будучи системой обыкновенных дифференциальных уравнений, не «обучается» или «обновляется» так же, как алгоритм машинного обучения, минимизируя функцию потерь. Вместо этого ее «динамика» относится к тому, как состояние системы эволюционирует во времени и какие стабильные или нестабильные паттерны она принимает. «Оптимизация» здесь заключается в понимании условий, при которых заболевание контролируется или сохраняется.
-
Достижение равновесия: Естественная тенденция системы — эволюционировать к точкам равновесия, где скорости изменения для всех компартментов становятся нулевыми ($dS/dt = 0, dV/dt = 0$ и т. д.). Это «стационарные состояния» системы.
- Равновесие без заболевания (DFE): Это состояние, когда нет инкубационных, бессимптомных или симптоматических индивидов ($E=A=I=0$). Заболевание исчезло.
- Эндемическое равновесие (EE): Это состояние, когда заболевание сохраняется в популяции с постоянным (ненулевым) числом инфицированных индивидов.
-
Базовое репродуктивное число ($R_0$): Этот единственный, критически важный параметр действует как основной «переключатель» поведения системы. Он выводится из параметров модели и представляет собой среднее количество вторичных инфекций, вызванных одним инфицированным индивидом в полностью восприимчивой популяции.
- Если $R_0 < 1$: Равновесие без заболевания является локально асимптотически устойчивым. Это означает, что если начальное количество инфицированных индивидов достаточно мало, заболевание естественным образом исчезнет. Система «сходится» к состоянию без заболевания.
- Если $R_0 > 1$: Равновесие без заболевания является неустойчивым. Это означает, что заболевание может распространяться и потенциально становиться эндемическим. Система будет удаляться от состояния без заболевания.
-
Анализ бифуркации: «Фазовые переходы» системы: Здесь динамика модели действительно раскрывается. Бифуркации описывают качественные изменения в поведении системы при изменении параметра (например, коэффициента передачи $\beta$, который напрямую влияет на $R_0$).
- Прямая бифуркация: В типичном сценарии, когда $R_0$ пересекает 1 снизу, DFE теряет устойчивость, и возникает стабильное эндемическое равновесие. Это «гладкий» переход, когда заболевание становится эндемическим, если передача достаточно высока.
- Обратная бифуркация: Это более сложная и тревожная динамика. Она означает, что стабильное эндемическое равновесие может существовать даже при $R_0 < 1$. В таких случаях заболевание может сохраняться, даже когда базовое репродуктивное число предполагает, что оно должно исчезнуть. Исход зависит от начального количества инфицированных индивидов (явление, называемое бистабильностью). Это критически важный вывод для общественного здравоохранения, поскольку простого снижения $R_0$ ниже 1 может быть недостаточно для искоренения заболевания, если начальные уровни инфекции высоки.
- Бифуркация седло-узла: Это происходит, когда две точки равновесия (часто стабильное и нестабильное эндемическое равновесие) появляются или исчезают при изменении параметра. Статья отмечает, что это может происходить вдоль расширенной ветви прямой бифуркации, способствуя сложной бистабильной динамике.
-
Оценка параметров с помощью MCMC: Чтобы динамика модели отражала реальные сценарии, авторы «обучают» или «подгоняют» модель, используя фактические данные по COVID-19. Они используют алгоритм Марковских цепей Монте-Карло (MCMC) для оценки изменяющихся во времени коэффициентов передачи $\beta(t)$ и вакцинации $\alpha(t)$.
- Как это работает: MCMC — это вычислительный метод, который генерирует выборки из вероятностного распределения. В данном контексте он итеративно предлагает новые значения для неизвестных параметров ($\beta(t)$ и $\alpha(t)$ в различных временных точках, представленных узлами сплайна) и принимает или отклоняет их на основе того, насколько хорошо выход модели соответствует наблюдаемым ежедневным новым подтвержденным случаям и дозам вакцин.
- «Обучение» на данных: За многие итерации алгоритм MCMC исследует пространство параметров, в конечном итоге сходясь к распределению значений параметров, которые наиболее согласуются с наблюдаемыми данными. Этот процесс позволяет модели «изучать» лежащую в основе динамику передачи и вакцинации на основе эмпирических доказательств, формируя ее параметры для наилучшего описания реальной кривой эпидемии. Использование кусочно-кубических сплайнов для $\beta(t)$ и $\alpha(t)$ позволяет модели адаптировать свое «обучение» к нестационарным, развивающимся скоростям с течением времени, улавливая влияние меняющихся мер общественного здравоохранения или вирусных вариантов.
По сути, «динамика оптимизации» этой модели заключается не в поиске единственного оптимального решения, а в понимании диапазона возможных долгосрочных поведений (равновесий) и того, как эти поведения меняются при изменении ключевых параметров, основываясь на подгонке к реальным данным. Присутствие обратных бифуркаций и бистабильности подчеркивает сложную и иногда контринтуитивную прирому контроля эпидемий.
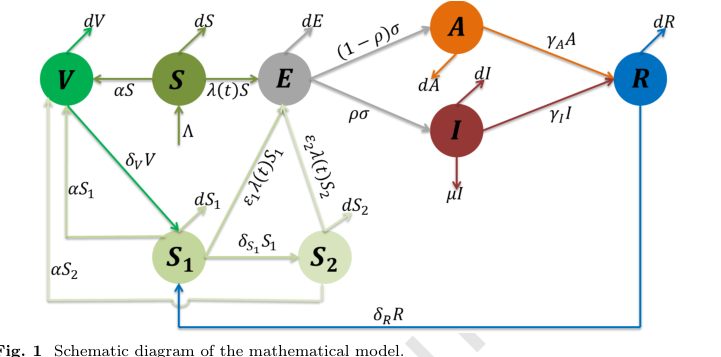 Figure 1. Schematic diagram of the mathematical model
Figure 1. Schematic diagram of the mathematical model
Результаты, ограничения и заключение
Экспериментальный дизайн и базовые уровни
Для строгой проверки своих математических утверждений авторы разработали эксперимент, сосредоточенный на подгонке их новой модели двухэтапного ослабления иммунитета (система (2)) к реальным эпидемиологическим данным. Основными «жертвами» или базовыми уровнями в этом контексте были не альтернативные модели в прямом сравнительном смысле, а скорее присущие ограничения более простых эпидемиологических рамок, которые не могут уловить сложную, нелинейную динамику ослабления иммунитета и изменяющихся во времени вмешательств. Окончательным доказательством эффективности их модели является ее способность точно воспроизводить наблюдаемые тенденции эпидемии.
Экспериментальная установка включала сбор данных эпиднадзора за COVID-19 из Соединенных Штатов за значительный период с 14 декабря 2020 г. по 6 июня 2022 г. Этот набор данных включал ежедневные новые подтвержденные случаи COVID-19 и ежедневные новые дозы вакцин. Для смягчения краткосрочных колебаний и периодических закономерностей к необработанным данным применялось 7-дневное скользящее среднее.
Ключевым аспектом дизайна было рассмотрение основных параметров: коэффициент передачи $\beta(t)$ и коэффициент вакцинации $\alpha(t)$ считались изменяющимися во времени. Для оценки этих динамических параметров использовались кусочно-кубические сплайновые функции. В частности, $\beta(t)$ аппроксимировался с использованием 18 узлов сплайна с интервалом узлов 30 дней, в то время как $\alpha(t)$ использовал 36 узлов сплайна с более коротким интервалом 15 дней для учета его более быстрых колебаний. Затем алгоритм Марковских цепей Монте-Карло (MCMC) использовался для оценки параметров, получая оптимальные значения для этих изменяющихся во времени параметров и других, перечисленных в Таблице 4. Этот подход позволил модели адаптироваться к развивающемуся эпидемическому ландшафту, косвенно учитывая такие факторы, как новые варианты и изменения в поведении.
Что доказывают свидетельства
Данные убедительно подтверждают способность модели улавливать богатую динамику ослабления иммунитета и ее влияние на распространение SARS-CoV-2. Наиболее убедительным доказательством является тесное соответствие между смоделированными данными модели (для ежедневных новых подтвержденных случаев и доз вакцин) и фактическими наблюдаемыми данными из Соединенных Штатов, как наглядно продемонстрировано на Рис. 3. Этот успешный подгон предоставляет неоспоримые доказательства того, что основной механизм двухэтапного процесса ослабления иммунитета в сочетании с изменяющимися во времени коэффициентами передачи и вакцинации эффективно работает на практике.
Помимо простой подгонки данных, численные симуляции строго подтвердили теоретические предсказания относительно динамики бифуркации:
- Прямые и обратные бифуркации: Модель последовательно демонстрирует как прямые, так и обратные бифуркации при $R_0 = 1$. В то время как прямая бифуркация подразумевает, что эпидемия стабилизируется при $R_0 > 1$, возникновение обратной бифуркации является критическим выводом. Она окончательно доказывает, что при определенных параметрических условиях стабильное эндемическое равновесие может существовать даже при базовом репродуктивном числе $R_0 < 1$. Это означает, что достижение $R_0$ ниже единицы не гарантирует автоматического искоренения заболевания, подчеркивая более сложную реальность, чем предполагают более простые модели.
- Бистабильность и мультистабильность: Анализ показал, что система может демонстрировать бистабильность или мультистабильность, что означает, что ноль, одно, два или даже три эндемических равновесия могут сосуществовать в зависимости от значений параметров. Это подразумевает, что долгосрочный исход эпидемии (искоренение против сохранения) может быть крайне чувствителен к начальным условиям, особенно в определенных диапазонах $R_0$.
- Бифуркация седло-узла: Численные симуляции далее показали, что бифуркация седло-узла может происходить вдоль расширенной ветви транскритического бифуркации. Это явление приводит к сосуществованию двух стабильных эндемических равновесий, подкрепляя концепцию бистабильности и предполагая, что траектория эпидемии может сходиться к различным стабильным состояниям в зависимости от начальных условий.
Кроме того, анализ чувствительности ключевых параметров дал четкое представление об эффективных мерах контроля:
- Продолжительность ослабления иммунитета: Данные однозначно показывают, что продление продолжительности вторичного ослабления иммунитета (как естественного, так и вакцинально-индуцированного) значительно снижает количество симптоматических случаев и общий риск заражения.
- Коэффициент вакцинации: Более высокий охват вакцинацией, как было доказано, существенно смягчает пики инфекций и снижает общий риск заражения.
- Относительная восприимчивость: Более низкая относительная восприимчивость (т. е. более сильный иммунитет) приводит к более благоприятной динамике инфекций. Исследование показало, что когда относительная восприимчивость ($\epsilon_1$ и $\epsilon_2$) высока, пик эпидемии может наступить раньше и быть более тяжелым. И наоборот, умеренные значения могут отсрочить пик, предоставляя ценное время для вмешательств. Совместный эффект увеличения охвата вакцинацией и модуляции относительной восприимчивости показал снижение пиков инфекций.
В совокупности данные доказывают, что предложенная модель двухэтапного ослабления иммунитета предлагает более нюансированное и точное понимание динамики SARS-CoV-2, подчеркивая ключевую роль устойчивого иммунитета, высокого охвата вакцинацией и сниженной восприимчивости в контроле эпидемий.
Ограничения и будущие направления
Хотя данное исследование предоставляет строгую основу для понимания ослабления иммунитета и его влияния на распространение SARS-CoV-2, важно признать его присущие ограничения и рассмотреть направления для дальнейшего развития.
Одним из значительных ограничений является то, что изменяющиеся во времени коэффициенты передачи и вакцинации модели, хотя и эффективны для подгонки реальных данных, косвенно отражают эффекты множества внешних факторов, таких как появление новых вирусных вариантов (например, Дельта, Омикрон), изменения в поведении человека и внедрение немедикаментозных мер вмешательства. Однако модель не может различать индивидуальный вклад этих факторов. Это означает, что мы можем видеть что произошло, но не точно почему с точки зрения конкретных внешних драйверов.
Кроме того, текущая модель не различает различные типы вакцин или их различную эффективность. Она также не учитывает поведенческую гетерогенность в популяции или пространственную структуру распространения заболевания. Эти упрощения, хотя и способствуют математической управляемости, ограничивают детализацию модели в отражении полной сложности реальных эпидемиологических сценариев.
Заглядывая вперед, возникает несколько тем для обсуждения для дальнейшей разработки и эволюции этих выводов:
- Разделение внешних факторов: Будущие исследования могли бы сосредоточиться на разработке подмоделей или включении дополнительных потоков данных для явного моделирования влияния конкретных вирусных вариантов, изменений в поведении или немедикаментозных мер вмешательства на коэффициенты передачи и вакцинации. Это позволило бы более детально понять их индивидуальный вклад в динамику эпидемий.
- Гетерогенность вакцин и эффективность: Развитие модели для различения различных вакцинных платформ (например, мРНК, вирусный вектор) и их специфических профилей ослабления и эффективности значительно повысило бы ее биологическую реалистичность и предсказательную силу для целенаправленных стратегий вакцинации.
- Пространственная и социальная динамика: Интеграция пространственных компонентов и поведенческой гетерогенности (например, различная приверженность мерам общественного здравоохранения, структуры социальных сетей) в модель могла бы дать представление о локальных вспышках, событиях суперраспространения и эффективности географически ориентированных вмешательств.
- Долгосрочное иммунное импринтирование: Выводы исследования о важности продолжительной вакцинально-индуцированной защиты и охвата на уровне популяции подчеркивают необходимость более глубокого изучения эффектов иммунного импринтирования. Как мы можем разрабатывать графики вакцинации или стратегии бустеров, которые максимизируют широту и долговечность иммунных ответов против развивающихся патогенов?
- Политические последствия обратной бифуркации и бистабильности: Демонстрация того, что эпидемия может сохраняться даже при $R_0 < 1$ (из-за обратной бифуркации) и что исходы могут зависеть от начальных условий (бистабильность), представляет собой серьезный вызов для политики общественного здравоохранения. Это требует смещения от единого фокуса на снижение $R_0$ ниже единицы к более динамичным, адаптивным стратегиям, которые учитывают начальные условия, ландшафты популяционного иммунитета и потенциал для возобновления даже в кажущихся контролируемыми средах. Какие новые метрики или пороговые значения необходимы для руководства политикой в таких сложных системах?
- Экономические и социальные издержки ослабления иммунитета: Дальнейшие исследования могли бы интегрировать экономические и социальные издержки, связанные с различными скоростями ослабления иммунитета и стратегиями вакцинации. Это обеспечило бы более целостное понимание компромиссов, связанных с решениями в области общественного здравоохранения, такими как инвестирование в более долговечные вакцины по сравнению с частыми кампаниями бустеров.
Выводы, полученные в результате этого анализа, являются ключевыми для оптимизации стратегий вакцинации и разработки более долговечных и эффективных вакцин. Сложная динамика, выявленная, особенно обратная бифуркация и бистабильность, подчеркивает, что контроль эпидемий — это не простая линейная проблема, а многогранная задача, требующая постоянной адаптации и глубокого понимания иммунологических и эпидемиологических взаимодействий.
