SARS-CoV-2感染引起的免疫衰退的丰富动力学与数据分析
The global pandemic of SARS-CoV-2 has constituted a serious threat to public health.
背景与学术传承
起源与学术谱系
本问题的确切起源直接源于全球SARS-CoV-2大流行以及随后的广泛疫苗接种工作。随着疫情的展开,人们清楚地认识到,自然感染和疫苗接种均能提供免疫保护,但这种保护并非永久性的,并且至关重要的是,其衰减并非以恒定或线性的速率进行(第13-15行)。这一观察结果对准确模拟疫情的长期轨迹和设计有效的公共卫生干预措施构成了重大挑战。历史背景根植于理解SARS-CoV-2免疫力如何随时间减弱的需求,这会导致突破性感染并损害疫苗的长期保护效力(第45-47行)。
先前方法的根本局限性或“痛点”是双重的。首先,早期模型要么过度简化了免疫衰减(例如,恒定或线性衰减),要么在试图捕捉已观察到的复杂性时,变得“高度复杂,使得系统性理论分析具有挑战性”(第112-114行)。这些复杂模型通常严重依赖数值模拟来探索控制策略或在孤立条件下检查分岔现象(第114-116行)。这种对数值方法的依赖,而非系统性理论分析,阻碍了对潜在动力学的全面且易于处理的理解。因此,作者们有必要开发一个“相对简单但具有生物学意义的模型,以捕捉由免疫衰减引起的非线性动力学”(第116-118行),以克服这些分析挑战,并为研究免疫衰减及其对疾病传播的影响提供一个更易于处理的框架。
直观领域术语
- 免疫衰减 (Immune Waning): 指一个人针对某种疾病的保护性免疫力随时间逐渐下降,无论这种免疫力是来自过去的感染还是疫苗。
- 类比: 想象一下你的手机电池在充满电后会缓慢地失去电量。你身体的保护机制并非瞬间关闭,而是逐渐减弱,使你再次感染的风险增加。
- 逆向分岔 (Backward Bifurcation): 在疾病模型中,这是一种特殊情况,即即使基本再生数 ($R_0$) 小于1,疾病仍能持续存在并成为地方性流行病。通常情况下,$R_0 < 1$ 意味着疾病应该会自然消亡。
- 类比: 想象一个重球放在一个略微倾斜的表面上。如果你给它一个小的推力,它可能会滚回到原来的位置。但如果你给它一个足够大的初始推力,它可能会越过一个小坡并卡在斜坡下方的另一个凹陷处,尽管整体坡度表明它应该滚回原处。这种现象也出现在其他领域。初始的“动量”(感染人数)可以决定疾病是否会“卡住”在地方性流行状态。
- 基本再生数 ($R_0$) (Basic Reproduction Number): 这是一个关键数字,代表一个感染个体在完全易感人群中平均引起的新感染数量。
- 类比: 考虑一种新的病毒式舞蹈潮流。如果一个人平均教给超过一个人 ($R_0 > 1$),这种舞蹈就会传播开来。如果他们教给少于一个人 ($R_0 < 1$),这种潮流最终会消退。
- 地方性流行稳态 (Endemic Equilibrium): 指流行病中的一种稳定状态,疾病在人群中持续存在,但感染个体的数量随时间保持相对恒定,既不会快速增加也不会消失。
- 类比: 想象一条河流的稳定流动。水一直在流动,但整体水位和水流速度保持不变。疾病一直存在,但其存在是可预测和稳定的,而非突然的爆发或完全的消失。
符号表
| 符号 | 描述 (单位) |
|---|---|
问题定义与约束
核心问题表述与困境
本文所解决的核心问题源于免疫力对抗SARS-CoV-2衰减的复杂性和非线性特征。
输入/当前状态:
初始阶段,我们拥有通过自然感染或疫苗接种获得一定水平SARS-CoV-2免疫保护的个体。然而,当前对这种免疫力的理解和建模在几个关键方面存在不足:
1. 非线性衰减: 免疫效力并非以恒定或线性的速率下降。相反,它随时间以一种更复杂、非线性的方式衰减(摘要,第14-15行)。
2. 模型复杂性 vs. 真实性: 试图捕捉免疫衰减的现有流行病学模型常常陷入两个极端:要么过于简化(例如,假设线性衰减),要么极其复杂(例如,年龄结构模型、个体特异性衰减率模型,或区分疫苗接种/康复个体的独立舱室)。这种复杂性使得系统性的理论分析,如理解分岔动力学,变得极其困难,并常常需要依赖孤立条件下的数值模拟(引言,第65-78行,112-116行,445-447行)。
3. 不完整的动态表征: 之前的模型难以全面表征免疫的动态过程,特别是诸如后向分岔(backward bifurcation)等现象,即即使基本再生数($R_0$)小于1,疾病仍可能持续存在(引言,第90-91行,96-102行)。这意味着将$R_0$降低到1以下可能不足以根除疾病,对公共卫生策略构成了重大挑战。
期望终点(输出/目标状态):
本文旨在开发一个新的数学模型,该模型能够:
1. 捕捉两阶段衰减: 通过整合更具生物学现实意义的“两阶段免疫衰减机制”(摘要,第15-16行;引言,第120-122行),准确表征免疫的动态过程。这意味着模拟一个初始的强免疫期,随后出现更快速的下降。
2. 实现简洁性和可处理性: 模型应“相对简单但具有生物学意义”(引言,第116-118行),并保持“数学上的可处理性”(讨论,第449-450行)。这种平衡对于进行严格的理论分析至关重要,包括全面的分岔分析。
3. 为公共卫生策略提供依据: 通过研究SARS-CoV-2感染的免疫学机制以及控制措施的影响,为制定更有效的公共卫生策略和政策提供科学依据(引言,第48-51行,118-119行)。
缺失环节/数学鸿沟:
确切的缺失环节是一个数学上可处理的、显式包含SARS-CoV-2非线性、两阶段免疫衰减机制的舱室模型,该模型能够对复杂的动态行为(如分岔和双稳态)进行严格的理论分析,并利用真实的流行病学数据进行稳健的参数估计。 之前的模型要么过度简化了衰减过程,要么过于复杂以至于无法进行全面的理论分析,从而在理解免疫衰减的全部动态影响方面留下了空白。
困境:
困扰先前研究人员的核心困境在于生物学真实性与数学可处理性之间的权衡。为了准确地表示免疫衰减的细微差别(例如,个体异质性、年龄结构、非线性衰减),模型往往变得极其复杂。然而,这种复杂性常常使其在分析上难以处理,迫使研究人员只能依赖特定场景下的数值模拟。本文试图通过引入一种特定的两阶段衰减机制来弥合这一差距,该机制既具有生物学意义,又足够简单,能够进行严格的数学分析,包括基本再生数的推导和全面的分岔分析(讨论,第448-450行)。
约束与失效模式
对SARS-CoV-2免疫衰减进行建模的问题极其困难,因为作者们遇到了几个严峻的、现实的障碍:
- 非线性与异质性免疫衰减: 免疫效力并非以恒定或线性的速率下降(摘要,第14-15行)。相反,免疫力随时间衰减,导致再感染易感性的异质性。个体通常在初始阶段保持高水平的保护,但此后抗体水平和保护效力会显著下降,最终趋于消失(引言,第105-111行)。这种复杂的生物学过程必须被准确地表示。
- 免疫逃逸机制的出现: 病毒不断进化,免疫逃逸机制随之出现,损害了疫苗和自然免疫的长期保护效力(引言,第46-47行)。尽管未被明确建模为一种机制,但这种生物学现实凸显了对能够适应不断变化的免疫格局的动态模型的需求。
- 时变流行病学参数: 关键参数如传播率($\beta(t)$)和疫苗接种率($\alpha(t)$)并非恒定,而是随时间显著变化。这些变化受到多种外部因素的影响,包括新变种(如Delta、Omicron)的出现、行为改变以及非药物干预措施(讨论,第491-493行)。这使得静态参数模型不足以应对,并需要能够估计时变参数的方法。
- 数据驱动的参数估计挑战: 模型需要拟合真实世界中嘈杂的流行病学数据(例如,每日新增确诊COVID-19病例、每日新增疫苗接种剂量),持续时间较长(例如,2020年12月至2022年6月在美国)(摘要,第23-25行;讨论,第471-473行)。这需要稳健的统计方法,如马尔可夫链蒙特卡洛(MCMC)结合分段三次样条函数,以处理数据的时变性和固有的不确定性(摘要,第25-26行;讨论,第473-474行)。
- 用于分岔分析的数学可处理性: 目标是进行严格的理论分析,包括基本再生数的推导和全面的分岔分析,以理解复杂动态行为,如前向分岔和后向分岔,以及多个地方性均衡点的共存(摘要,第16-22行;讨论,第449-450行)。这对模型的复杂性提出了严格的限制,因为过于精细的模型很快就会变得在分析上难以处理。
- 确保模型稳定性和真实性: 模型必须确保种群舱室保持有界且非负,这是任何现实流行病学模型的基本要求(模型推导,第144-145行;不变区域,引理1,第184-187行)。这一数学约束确保了模型的输出在生物学上是合理的。
- 解释复杂的分岔现象: 模型揭示了复杂的动力学行为,如鞍节点分岔(saddle-node bifurcations)和双稳态(bistability),其中可能共存多个稳定的地方性均衡点。这意味着即使在$R_0 < 1$的情况下,疾病也可能持续存在,这是一个挑战传统公共卫生策略的关键发现,需要仔细解释(摘要,第19-22行;讨论,第461-467行)。理解这些现象需要严格的数学证明和数值验证。
为何采用此方法
选择的必然性
作者开发一种新颖的两阶段免疫衰减模型的决定并非随意,而是对传统流行病学模型在面对 SARS-CoV-2 免疫复杂动态时固有的局限性的直接回应。认识到标准的“SOTA”(State-of-the-Art)流行病学方法不足,源于对该病毒和人类免疫反应的几项关键观察:
首先,很明显,无论是自然感染还是疫苗接种引起的免疫保护,“其衰减速率并非恒定或线性的”(摘要,第 14-15 行)。这立即使得基本的 SIRS(易感-感染-康复-易感)模型,这些模型通常假设免疫力存在简单、连续的衰减,不足以捕捉细微的生物学过程。现实中“短时间内出现的突破性感染 [7]”以及“免疫逃逸机制的出现 [8]”(引言,第 45-48 行)进一步强调了对免疫衰减进行更动态和多方面表述的必要性。
其次,一个关键的见解是反向分岔现象,即“$R_0 < 1$ 并不一定能保证疾病的根除”(引言,第 91-92 行)。传统模型基本假设,如果基本再生数 ($R_0$) 低于 1,疫情将自然消亡。然而,即使在 $R_0$ 可能低于该阈值的情况下,SARS-CoV-2 的持续存在也凸显了这些更简单框架中的一个关键缺陷。作者的模型明确捕捉了这种复杂的动态,表明“即使基本再生数 $R_0 < 1$,疫情也会持续存在”(摘要,第 21-22 行),这是简单模型无法解释的一个特征。
最后,尽管现有的先进模型已开始纳入免疫衰减的某些方面(例如 [17, 18, 19]),但许多模型“非常复杂,使得系统性的理论分析具有挑战性”,并且常常“依赖于数值模拟来探索控制策略或在孤立条件下检查分岔现象”(引言,第 112-115 行)。作者明确旨在“解决这些局限性”,寻求一个“相对简单但具有生物学意义”的模型(引言,第 115-117 行),以便进行严格的理论分析,而这在其他方法中常常因过度复杂而受到影响。这种对生物学真实性和数学可处理性之间平衡的需求,巩固了其选择特定两阶段区室结构的决定。
比较优势
这种两阶段免疫衰减模型的定性优越性,超越了单纯的性能指标,在于其结构优势,使其能够在保持分析严谨性的同时捕捉复杂的流行病学现实。
- 生物学上真实的免疫衰减: 最显著的结构优势在于明确引入了两个不同的区室,$S_1(t)$ 和 $S_2(t)$,分别代表“部分和进一步衰减免疫力”的个体(引言,第 120-127 行)。这使得模型能够超越简单的线性衰减,将免疫力描述为“从完全免疫到部分免疫状态的非线性转变”(讨论,第 448-449 行)。这种多阶段方法更忠实地反映了保护力随时间逐渐且异质性地减弱的生物学过程,而不是均匀、连续的衰减。
- 稳健的分岔分析和双稳态性: 该模型的设计有利于对前向和后向分岔进行严格推导和分析(摘要,第 17-18 行;讨论,第 454-455 行)。能够证明后向分岔是关键的定性飞跃,因为它解释了“$R_0 < 1$ 并不一定能保证疾病的根除”(引言,第 91-92 行)。这意味着即使传统指标表明疾病应该消亡,它也可能变得地方性流行。此外,该模型揭示了“多个地方性平衡共存”和“双稳态性”(摘要,第 18-22 行;讨论,第 458-469 行),这意味着疫情的长期轨迹可能高度依赖于初始条件,这种动态复杂性是简单模型无法实现的。
- 用于深入洞察的数学可处理性: 与许多“非常复杂”且“常常依赖于数值模拟”的现有模型不同(引言,第 112-113 行),这种两阶段模型被设计为“相对简单但具有生物学意义”(引言,第 115-117 行)。这种结构选择允许“基本再生数的严格推导和全面的分岔分析”(讨论,第 449-451 行)。这种平衡是一个关键优势,它提供了对驱动疫情动态机制的深入理论洞察,而不仅仅是描述性模拟。
- 整合时变真实世界数据: 该模型结合了时变传播率 $\beta(t)$ 和疫苗接种率 $\alpha(t)$,使用分段三次样条函数和 MCMC 算法进行估计(讨论,第 470-473 行)。这使得模型能够适应真实世界的流行病学数据和不断变化的干预策略,提供比依赖静态参数的模型更动态和适用的框架。
该论文并未讨论计算复杂性,例如从 $O(N^2)$ 到 $O(N)$ 的内存减少或在机器学习算法背景下处理高维噪声。其优越性根植于其增强的流行病学真实性和理解疾病传播的分析能力。
与约束的对齐
所选的两阶段免疫衰减模型完美地符合从问题定义中推导出的隐式约束,在 SARS-CoV-2 动态的挑战与解决方案的独特属性之间建立了牢固的“结合”。
- 约束:免疫衰减的准确表示: 问题要求一个模型能够认识到“免疫功效的衰减速率并非恒定或线性的”,并且免疫力“会随着时间的推移而减弱,导致再感染的易感性存在异质性”(摘要,第 14-15 行;引言,第 105-106 行)。解决方案的独特属性是其“两阶段免疫衰减机制”(摘要,第 16 行),它明确引入了“部分和进一步衰减免疫力”的区室($S_1(t)$ 和 $S_2(t)$)(引言,第 120-127 行)。这直接解决了免疫衰减的非线性和异质性本质,提供了更具生物学准确性和细微差别的表示。
- 约束:解释复杂的疫情持续性: 一个关键的要求是解释 SARS-CoV-2 的实际持续存在,即使传统指标表明可以根除。该模型能够展示“前向和后向分岔”以及“双稳态性”(摘要,第 17-22 行;讨论,第 454-469 行)完美契合。特别是后向分岔表明,“$R_0 < 1$ 并不一定能保证疾病的根除”(引言,第 91-92 行),使得疫情得以持续。这直接解决了简单模型预测与现实观察之间的差异。
- 约束:用于政策洞察的数学可处理性: 需要一个既真实又易于进行严格理论分析的模型,这对于为公共卫生策略提供信息至关重要。尽管许多现有模型“非常复杂,使得系统性的理论分析具有挑战性”(引言,第 112-113 行),但这种两阶段模型被设计为“相对简单但具有生物学意义”(引言,第 115-117 行)。这允许“基本再生数的严格推导和全面的分岔分析”(讨论,第 449-451 行),提供清晰、可操作的见解,而这些见解可能会被过于复杂、难以处理的模型所掩盖。
- 约束:数据驱动和动态参数化: 有效地模拟快速演变的疫情需要能够整合真实世界数据并考虑时变因素的能力。解决方案使用“MCMC 算法结合分段三次样条函数”从“美国 COVID-19 流行病学数据”中估计时变传播率 $\beta(t)$ 和疫苗接种率 $\alpha(t)$(摘要,第 23-25 行;讨论,第 470-473 行),完美满足了这一约束。这种动态参数化增强了模型的现实性和对实时疫情控制的预测能力。
这种方法有效地弥合了生物学复杂性与分析可行性之间的差距,使其成为理解和管理 SARS-CoV-2 的理想工具。
替代方案的拒绝
该论文专注于区室流行病学建模,因此不讨论或拒绝 GANs 或 Diffusion 模型等深度学习方法,因为它们超出了其范围。然而,它隐含地拒绝或强调了其他流行病学建模替代方案的局限性:
-
标准 SIR/SIRS 模型: 这些基础模型因无法捕捉 SARS-CoV-2 免疫的特定复杂性而被隐含地认为不足。
- SIR 模型: 这些模型假设终生免疫(引言,第 53-54 行),这对于 SARS-CoV-2 来说显然是错误的,因为免疫力会减弱。
- 基本 SIRS 模型: 虽然考虑了免疫衰减,但它们通常将其简化为“恒定或线性速率”(摘要,第 14-15 行)或简单、连续的衰减(讨论,第 445-446 行)。作者的工作通过表明需要“两阶段免疫衰减机制”来反映“从完全免疫到部分免疫状态的非线性转变”(讨论,第 448-449 行),直接反驳了这一点。
- 未能解释后向分岔: 拒绝这些更简单模型的一个关键原因是它们无法解释后向分岔等现象,即即使基本再生数 $R_0 < 1$,疫情也会持续存在(摘要,第 21-22 行;讨论,第 462-469 行)。标准 SIRS 模型在这种情况下会预测根除,使其不适用于 SARS-CoV-2。
-
现有过于复杂的流行病学模型: 该论文还暗示拒绝了那些尽管试图捕捉更多细节但变得分析上难以处理的模型。作者指出,“现有模型大多非常复杂,使得系统性的理论分析具有挑战性。这些研究常常依赖于数值模拟来探索控制策略或在孤立条件下检查分岔现象。”(引言,第 112-115 行)。这表明,尽管这些模型(例如,具有连续衰减函数、个体特定速率或众多独立区室的模型,如讨论中第 445-447 行所述)可能提供精细的细节,但它们的复杂性阻碍了作者优先考虑的严格理论分析和全面的分岔研究。相比之下,所选的两阶段模型“提供了一个更简单、更具生物学解释性的框架”,同时仍然允许“基本再生数的严格推导和全面的分岔分析”(讨论,第 448-451 行)。这突显了一个有意识的选择,即避免那些牺牲分析深度以换取过度、可能无法验证的细节的模型。
本质上,作者拒绝了那些要么过于简单而无法反映 SARS-CoV-2 观察到的非线性免疫动态和复杂分岔现象,要么过于复杂而无法进行所需的严格理论分析和机制理解的替代方案。他们的两阶段模型在生物学真实性和分析可行性之间取得了务实的平衡,提供了足够的生物学真实性,而不会变得分析上难以处理。
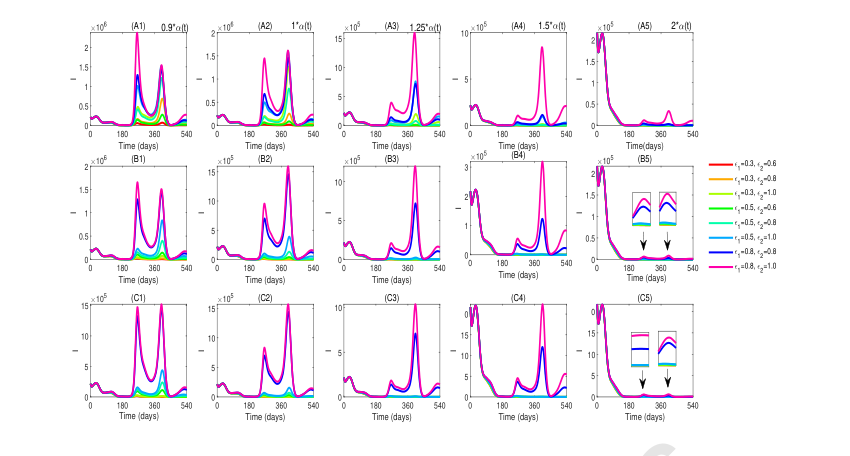 Figure 5. The impact of different vaccination rates, duration of secondary waning immunity, and two relative susceptibilities on disease transmission dynamics. By combining ε1 = 0.3, 0.5, 0.8 and ε2 = 0.6, 0.8, 1 in all possible pairwise combinations, we derive situations in which two relative suscep- tibilities change concurrently. (A1)-(C1), (A2)-(C2), (A3)-(C3), (A4)-(C4), and (A5)-(C5) correspond to multiples of the original vaccination rate of 0.9, 1, 1.25, 1.5, and 2, respectively. The figures are arranged into five columns based on different multiples of the original vaccination rate in the model and into three rows according to different immune waning durations. The durations of the secondary waning immunity 1 δV + 1 δS1 = 1 δR + 1 δS1 = 180, 365, 540 days, respectively, corresponds to (A1)-(A5),
Figure 5. The impact of different vaccination rates, duration of secondary waning immunity, and two relative susceptibilities on disease transmission dynamics. By combining ε1 = 0.3, 0.5, 0.8 and ε2 = 0.6, 0.8, 1 in all possible pairwise combinations, we derive situations in which two relative suscep- tibilities change concurrently. (A1)-(C1), (A2)-(C2), (A3)-(C3), (A4)-(C4), and (A5)-(C5) correspond to multiples of the original vaccination rate of 0.9, 1, 1.25, 1.5, and 2, respectively. The figures are arranged into five columns based on different multiples of the original vaccination rate in the model and into three rows according to different immune waning durations. The durations of the secondary waning immunity 1 δV + 1 δS1 = 1 δR + 1 δS1 = 180, 365, 540 days, respectively, corresponds to (A1)-(A5),
数学与逻辑机制
主方程
本文分析的核心在于一个由八个耦合常微分方程(ODEs)组成的系统,该系统描述了人群中个体在不同健康和免疫状态之间的动态流动。该系统在论文中标记为 (2),是模拟 SARS-CoV-2 传播和控制的数学引擎,并纳入了两阶段的免疫衰减机制。
$$ \begin{aligned} \frac{dS}{dt} &= \Lambda - \lambda(t)S - (\alpha + d)S \\ \frac{dV}{dt} &= \alpha(S + S_1 + S_2) - (\delta_V + d)V \\ \frac{dS_1}{dt} &= \delta_V V + \delta_R R - \epsilon_1\lambda(t)S_1 - (\alpha + \delta_{S_1} + d)S_1 \\ \frac{dS_2}{dt} &= \delta_{S_1} S_1 - \epsilon_2\lambda(t)S_2 - (\alpha + d)S_2 \\ \frac{dE}{dt} &= \lambda(t)S + \epsilon_1\lambda(t)S_1 + \epsilon_2\lambda(t)S_2 - (\sigma + d)E \\ \frac{dA}{dt} &= (1 - \rho)\sigma E - (\gamma_A + d)A \\ \frac{dI}{dt} &= \rho\sigma E - (\gamma_I + \mu + d)I \\ \frac{dR}{dt} &= \gamma_A A + \gamma_I I - (\delta_R + d)R \end{aligned} $$
至关重要的是,个体被感染的速率,即“感染力”,$\lambda(t)$,本身是一个动态组成部分,定义为:
$$ \lambda(t) = \frac{\beta(\theta E + \epsilon A + I)}{N} $$
其中,$N$ 代表总人口,即八个隔室中所有个体的总和:$N(t) = S(t) + V(t) + S_1(t) + S_2(t) + E(t) + A(t) + I(t) + R(t)$。
条目解剖
让我们逐一剖析这些方程,以理解每个组成部分的含义及其存在的原因。这就像拆解一个复杂的时钟,看看每个齿轮和弹簧如何对其整体功能做出贡献。
隔室变量(个体的“状态”)
- $S(t)$: 代表在时间 $t$ 时完全易感个体的数量。
- 数学定义: ODE 系统中的状态变量。
- 物理/逻辑作用: 这些是未对 SARS-CoV-2 产生免疫力的个体,可能被感染。
- 为何是变量: 随着人们的出生、接种疫苗或感染,其数值会随时间变化。
- $V(t)$: 代表已接种疫苗且完全免疫的个体的数量。
- 数学定义: 状态变量。
- 物理/逻辑作用: 已接种疫苗且目前受到保护的个体。
- $S_1(t)$: 表示首次免疫力减弱的个体。
- 数学定义: 状态变量。
- 物理/逻辑作用: 他们失去了一些保护,再次变得部分易感。这是免疫衰减的第一阶段。
- $S_2(t)$: 代表免疫力进一步减弱的个体,导致其抵抗病原体的能力显著下降。
- 数学定义: 状态变量。
- 物理/逻辑作用: 这些个体免疫力非常低,极易感。这是免疫衰减的第二阶段,更为严重。
- $E(t)$: 代表有感染潜力的暴露个体的数量。
- 数学定义: 状态变量。
- 物理/逻辑作用: 已感染但尚未产生感染性的个体(潜伏期)。
- $A(t)$: 表示无症状感染个体的数量。
- 数学定义: 状态变量。
- 物理/逻辑作用: 感染后不表现症状但仍能传播病毒的个体。
- $I(t)$: 代表有症状感染个体的数量。
- 数学定义: 状态变量。
- 物理/逻辑作用: 感染后表现症状且通常具有高度传染性的个体。
- $R(t)$: 代表已康复且完全免疫的个体的数量。
- 数学定义: 状态变量。
- 物理/逻辑作用: 已从感染中康复并暂时获得完全免疫的个体。
- $N(t)$: 代表时间 $t$ 时的总人口。
- 数学定义: 所有其他隔室变量的总和。
- 物理/逻辑作用: 用于标准化感染力,暗示接触率是密度依赖的。
- 为何是求和: 它汇总了系统中的所有个体。
参数和系数(系统的“规则”)
- $\Lambda$: 易感个体招募率(数量/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: 代表进入易感人群的新增人口,通常是出生或移民。
- 为何是加法: 这是一个源项,向 $S$ 隔室添加个体。
- $\beta$: 传播率(1/天)。
- 数学定义: 一个正系数,可能随时间变化 ($\beta(t)$)。
- 物理/逻辑作用: 决定了病毒从感染者传播给易感者的有效性。
- 为何是乘法: 它缩放了感染的总速率,作为传播的“强度”因子。
- $\alpha$: 接种疫苗的个体比例(1/天)。
- 数学定义: 一个正系数,可能随时间变化 ($\alpha(t)$)。
- 物理/逻辑作用: 代表易感、$S_1$ 和 $S_2$ 个体接种疫苗并进入 $V$ 隔室的速率。
- 为何是乘法: 它缩放了进入疫苗接种隔室的个体流量。
- $d$: 人口自然死亡率(1/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: 代表除疾病本身以外的所有原因造成的死亡。它适用于所有隔室。
- 为何是减法: 这是一个移除项,减少了每个隔室的人口。
- $\mu$: 有症状感染个体中的死亡率(1/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: 这是由疾病本身引起的额外死亡率,仅影响有症状的个体 ($I$)。
- 为何是减法: 这是从 $I$ 隔室移除的额外项。
- $\delta_V$: 疫苗诱导的免疫力从 $V$ 到 $S_1$ 的衰减率(1/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: 已接种疫苗的个体失去完全免疫力并转变为第一阶段衰减免疫力 ($S_1$) 的速率。
- 为何是加减法: 它决定了隔室之间个体的流动。
- $\delta_{S_1}$: 免疫力从 $S_1$ 到 $S_2$ 的衰减率(1/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: $S_1$ 中的个体进一步失去免疫力并转变为第二阶段衰减免疫力 ($S_2$) 的速率。
- 为何是加减法: 它决定了隔室之间个体的流动。
- $\delta_R$: 自然免疫力从 $R$ 到 $S_1$ 的衰减率(1/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: 自然康复的个体失去完全免疫力并转变为 $S_1$ 的速率。
- 为何是加减法: 它决定了隔室之间个体的流动。
- $\epsilon_1$: $S_1$ 个体对感染的相对易感性(无量纲)。
- 数学定义: 一个常数正系数,$0 \le \epsilon_1 \le 1$。
- 物理/逻辑作用: 修改 $S_1$ 个体的感染率。如果 $\epsilon_1 < 1$,则它们的易感性低于完全易感个体。
- 为何是乘法: 它作为 $S_1$ 个体感染力的一种缩放因子。
- $\epsilon_2$: $S_2$ 个体对感染的相对易感性(无量纲)。
- 数学定义: 一个常数正系数,$0 \le \epsilon_2 \le 1$。
- 物理/逻辑作用: 与 $\epsilon_1$ 类似,但针对 $S_2$ 个体。通常 $\epsilon_2 > \epsilon_1$ 或 $\epsilon_2 = 1$ 以反映更高的易感性。
- 为何是乘法: 它作为 $S_2$ 个体感染力的一种缩放因子。
- $\theta$: $E$ 传播概率降低的因子(无量纲)。
- 数学定义: 一个常数正系数,$0 \le \theta \le 1$。
- 物理/逻辑作用: 降低了暴露个体 ($E$) 对感染力的贡献,表明它们可能不如有症状个体具有传染性。
- 为何是乘法: 它缩放了 $E$ 的传染性贡献。
- $\epsilon$: $A$ 传播概率降低的因子(无量纲)。
- 数学定义: 一个常数正系数,$0 \le \epsilon \le 1$。
- 物理/逻辑作用: 降低了无症状个体 ($A$) 对感染力的贡献。
- 为何是乘法: 它缩放了 $A$ 的传染性贡献。
- $\sigma$: $E$ 向感染个体进展的速率(1/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: 暴露个体完成潜伏期并变得具有传染性的速率(无症状或有症状)。
- 为何是乘法: 它缩放了 $E$ 的个体流出。
- $\rho$: 有症状感染个体的比例(无量纲)。
- 数学定义: 一个常数正系数,$0 \le \rho \le 1$。
- 物理/逻辑作用: 决定了离开暴露隔室 ($E$) 的个体中成为有症状者 ($I$) 的比例。剩余比例 $(1-\rho)$ 成为无症状者 ($A$)。
- 为何是乘法: 它作为 $E$ 流动的分割因子。
- $\gamma_A$: 无症状感染个体康复率(1/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: 无症状个体康复并获得免疫力的速率。
- 为何是乘法: 它缩放了 $A$ 的个体流出。
- $\gamma_I$: 有症状感染个体康复率(1/天)。
- 数学定义: 一个常数正系数。
- 物理/逻辑作用: 有症状个体康复并获得免疫力的速率。
- 为何是乘法: 它缩放了 $I$ 的个体流出。
数学运算符
- $d/dt$: 相对于时间的导数。
- 数学定义: 表示瞬时变化率。
- 物理/逻辑作用: 在这些 ODE 中,它描述了每个隔室中的个体数量在极小时间间隔内的变化方式。
- 为何是导数: 该模型假设人口数量是连续变化的,这对于流行病学模型中的大人口来说是典型的。
- 加法 ($+$) 和减法 ($-$):
- 数学定义: 标准算术运算。
- 物理/逻辑作用: 这些运算符代表个体流入(加法)或流出(减法)特定隔室。例如,$\Lambda$ 加到 $S$,而 $\lambda(t)S$ 从 $S$ 中减去。
- 为何是加减法: 这是在隔室模型中模拟人口动态、跟踪增减的基本方法。
- 乘法 ($\times$ 或隐含):
- 数学定义: 标准算术运算。
- 物理/逻辑作用: 用于计算依赖于人口乘积的速率(例如,感染率 $\lambda(t)S$ 取决于易感个体数量和感染力)或应用缩放因子(例如,$\epsilon_1\lambda(t)S_1$)。
- 为何是乘法: 这反映了“质量作用”原理,即相互作用的速率(如感染)与相互作用人口的乘积成正比。它还应用无量纲缩放因子来修改速率。
- 除法 ($/$):
- 数学定义: 标准算术运算。
- 物理/逻辑作用: 在感染力 $\lambda(t)$ 中,除以 $N$(总人口)可以标准化传染性接触项。
- 为何是除法: 这意味着频率依赖性传播,即感染的概率取决于人群中感染个体的比例,而不是其绝对数量。这对于大型、混合充分的人群通常更现实。
分步流程
想象一个单一的、抽象的个体,一个“数据点”,在这个复杂的免疫系统和疾病进展的机械装配线上移动。
-
进入系统: 我们的个体开始其旅程,被“招募”到易感 ($S$) 隔室。这就像一个新零件进入工厂车间。速率 $\Lambda$ 决定了每天有多少新零件到达。
-
初始选择($S$ 隔室): 在 $S$ 状态下,我们的个体面临几个路径:
- 接种疫苗: 他们可能以 $\alpha S$ 的速率接种疫苗,立即进入已接种疫苗 ($V$) 隔室,获得完全免疫。
- 自然死亡: 他们可能以 $dS$ 的速率死于非疾病原因,退出系统。
- 感染: 如果他们遇到一个感染者(来自 $E$、$A$ 或 $I$),他们将以 $\lambda(t)S$ 的速率被感染,并进入暴露 ($E$) 隔室。这是他们“感染”病毒的时刻。
-
潜伏期($E$ 隔室): 在 $E$ 状态下,我们的个体正在潜伏病毒。他们已被感染,但尚未能有效传播。
- 进展: 潜伏期后,他们将以 $\sigma E$ 的速率进展到感染状态。
- 自然死亡: 他们也可能以 $dE$ 的速率自然死亡。
-
变得有传染性($A$ 或 $I$ 隔室): 离开 $E$ 隔室后,我们的个体被“分拣”到两个传染性路径之一:
- 无症状 ($A$): 以 $(1-\rho)$ 的概率,他们成为无症状者,以 $(1-\rho)\sigma E$ 的速率进入无症状 ($A$) 隔室。在这里,他们可以在不表现症状的情况下传播病毒。
- 有症状 ($I$): 以 $\rho$ 的概率,他们成为有症状者,以 $\rho\sigma E$ 的速率进入有症状 ($I$) 隔室。在这里,他们表现出症状,并且通常更具传染性。
-
传染期和康复($A$ 和 $I$ 隔室):
- 从 $A$: 我们的无症状个体可以以 $\gamma_A A$ 的速率康复,进入已康复 ($R$) 隔室。他们也可能以 $dA$ 的速率自然死亡。
- 从 $I$: 我们的有症状个体可以以 $\gamma_I I$ 的速率康复,同样进入 $R$ 隔室。然而,他们面临额外的风险:以 $\mu I$ 的速率因疾病死亡,或以 $dI$ 的速率自然死亡。
-
暂时免疫($R$ 和 $V$ 隔室): 一旦进入 $R$(已康复)或 $V$(已接种疫苗)状态,我们的个体将享受一段完全免疫期。但这种免疫并非永久。
- $V$ 的衰减: 已接种疫苗的个体以 $\delta_V V$ 的速率失去免疫力,转变为$S_1$(第一阶段衰减免疫力) 隔室。
- $R$ 的衰减: 自然康复的个体以 $\delta_R R$ 的速率失去自然免疫力,同样转变为 $S_1$。
- 自然死亡: $V$ 或 $R$ 隔室中的个体也可能分别以 $dV$ 和 $dR$ 的速率自然死亡。
-
免疫力下降($S_1$ 和 $S_2$ 隔室):
- 从 $S_1$: $S_1$ 隔室中的个体具有部分衰减的免疫力。他们可以:
- 以 $\alpha S_1$ 的速率再次接种疫苗,返回 $V$ 隔室。
- 以 $dS_1$ 的速率自然死亡。
- 以较低的 $\epsilon_1\lambda(t)S_1$ 速率再次感染,返回 $E$ 隔室。
- 以 $\delta_{S_1} S_1$ 的速率经历进一步的免疫力衰减,转变为$S_2$(第二阶段衰减免疫力) 隔室。
- 从 $S_2$: $S_2$ 隔室中的个体具有显著衰减的免疫力。他们可以:
- 以 $\alpha S_2$ 的速率再次接种疫苗,返回 $V$ 隔室。
- 以 $dS_2$ 的速率自然死亡。
- 以(可能更高)的较低 $\epsilon_2\lambda(t)S_2$ 速率再次感染,返回 $E$ 隔室。
- 从 $S_1$: $S_1$ 隔室中的个体具有部分衰减的免疫力。他们可以:
这种连续的流动,个体根据这些速率在隔室之间移动,描述了人群中免疫和感染的整个生命周期。
优化动力学
该模型是一个常微分方程系统,它不像机器学习算法那样通过最小化损失函数来“学习”或“更新”。相反,它的“动力学”指的是系统状态如何随时间演变,以及它会稳定到什么稳定或不稳定的模式。这里的“优化”在于理解疾病得到控制或持续存在的条件。
-
达到平衡: 系统的自然趋势是演变到平衡点,此时所有隔室的变化速率都为零 ($dS/dt = 0, dV/dt = 0$ 等)。这些是系统的“稳态”。
- 无病平衡 (DFE): 这是一个没有暴露、无症状或有症状个体存在的状态 ($E=A=I=0$)。疾病已经消失。
- 地方性流行平衡 (EE): 这是一个疾病在人群中持续存在的状态,有恒定的(非零)感染个体数量。
-
基本再生数 ($R_0$): 这个关键参数是系统行为的主要“开关”。它源自模型的参数,代表一个感染个体在完全易感人群中平均引起的继发感染数量。
- 如果 $R_0 < 1$: 无病平衡点是局部渐近稳定的。这意味着如果初始感染个体数量足够少,疾病将自然消亡。系统“收敛”到没有疾病的状态。
- 如果 $R_0 > 1$: 无病平衡点是不稳定的。这意味着疾病可以传播并可能变得地方性流行。系统将远离无病状态。
-
分岔分析:系统的“相变”: 这是模型复杂动力学真正闪光的地方。分岔描述了当参数(如直接影响 $R_0$ 的传播率 $\beta$)变化时,系统行为的定性变化。
- 正向分岔: 在典型情况下,当 $R_0$ 从下方跨越 1 时,DFE 失稳,并出现一个稳定的地方性流行平衡。这是一个“平滑”的过渡,如果传播率足够高,疾病就会变得地方性流行。
- 负向分岔: 这是一种更复杂且令人担忧的动力学。它意味着即使在 $R_0 < 1$ 时,也可能存在一个稳定的地方性流行平衡。在这种情况下,即使基本再生数表明疾病应该消亡,疾病也可能持续存在。结果取决于初始感染个体的数量(一种称为双稳态的现象)。这是公共卫生的关键见解,因为如果初始感染水平很高,仅仅将 $R_0$ 降至 1 以下可能不足以根除疾病。
- 鞍节点分岔: 当两个平衡点(通常是一个稳定的和一个不稳定的地方性流行平衡)随着参数变化而出现或消失时,就会发生这种情况。论文指出,这可能发生在正向分岔的扩展分支上,导致复杂双稳态动力学。
-
通过 MCMC 进行参数估计: 为了使模型的动力学反映现实场景,作者使用实际的 COVID-19 数据来“训练”或“拟合”模型。他们采用马尔可夫链蒙特卡洛 (MCMC) 算法来估计随时间变化的传播率 $\beta(t)$ 和疫苗接种率 $\alpha(t)$。
- 工作原理: MCMC 是一种计算技术,可以从概率分布中生成样本。在此上下文中,它会迭代地提出未知参数(各个时间点的 $\beta(t)$ 和 $\alpha(t)$,由样条节点表示)的新值,并根据模型输出与观察到的每日新增确诊病例和疫苗接种剂数的匹配程度来接受或拒绝它们。
- 从数据中“学习”: 经过许多次迭代,MCMC 算法会探索参数空间,最终收敛到与观测数据最一致的参数值分布。这个过程使模型能够从经验证据中“学习”潜在的传播和疫苗接种动力学,从而调整其参数以最好地描述现实世界的流行病曲线。使用分段三次样条来表示 $\beta(t)$ 和 $\alpha(t)$ 允许模型适应随时间变化的非恒定速率的“学习”,从而捕捉不断变化的公共卫生干预措施或病毒变种的影响。
本质上,该模型的“优化动力学”并非寻找一个单一的最优解,而是理解各种可能的长期行为(平衡点)以及这些行为如何随着关键参数的变化而变化,并通过拟合真实世界数据来获得信息。负向分岔和双稳态的存在突显了流行病控制的复杂性,有时甚至是反直觉的。
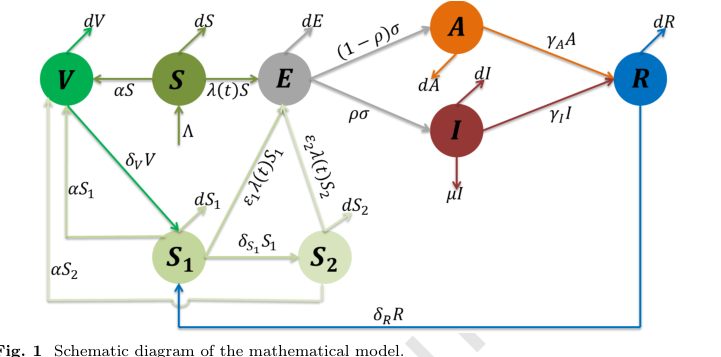 Figure 1. Schematic diagram of the mathematical model
Figure 1. Schematic diagram of the mathematical model
结果、局限性与结论
实验设计与基线模型
为了严格验证其数学论断,作者构建了一个实验,核心在于将他们新颖的两阶段免疫衰减模型(方程 (2))拟合到真实世界的流行病学数据。在此背景下,主要的“受害者”或基线模型并非直接可比的替代模型,而是更简单流行病学框架的固有局限性,这些框架未能捕捉免疫衰减和时变干预措施的复杂非线性动力学。其模型有效性的决定性证据在于其准确重现已观察到的流行趋势的能力。
实验设置包括收集美国的新冠肺炎(COVID-19)监测数据,时间跨度从2020年12月14日至2022年6月6日。该数据集包括每日新增确诊的新冠肺炎病例和每日新增接种疫苗剂量。为缓解短期波动和周期性模式的影响,对原始数据应用了7日移动平均。
设计的一个关键方面是对关键参数的处理:传播率 $\beta(t)$ 和疫苗接种率 $\alpha(t)$ 被视为时变的。为了估计这些动态参数,采用了分段三次样条函数。具体而言,$\beta(t)$ 使用18个样条节点和30天的节点间隔进行近似,而 $\alpha(t)$ 使用36个样条节点和更短的15天节点间隔,以适应其更快速的波动。随后利用马尔可夫链蒙特卡洛(MCMC)算法进行参数估计,获得这些时变参数以及表4中列出的其他参数的最优值。这种方法使模型能够适应不断演变的疫情形势,间接考虑了新变种和行为变化等因素。
证据证明的内容
证据有力地支持了该模型捕捉免疫衰减丰富动力学及其对 SARS-CoV-2 传播影响的能力。最令人信服的证明是模型模拟数据(每日新增确诊病例和疫苗接种剂量)与美国实际观测数据之间的紧密一致性,如图3所示。这种成功的拟合提供了无可辩驳的证据,表明两阶段免疫衰减过程的核心机制,结合时变传播率和疫苗接种率,在现实中是有效的。
除了简单的数据拟合,数值模拟还严格验证了关于分岔动力学的理论预测:
- 正向和反向分岔: 该模型在 $R_0 = 1$ 处始终表现出正向和反向分岔。虽然正向分岔意味着当 $R_0 > 1$ 时,疫情会稳定下来,但反向分岔的出现是一个关键发现。它明确证明,在某些参数条件下,即使基本再生数 $R_0 < 1$,也可能存在一个稳定的地方性均衡。这意味着将 $R_0$ 降低到一以下并不自动保证疾病的根除,这揭示了一个比简单模型所暗示的更复杂的现实。
- 双稳态和多稳态: 分析显示,系统可以表现出双稳态或多稳态,这意味着根据参数值,可以共存零个、一个、两个甚至三个地方性均衡。这表明疫情的长期结果(根除或持续存在)可能高度依赖于初始条件,尤其是在某些 $R_0$ 范围内。
- 鞍节点分岔: 数值模拟进一步表明,在跨界分岔的扩展分支上可能发生鞍节点分岔。这种现象导致两个稳定的地方性均衡共存,强化了双稳态的概念,并表明疫情的轨迹可以根据初始条件收敛到不同的稳定状态。
此外,关键参数的敏感性分析为有效的控制措施提供了清晰的见解:
- 免疫衰减持续时间: 证据明确表明,延长继发性免疫衰减(自然感染和疫苗诱导)的持续时间,可以显著减少有症状感染的数量并降低总体感染风险。
- 疫苗接种率: 事实证明,更高的疫苗接种覆盖率可以显著缓解感染高峰并降低总体感染风险。
- 相对易感性: 较低的相对易感性(即更强的免疫力)会导致更有利的感染动力学。研究表明,当相对易感性($\epsilon_1$ 和 $\epsilon_2$)较高时,疫情高峰可能提前出现且更为严重。相反,中等值可以延迟高峰,为干预措施提供宝贵的时间。研究表明,提高疫苗接种覆盖率和调节相对易感性的组合效应可以降低感染高峰。
总而言之,证据表明所提出的两阶段免疫衰减模型提供了对 SARS-CoV-2 动力学更细致、更准确的理解,强调了持续免疫、高疫苗接种率和降低易感性在控制疫情中的关键作用。
局限性与未来方向
尽管本研究为理解免疫衰减及其对 SARS-CoV-2 传播的影响提供了一个严谨的框架,但认识到其固有的局限性并考虑未来发展的方向至关重要。
一个显著的局限性是,该模型中的时变传播率和疫苗接种率虽然在拟合真实世界数据方面有效,但它们隐式地捕捉了多种外部因素的影响,例如新病毒变种(如 Delta、Omicron)的出现、人类行为的变化以及非药物干预措施的实施。然而,该模型无法区分这些因素的个体贡献。这意味着我们可以看到“发生了什么”,但无法精确知道“为什么”是由于特定的外部驱动因素。
此外,当前模型并未区分各种疫苗类型或其不同的效力。它也没有明确考虑人群中的行为异质性或疾病传播的空间结构。这些简化措施虽然有助于数学上的可处理性,但限制了模型在反映真实流行病学场景全部复杂性方面的精细度。
展望未来,出现了几个讨论话题,以进一步发展和演进这些发现:
- 解耦外部因素: 未来的研究可以侧重于开发子模型或整合额外的数据流,以明确建模特定病毒变种、行为转变或非药物干预措施对传播率和疫苗接种率的影响。这将有助于更精细地理解它们对疫情动力学的个体贡献。
- 疫苗异质性和效力: 将模型演化为区分不同的疫苗平台(例如,mRNA、病毒载体)及其特定的衰减曲线和效力,将显著增强其生物学真实性和对定制疫苗接种策略的预测能力。
- 空间和社会动力学: 将空间组成部分和行为异质性(例如,对公共卫生措施的不同依从性、社会网络结构)整合到模型中,可以为局部疫情、超级传播事件以及地理定向干预措施的有效性提供见解。
- 长期免疫印迹: 研究结果强调了延长疫苗诱导保护和人群覆盖率的重要性,这表明需要对免疫印迹效应进行更深入的研究。我们如何设计疫苗接种计划或加强针策略,以最大化对不断演变的病原体的免疫反应的广度和持久性?
- 反向分岔和双稳态的政策含义: 证明即使在 $R_0 < 1$ 的情况下疫情也可能持续存在(由于反向分岔),并且结果可能取决于初始条件(双稳态),这对公共卫生政策提出了严峻的挑战。这需要从仅关注将 $R_0$ 降低到一以下,转向更动态、更具适应性的策略,这些策略需要考虑初始条件、人群免疫格局以及在看似受控的环境中复发的可能性。需要哪些新的指标或阈值来指导此类复杂系统中的政策?
- 免疫衰减和疫苗接种策略的经济和社会成本: 进一步的研究可以整合与不同免疫衰减率和疫苗接种策略相关的经济和社会成本。这将提供对公共卫生决策中权衡取舍的更全面理解,例如投资于更持久的疫苗而非频繁的加强针接种活动。
从本次分析中获得的见解对于优化疫苗接种策略和开发更持久有效的疫苗至关重要。所揭示的复杂动力学,特别是反向分岔和双稳态,强调疫情控制不是一个简单的线性问题,而是一个多方面的挑战,需要持续的适应以及对免疫学和流行病学相互作用的深刻理解。
与其他域的同构
结构骨架
核心机制是一个多室动态系统,模拟实体在状态之间的流动和转化,并基于关键速率参数表现出分岔和双稳态等复杂的非线性行为。
