基于膝关节MR图像重构健康画像的患者特异性放射组学特征选择
New method combines interpretable "radiomic features" with AI-generated "healthy scans" for better, explainable medical image analysis.
背景与学术渊源
膝关节损伤(如前交叉韧带(ACL)或半月板撕裂)的诊断长期以来依赖于准确性有限的体格检查。磁共振(MR)成像虽是临床金标准,但利用端到端深度学习(DL)模型进行的自动化分析往往表现为“黑盒”。这种透明度的缺失使得临床医生难以理解模型做出特定诊断的逻辑,而这正是医疗决策中的关键痛点。尽管经典放射组学(如强度或形状等手工特征)具有高可解释性,但其性能往往不及复杂的深度学习模型。作者旨在通过构建一个框架来弥合这一差距,该框架在保持放射组学可解释性的同时,实现了与SOTA深度学习模型相当的性能。
直观领域术语
- 放射组学 (Radiomics): 可将其视为医学图像的“数字指纹”。计算机不再仅仅观察图像,而是提取数百个微小且具体的数学度量(如纹理、形状或强度模式),这些度量对于人眼而言过于细微,难以进行一致性量化。
- 健康画像 (Healthy Persona): 想象医生通过将受损肢体与同一患者的“完美”肢体进行对比来诊断骨折。作者利用AI“构想”出患者膝关节在健康状态下的样貌,从而提供一个基准,精确凸显病理特征偏离正常状态的位置。
- 去噪扩散概率模型 (DDPM): 可将其视为一种高度复杂的“图像修复器”。它通过练习如何从图像中去除“噪声”(随机静态干扰)来学习健康膝关节的统计模式,直至仅保留清晰的健康结构。它利用这一能力从受损输入中重构出“健康画像”。
符号表
| 符号 | 描述 |
|---|---|
| $\mathbf{x}$ | 包含感兴趣区域(ROI)的输入图像块。 |
| $\mathbf{f}$ | 从图像中提取的 $F$ 个放射组学特征池。 |
| $g_\theta(\mathbf{x})$ | 具有参数 $\theta$ 的特征加权神经网络。 |
| $\mathbf{p}$ | 用于选择特定特征的预测概率。 |
| $\mathbf{f}^w$ | 用于分类的加权特征向量,$\mathbf{f}^w = \{p_i f_i\}_{i=1}^F$。 |
| $r_\phi(\mathbf{f}^w)$ | 具有参数 $\phi$ 的逻辑回归分类器。 |
| $\mathbf{x}^{\text{persona}}$ | 患者图像的合成健康版本。 |
数学解释
作者将特征选择问题视为一个优化任务,模型通过学习为特征分配重要性权重。其目标是在给定图像 $\mathbf{x}$ 的条件下,最大化正确分类的似然度。
类别 $c$ 与特征 $\mathbf{f}$ 的联合概率建模为:
$$P(c, \mathbf{f} | \mathbf{x}; \theta, \phi) = P(c | \mathbf{f}, \mathbf{x}; \phi) \times P(\mathbf{f} | \mathbf{x}; \theta)$$
由于特征提取函数 $\mathbf{f} = e(\mathbf{x})$ 是确定性的,模型简化了边缘化过程,重点关注分类概率 $P(c | \mathbf{x}; \theta, \phi)$。训练目标是最小化负对数似然(交叉熵损失):
$$\mathcal{L}_{\text{loss}}(\theta, \phi) = -\sum_{i=1}^{N} \log P(\hat{c}^i | \mathbf{x}^i; \theta, \phi)$$
通过最小化该损失,模型同时学习选择最相关的放射组学特征(通过 $\theta$)并对损伤进行分类(通过 $\phi$)。推理阶段的“硬选择”(使用阈值 $T$ 对概率进行二值化)是一种启发式方法,它弥合了软训练权重与临床可解释性所需的离散特征集之间的差距。健康画像的引入有效地将特征池扩大至 $F = 6mP$,使模型能够将患者的实际状态与其自身重构的健康基准进行对比,这是隔离病理变化的有效手段。
该框架成功证明,通过将生成式AI与传统统计模型相结合,我们可以在不牺牲特征“人类可解释性”的前提下实现高性能诊断。这是一种稳健的医学图像分析方法,标志着迈向可信AI的重要一步。
问题定义与约束
核心问题表述与困境
起点(输入):
当前膝关节损伤的医学影像诊断由两种竞争范式主导:“手工”放射组学特征(可解释但性能较弱)与端到端深度学习(强大但缺乏透明度)。
终点(目标):
作者旨在通过创建一个框架来弥合这一差距,该框架在实现深度学习高诊断性能的同时,保留经典放射组学的人类可读性。
困境与约束:
1. 可解释性壁垒: 标准深度学习模型是不透明的。
2. 特征选择瓶颈: 使用所有放射组学特征会导致“维度灾难”。
3. 基准缺失: 若无患者特异性的健康基准,难以精确量化组织偏离健康状态的程度。
4. 计算与数据约束: 作者必须克服训练生成模型(DDPM)以准确重构健康组织的难度,同时避免引入可能偏倚后续放射组学分析的伪影。
方案优势
作者识别出了一个根本瓶颈:端到端深度学习的“黑盒”性质。他们开发了一个利用深度学习来优化放射组学特征选择的框架。
方法逻辑
- 特征加权网络: 3D-ResNet-18 作为门控机制,为放射组学特征池预测概率 $p = \{p_i\}_{i=1}^F$。
- 健康画像: 他们使用 3D 去噪扩散概率模型(DDPM)重构患者膝关节的“健康画像”。通过从病理图像及其合成的健康对应物中提取特征,他们创建了一个能更有效凸显异常的差异化特征集。
比较优势
- 结构优势: 该方法将输入简化为一组可解释的、基于块的放射组学特征,保持了线性的、人类可解释的决策边界。
- 生成式增强: DDPM 提供了一个明确的、患者特异性的参考点,减轻了分类器推断基准解剖结构的负担。
数学与逻辑机制
训练过程的核心是最小化负对数似然:
$$\mathcal{L}_{\text{loss}}(\theta, \phi) = -\sum_{i=1}^{N} \log P(\hat{c}^i | \mathbf{x}^i; \theta, \phi)$$
步骤流程
- 输入: 原始 MRI 块 $\mathbf{x}$ 进入系统。
- 画像生成: 3D DDPM 接收掩码后的病理图像并“填补空白”,生成健康画像。
- 特征提取: 系统从原始块和健康画像中提取放射组学特征。
- 加权: 特征加权网络 $g_\theta(\mathbf{x})$ 为每个特征分配概率 $p_i$。
- 分类: 加权特征 $\mathbf{f}^w = \{p_i f_i\}$ 被输入到逻辑回归模型 $r_\phi$ 中。
结果、局限性与结论
成功证据
作者的方法击败了多个基准模型,包括 MRNet、ELNet 和 SKID。
* 性能: 该方法在一般异常检测中达到了 0.90 的准确率,在半月板撕裂检测中达到了 0.82。
* 消融实验证明: 移除“健康画像”或“特征加权网络”会导致性能出现统计学意义上的显著下降。
未来讨论议题
- 向其他病理的泛化: 这种“健康画像”方法能否应用于肿瘤等更复杂、异质性更强的疾病?
- 不确定性量化: 未来的迭代可以探索概率阈值化,为放射科医生提供“置信度评分”。
- 计算效率: 我们能否开发这些生成模型的“蒸馏”版本,以近乎实时的速度提供健康画像?
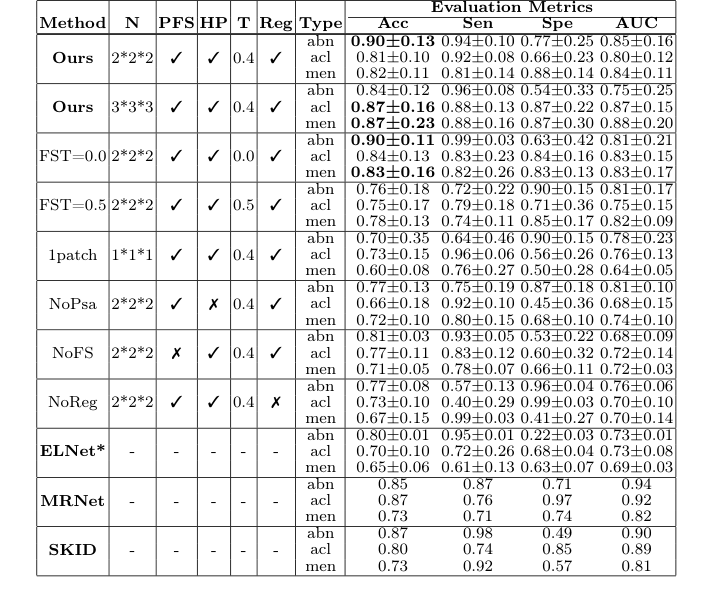 Table 1. Comparison of different configurations and methods. N: Number of subpatches; PFS: Patient-specific features selection; HP: Healthy persona; T: Feature selection threshold; Reg: Registration in preprocessing. * denotes repro- duced results
Table 1. Comparison of different configurations and methods. N: Number of subpatches; PFS: Patient-specific features selection; HP: Healthy persona; T: Feature selection threshold; Reg: Registration in preprocessing. * denotes repro- duced results
与其他领域的同构性
患者特异性放射组学特征选择分析
本文通过提出一种结合经典放射组学特征与生成式“健康画像”模型的混合框架,解决了深度学习的“黑盒”问题。
