Выбор радиомических признаков для конкретного пациента с использованием реконструированной «здоровой персоны» на МРТ коленного сустава
Диагностика травм коленного сустава, таких как разрывы передней крестообразной связки (ПКС) или мениска, исторически опиралась на физикальное обследование, обладающее ограниченной точностью.
Общие сведения и академический контекст
Диагностика травм коленного сустава, таких как разрывы передней крестообразной связки (ПКС) или мениска, исторически опиралась на физикальное обследование, обладающее ограниченной точностью. Магнитно-резонансная томография (МРТ) является клиническим «золотым стандартом», однако автоматизированный анализ с использованием end-to-end Deep Learning (DL) моделей зачастую функционирует как «черный ящик». Отсутствие прозрачности не позволяет клиницистам понять, почему модель выносит конкретный диагноз, что является критической проблемой при принятии медицинских решений. Хотя классическая радиомика (признаки, созданные вручную, такие как интенсивность или форма) обеспечивает высокую интерпретируемость, она часто уступает по эффективности сложным DL-моделям. Авторы стремились преодолеть этот разрыв, создав фреймворк, который сохраняет интерпретируемость радиомики, достигая при этом производительности, сопоставимой с SOTA DL-моделями.
Интуитивно понятные доменные термины
- Радиомика (Radiomics): Это своего рода «цифровое дактилоскопирование» медицинских изображений. Вместо простого визуального осмотра компьютер извлекает сотни специфических математических показателей (текстура, форма, паттерны интенсивности), которые слишком тонки для количественной оценки человеческим глазом.
- Здоровая персона (Healthy Persona): Представьте врача, который диагностирует перелом, сравнивая поврежденную конечность с «идеальной» версией конечности того же пациента. Авторы используют ИИ, чтобы «вообразить», как выглядело бы колено пациента, будь оно абсолютно здоровым, создавая базис для точного выявления отклонений патологии от нормы.
- Denoising Diffusion Probabilistic Model (DDPM): Это высокотехнологичный «реставратор изображений». Модель обучается статистическим закономерностям здоровых коленей, практикуясь в удалении «шума» (случайных помех) до тех пор, пока не останется четкая здоровая структура. Этот навык используется для реконструкции «здоровой персоны» на основе поврежденного входного изображения.
Таблица обозначений
| Обозначение | Описание |
|---|---|
| $\mathbf{x}$ | Входной фрагмент изображения, содержащий область интереса (ROI). |
| $\mathbf{f}$ | Пул из $F$ радиомических признаков, извлеченных из изображения. |
| $g_\theta(\mathbf{x})$ | Нейронная сеть для взвешивания признаков с параметрами $\theta$. |
| $\mathbf{p}$ | Предсказанные вероятности выбора конкретных признаков. |
| $\mathbf{f}^w$ | Взвешенный вектор признаков для классификации, $\mathbf{f}^w = \{p_i f_i\}_{i=1}^F$. |
| $r_\phi(\mathbf{f}^w)$ | Классификатор логистической регрессии с параметрами $\phi$. |
| $\mathbf{x}^{\text{persona}}$ | Синтезированная здоровая версия изображения пациента. |
Математическая интерпретация
Авторы решают задачу выбора признаков как задачу оптимизации, в которой модель учится присваивать веса важности признакам. Цель состоит в максимизации правдоподобия (likelihood) правильной классификации при заданном изображении $\mathbf{x}$.
Совместная вероятность класса $c$ и признаков $\mathbf{f}$ моделируется как:
$$P(c, \mathbf{f} | \mathbf{x}; \theta, \phi) = P(c | \mathbf{f}, \mathbf{x}; \phi) \times P(\mathbf{f} | \mathbf{x}; \theta)$$
Поскольку функция извлечения признаков $\mathbf{f} = e(\mathbf{x})$ является детерминированной, модель упрощает маргинализацию, фокусируясь на вероятности классификации $P(c | \mathbf{x}; \theta, \phi)$. Целевая функция обучения заключается в минимизации отрицательного логарифмического правдоподобия (cross-entropy loss):
$$\mathcal{L}_{\text{loss}}(\theta, \phi) = -\sum_{i=1}^{N} \log P(\hat{c}^i | \mathbf{x}^i; \theta, \phi)$$
Минимизируя эту функцию потерь, модель одновременно учится выбирать наиболее релевантные радиомические признаки (через $\theta$) и классифицировать повреждение (через $\phi$). «Жесткий отбор» (hard selection) на этапе инференса (бинарная классификация вероятностей с порогом $T$) представляет собой эвристику, связывающую «мягкие» веса обучения с необходимостью дискретного набора признаков для клинической интерпретируемости. Включение «здоровой персоны» эффективно удваивает пул признаков до $F = 6mP$, позволяя модели сравнивать фактическое состояние пациента с его собственным реконструированным здоровым базисом, что является эффективным способом изоляции патологических изменений.
Фреймворк успешно демонстрирует, что сочетание генеративного ИИ с традиционными статистическими моделями позволяет достичь высокой диагностической точности, не жертвуя «человекочитаемой» природой признаков. Это надежный подход к анализу медицинских изображений, представляющий собой значительный шаг в сторону доверенного ИИ (trustable AI).
Постановка задачи и ограничения
Формулировка основной проблемы и дилемма
Исходная точка (Input):
Современная диагностика травм коленного сустава доминируется двумя конкурирующими парадигмами: «ручными» радиомическими признаками (интерпретируемыми, но слабыми) и end-to-end Deep Learning (мощными, но непрозрачными).
Желаемый результат (Goal):
Авторы стремятся преодолеть этот разрыв, создав фреймворк, который обеспечивает высокую диагностическую эффективность глубокого обучения, сохраняя при этом интерпретируемость классической радиомики.
Дилемма и ограничения:
1. Барьер интерпретируемости: Стандартные DL-модели непрозрачны.
2. Узкое место выбора признаков: Использование всех радиомических признаков приводит к «проклятию размерности».
3. Отсутствие базиса: Без специфического для пациента здорового базиса сложно количественно оценить степень отклонения ткани от здорового состояния.
4. Вычислительные ограничения и ограничения данных: Авторам пришлось преодолеть трудности обучения генеративной модели (DDPM) для точной реконструкции здоровой ткани без внесения артефактов, которые могли бы исказить последующий радиомический анализ.
Обоснование подхода
Авторы выявили фундаментальное узкое место: «черный ящик» end-to-end DL. Они разработали фреймворк, использующий DL для оптимизации выбора радиомических признаков.
Логика подхода
- Сеть взвешивания признаков: 3D-ResNet-18 действует как механизм гейтирования, предсказывая вероятности $p = \{p_i\}_{i=1}^F$ для пула радиомических признаков.
- Здоровая персона: Использована 3D DDPM для реконструкции «здоровой персоны» колена пациента. Извлекая признаки как из патологического изображения, так и из его синтетического здорового аналога, авторы создали дифференциальный набор признаков, более эффективно выделяющий аномалии.
Сравнительное преимущество
- Структурное преимущество: Метод сводит входные данные к набору интерпретируемых радиомических признаков на основе патчей, поддерживая линейную, понятную человеку границу принятия решений.
- Генеративная аугментация: DDPM предоставляет явную, специфичную для пациента точку отсчета, снижая нагрузку на классификатор по определению базовой анатомии.
Математический и логический механизм
Ядром процесса обучения является минимизация отрицательного логарифмического правдоподобия:
$$\mathcal{L}_{\text{loss}}(\theta, \phi) = -\sum_{i=1}^{N} \log P(\hat{c}^i | \mathbf{x}^i; \theta, \phi)$$
Пошаговый процесс
- Вход: Необработанный МРТ-патч $\mathbf{x}$ поступает в систему.
- Генерация персоны: 3D DDPM принимает маскированное патологическое изображение и «заполняет пробелы», генерируя здоровую персону.
- Извлечение признаков: Система извлекает радиомические признаки как из исходного патча, так и из здоровой персоны.
- Взвешивание: Сеть взвешивания признаков $g_\theta(\mathbf{x})$ присваивает вероятность $p_i$ каждому признаку.
- Классификация: Взвешенные признаки $\mathbf{f}^w = \{p_i f_i\}$ подаются в модель логистической регрессии $r_\phi$.
Результаты, ограничения и заключение
Доказательства эффективности
Авторы превзошли несколько базовых моделей, включая MRNet, ELNet и SKID.
* Производительность: Метод достиг точности 0.90 для общих аномалий и 0.82 для разрывов мениска.
* Абляционное исследование: Удаление «здоровой персоны» или «сети взвешивания признаков» приводило к статистически значимому снижению производительности.
Темы для будущих дискуссий
- Обобщение на другие патологии: Может ли этот подход со «здоровой персоной» быть применен к более сложным, гетерогенным заболеваниям, таким как опухоли?
- Количественная оценка неопределенности: Будущие итерации могут исследовать вероятностное пороговое значение для предоставления радиологам «оценки уверенности» (confidence score).
- Вычислительная эффективность: Можно ли разработать «дистиллированные» версии этих генеративных моделей, обеспечивающие создание здоровой персоны в режиме, близком к реальному времени?
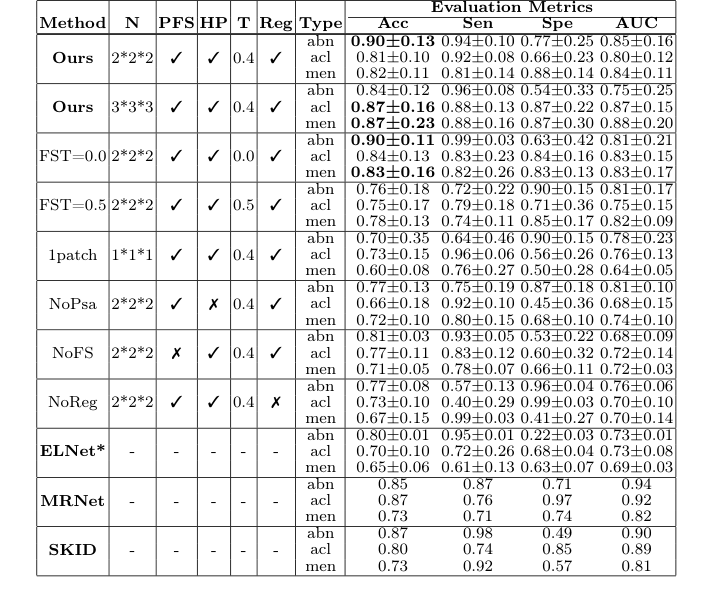 Table 1. Comparison of different configurations and methods. N: Number of subpatches; PFS: Patient-specific features selection; HP: Healthy persona; T: Feature selection threshold; Reg: Registration in preprocessing. * denotes repro- duced results
Table 1. Comparison of different configurations and methods. N: Number of subpatches; PFS: Patient-specific features selection; HP: Healthy persona; T: Feature selection threshold; Reg: Registration in preprocessing. * denotes repro- duced results
