多機能光ファイバー・セラノスティックプローブによる閉ループ腫瘍光熱療法
The combination of optical fiber and phototheranostic agents has emerged as a promising strategy to address the challenges of limited light penetration depth and systemic toxicity of nanomaterials.
背景と学術的系譜
起源と学術的系譜
本稿で取り上げる問題は、年間数百万人の新規患者と死亡者を出す、がんという地球規模の重大な健康課題に端を発する。この悲惨な状況は、より正確かつ効果的な診断・治療法の開発に向けた広範な研究を促進してきた。この文脈において、「セラノスティクス」という概念が登場し、診断機能と治療機能を単一の空間的に共局在するプラットフォームに統合し、即時的かつ標的化された治療とリアルタイムモニタリングを可能にすることを目指している。
特に、診断と治療の両方に光を利用するフォトセラノスティクスは、その高い特異性、時空間的制御性、および非電離性から大きな注目を集めている。しかし、その臨床応用は、生物組織における光の浸透深度の固有の限界(散乱と吸収により通常10 mm未満)と、セラノスティクス剤として使用されるナノマテリアルの健康組織への非特異的蓄積による全身毒性という、二つの主要な障害に直面していた。
光ファイバーと光セラノスティクス剤の組み合わせは、これらの限界を克服する有望な戦略として特定された。光ファイバーは、深部腫瘍への効率的な光伝送を促進し、治療剤の局所的封じ込めを可能にすることで、全身毒性を軽減する。これらの利点にもかかわらず、従来の光ファイバープローブ設計は、いくつかの「痛点」に悩まされていた。既存のアプローチのほとんどは、ファイバーあたりの単一機能実装に限定されるか、あるいは試薬間のスペクトル重複による機能間クロストークを経験していた。このため、しばしばマルチファイバー構成が必要となり、デバイスの剛性増加、大型化、より侵襲的な処置、およびリアルタイム治療フィードバックの欠如につながっていた。これらの問題は、組織損傷および治療後炎症のリスクを増大させ、広範な臨床導入を妨げていた。本稿は、波長分割多重(WDM)技術に着想を得た、単一ファイバー多機能統合スキームを提案することにより、これらの根本的な限界に直接対処し、リアルタイムフィードバックを伴う閉ループ腫瘍光熱療法を可能にする。
直感的ドメイン用語
- セラノスティクス (Theranostics): 体内のどこが悪いかを即座に医師に伝え、その正確な場所に適切な治療を一度に施すことができる、非常に高度な医療ツールの「診断・治療」スーパーヒーローのようなものを想像してください。診断と治療の組み合わせです。
- 光熱療法 (Photothermal Therapy, PTT): 虫眼鏡が葉っぱの小さな部分に太陽光を集中させて焦がすことができるように、非常に焦点を絞った小さなレーザービームを使って、不要な細胞を穏やかに加熱して破壊することだと考えてください。「光(photo)」の部分は光が使われることを意味し、「熱(thermal)」の部分は熱が発生することを意味します。
- 波長分割多重 (Wavelength Division Multiplexing, WDM): 非常に忙しい一本の高速道路を想像してください。ただし、車ではなく、それぞれが異なる「色」の光に乗って移動するさまざまな種類の情報が運ばれています。これにより、多くの異なる信号が互いに干渉することなく同じファイバー上を同時に移動でき、道路の効率が大幅に向上します。
- 腫瘍微小環境 (Tumor Microenvironment, TME): これは、腫瘍の成長を支えるすべての細胞、血管、化学信号を含む、腫瘍の直接的な周囲環境を指します。これは、腫瘍が自らのために作り出す特定の「近所」のようなもので、しばしば健康な組織とは異なり、より酸性であることが多いです。
- 比率蛍光プローブ (Ratiometric Fluorescent Probes): 単に一つの色の光の明るさを測定するだけでなく、二つの異なる色の明るさを測定し、それらの比率を比較するスマートな光センサーを考えてみてください。これにより、全体的な明るさが外部要因によって変化した場合でも、測定がはるかに信頼性が高く正確になります。これは、単一の数値に頼るよりも二つの数値を比較する方が、より安定した結果が得られるのと似ています。
記法表
| 記法 | 説明 |
|---|---|
| $I_{450}/I_{405}$ | 450 nm と 405 nm における蛍光強度の比率。pHセンシングに使用。 |
| $R$ | pH分解能。信頼性をもって検出可能な最小のpH変化を示す。 |
| $s$ | 感度。pHキャリブレーション曲線の傾きを表す。 |
| $T_1$ | pHまたは温度センシングにおいて、値が増加するときの応答時間。 |
| $T_2$ | pHまたは温度センシングにおいて、値が減少するときの応答時間。 |
| $I_{618}/I_{546}$ | 618 nm と 546 nm における蛍光強度の比率。温度センシングに使用。 |
| $p$ | p値。実験結果の有意性を判断するために使用される統計的尺度。 |
| $V/V_0$ | 正規化腫瘍体積。初期体積に対する腫瘍体積の比率を表す。 |
| $\sigma$ | 標準偏差。一連の値の変動または分散の量を示す尺度。 |
問題定義と制約
中核問題の定式化とジレンマ
本稿が取り組む根本的な問題は、効果的かつ低侵襲ながんセラノスティクス(診断と治療を組み合わせたアプローチ)という、極めて重要なニーズに起因する。現在の方法には、臨床応用を妨げる重大な限界が存在する。
入力/現状は、いくつかの欠点によって特徴づけられる:
1. 限定的な光浸透と全身毒性: 伝統的な光セラノスティクス剤は、しばしばナノマテリアルベースであり、散乱と吸収により、組織への光浸透深度が固有に限定されている(通常10 mm未満)。さらに、正常組織や臓器への非特異的な蓄積が全身毒性を引き起こす。
2. 光ファイバーの多重化ポテンシャルの過小評価: 光ファイバーは深部腫瘍へのアクセスや薬剤の局所的封じ込めといった利点を提供するが、単一プラットフォームへの複数機能統合の可能性は、ほとんど活用されてこなかった。
3. 機能間クロストークとデバイスの複雑性: 従来の光ファイバープローブは、ファイバーあたりの単一機能実装に限定されるか、複数の機能を統合しようとする際に機能間クロストークに悩まされていた。このクロストークは、主に異なる機能性試薬の吸収または発光帯間のスペクトル重複に起因していた。これを回避するために、研究者はしばしばマルチファイバー構成に頼っていたが、これは必然的にデバイスの剛性と寸法を増加させ、低侵襲処置との互換性を低下させ、組織損傷および治療後炎症のリスクを高めていた。
4. リアルタイム治療フィードバックの欠如: 既存の方法は、治療量と有効性のリアルタイムモニタリング能力を欠いていることが多く、閉ループ制御と個別化精密医療を妨げている。
望ましい終点(出力/目標状態)は、以下の能力を持つ、単一のコンパクトな多機能光ファイバーセラノスティックプローブである:
1. 閉ループ腫瘍光熱療法 (PTT): リアルタイムフィードバックのための単一プラットフォーム上での診断機能と治療機能の統合を含む。
2. 多パラメータモニタリング: 特にpHと温度である、主要な腫瘍微小環境(TME)パラメータの同時モニタリングを可能にする。
3. 低侵襲処置: デバイスはコンパクト(著者らが達成したように、例えば直径440 µm)であり、腫瘍病変に処置手技でアクセス可能であり、拡大切開や繰り返しの侵襲的処置を回避する。
4. 治療前腫瘍同定: 腫瘍pH勾配を明らかにするための、腫瘍辺縁の正確な同定。
5. 治療中熱線量制御: 温度を同時にモニタリングすることによる、PTT中の熱線量の正確な制御。
6. 治療後有効性評価: 酸性TMEの逆転をモニタリングすることによる、治療有効性の迅速な評価。
7. 光浸透と毒性の克服: ナノマテリアルベースの戦略に伴う、光浸透深度と全身毒性の限界に対処する。
本稿が橋渡ししようとしている正確な欠落リンクまたは数学的ギャップは、機能間クロストークなしに複数のセラノスティクス機能(pHセンシング、温度センシング、光熱療法)を同時に実行でき、リアルタイムフィードバックを提供する、堅牢な単一ファイバープラットフォームの開発である。中核となる数学的/設計上の課題は、波長分割多重(WDM)を可能にするために、複数の機能性試薬(pH指示薬、温度指示薬、光熱剤)を選択し、共固定化することである。これらの試薬の励起および発光スペクトルは十分に分離されており、単一ファイバー上でのWDMを可能にする。これにより、個別の機能が特定の波長によってオンデマンドで活性化され、以前の単一ファイバー多重化の試みを悩ませていたスペクトル重複の問題が効果的に排除される。本稿の解決策は、吸収帯が重複しないHPTS-IP、LnMOF、およびICGを慎重に選択することであり、これによりWDMが可能になる。
過去の研究者を閉じ込めてきた痛みを伴うトレードオフまたはジレンマは、機能的多重化とデバイスの単純性/性能との間の固有の対立である。複数の機能を達成するためには、以下のいずれかを行う必要があった:
* デバイスの複雑性を増加させる: 複数のファイバーを使用し、低侵襲処置に適さないかさばる剛性デバイスにつながり、患者のリスクを高める。
* 機能的完全性を犠牲にする: 単一ファイバーに複数の試薬を統合しようとするが、スペクトル重複による深刻な機能間クロストークに遭遇し、多機能性が信頼できない、あるいは不正確になる。これは、一方の側面(例:機能の追加)を改善することが、直接もう一方(例:信号整合性またはデバイスサイズ)を壊すことを意味した。
制約と失敗モード
多機能光ファイバーセラノスティックプローブの開発という問題は、著者が直面したいくつかの厳しい現実的な壁のために、非常に困難である:
-
物理的制約:
- 限定的な光浸透深度: 生物組織における光の固有の散乱と吸収は、その浸透を厳しく制限し、通常は10 mm未満に限定される。これは、光熱療法における深部腫瘍の治療を困難にする。
- 全身毒性: セラノスティクスナノマテリアルの正常組織や臓器への非特異的蓄積は、望ましくない全身毒性を引き起こし、臨床応用の主要な障害となっている。
- デバイスの剛性と寸法: 低侵襲処置のためには、プローブは柔軟でコンパクトでなければならない。マルチファイバー設計は剛性と寸法を増加させ、処置手技との互換性を低下させ、組織損傷のリスクを高める。
- テーパーファイバー設計の限界: 光ファイバーのテーパー形状は重要である。過度に短いテーパーは光漏れのリスクがあり、信号対雑音比(SNR)を低下させる一方、長すぎるテーパーは局所的センシングと治療には適さない。チップ径は、エバネッセント場の強度(したがって蛍光励起/収集効率)と指示薬固定化のための利用可能な表面積の両方に影響するため、慎重な最適化が必要である(著者らは100 µmが最適であると見出した)。
- ハイドロゲル膜の完全性: 機能性試薬をカプセル化するために使用されるゾルゲルマトリックスは、安定しており生体適合性がある必要がある。純粋なテトラエトキシシラン(TEOS)膜は、深刻な亀裂を起こしやすく、膜の均一性が低く、浸出率が高い結果となり、センサーの安定性と生体適合性を損なう。GLYMOのような共前駆体やTriton X-100のような界面活性剤の添加は、これを軽減するために必要である。
-
データ駆動型および性能制約:
- 機能間クロストーク: 単一ファイバー上での多重化における主要な課題は、異なる機能性試薬(pH指示薬、温度指示薬、光熱剤)の励起および発光帯間のスペクトル重複を防ぐことである。この重複は、不正確な読み取りと、異なる機能からの信号を区別できないことにつながる。
- リアルタイム遅延要件: 閉ループ治療とリアルタイムモニタリングのためには、センサーは十分に高速な応答時間を持つ必要がある。本稿では、pHセンシング応答時間3.2秒(pH増加時)および12.8秒(pH減少時)、温度センシング応答時間2.0秒(温度増加時)および0.6秒(温度減少時)を報告しており、これらはin vivoモニタリングには許容範囲内と見なされている。
- センサーの安定性と信頼性: 機能性試薬は、生理環境下で経時的にファイバー表面から有意に浸出することなく、安定性を維持する必要がある。浸出試験では、蛍光強度の低下は最小限(72時間でHPTS-IPで1.6%、LnMOFで3.5%)であり、良好な安定性を示している。
- 生理学的要因からの干渉: センシング性能は、複雑な生理環境に存在する様々な干渉物質、光退色、指示薬濃度変動、およびファイバー形態の変化に対して堅牢でなければならない。比率蛍光プローブの使用と慎重な試薬選択は、これらの問題を軽減するのに役立つ。
- 組織自家蛍光: 組織からの内因性蛍光は、プローブの信号に干渉し、センシングの精度と特異性を低下させる可能性がある。エバネッセント場の浅い浸透深度は、指示薬濃度が高い場所で、高いSNRを維持するのに役立つ。
- 正確な熱線量制御: 光熱療法中、隣接する正常組織に過度の加熱を引き起こすことなく、効果的な熱線量を提供することが重要である。過熱は組織損傷、血管虚脱、および血流障害を引き起こす可能性がある。これには、正確なリアルタイム温度モニタリングが必要である。
なぜこのアプローチなのか
選択の必然性
著者らが波長分割多重(WDM)技術を活用した単一ファイバー多機能統合戦略を追求するという決定は、単なる改善ではなく、既存アプローチの固有の限界によって駆動された必然的な選択であった。本稿は、従来の「最先端(SOTA)」手法がどこで失敗したかを正確に特定している:「最近の進歩にもかかわらず、光ファイバープローブの多重化ポテンシャルは過小評価されたままである。現在の研究は、ファイバーあたりの単一機能実装に限定されるか、主に機能試薬間のスペクトル重複に起因する機能間クロストークに悩まされている。」このスペクトル重複の問題は、多パラメータモニタリングや統合セラノスティクスを達成するために、しばしばマルチファイバー構成が必要となることを意味した。しかし、そのようなセットアップは、「必然的にデバイスの剛性と寸法を増加させ、低侵襲処置との互換性を低下させ、組織損傷および治療後炎症のリスクを高める。」これらの重大な欠点—リアルタイムフィードバックの欠如、侵襲性、および機能間クロストーク—を考慮すると、パラダイムシフトが必要であった。WDMベースの単一ファイバーアプローチは、スペクトル干渉なしに単一のコンパクトなプラットフォーム上で複数の機能を可能にすることにより、これらの根本的な課題を克服する唯一の実行可能な解決策として浮上した。
比較優位性
単純な性能指標を超えて、この方法は主にその構造設計を通じて、深遠な質的優位性を提供する。中核的な利点は、波長分割多重を使用して単一光ファイバー上に複数の機能(pHセンシング、温度モニタリング、光熱療法)を統合する能力にある。この構造的革新は、スペクトル重複が信号整合性を低下させた以前のマルチエージェントシステムにおける重大な問題であった機能間クロストークを本質的に最小限に抑える。スペクトル帯域が「重複しない」試薬(HPTS-IP、LnMOF、ICG)を慎重に選択することにより、プローブは各パラメータの正確で信頼性の高い測定を保証する。
さらに、pHと温度センシングのために選択された比率蛍光プローブは、重要な質的利点を提供する。この比率検出戦略は、「光退色、指示薬濃度変動、およびファイバー形態変化がセンシング結果に与える干渉を軽減し、正確で信頼性の高い信号の取得を容易にする。」これは、ノイズや環境変動に非常に敏感な強度ベースのセンシングよりも大幅な改善である。コンパクトな単一ファイバー設計は、マルチファイバーバンドルと比較して物理的なフットプリントと剛性を劇的に低減し、低侵襲処置に対して圧倒的に優れている。また、セラノスティクス剤を局所化し、遊離ナノマテリアルに伴う全身毒性を効果的に軽減する。
制約への適合性
選択された方法は、高度なセラノスティクス応用の厳格な制約に完全に適合している。
* 低侵襲性: 単一の柔軟な光ファイバー(直径=440 µm、チップ径=100 µm)の使用は、「処置手技による腫瘍病変へのアクセス」を可能にし、マルチファイバーまたはより大きなプローブ設計と比較して侵襲性を劇的に低減する。これは、組織損傷および治療後炎症の最小化という制約に直接対応する。
* リアルタイムフィードバックと閉ループ治療: 単一プラットフォーム上でのpHと温度指示薬と光熱剤の統合は、「リアルタイムフィードバックを伴う閉ループ腫瘍光熱療法」を可能にする。これは、プローブが治療前腫瘍同定(pH勾配経由)、治療中線量制御(PTT中の温度モニタリング経由)、および治療後有効性評価(TME pH逆転のモニタリング経由)を実行できることを意味し、動的で適応的な治療に対する重要なニーズを満たす。
* 多パラメータモニタリング: 波長分割多重スキームにより、単一ファイバー上でpHと温度を同時にモニタリングし、光熱療法を行うことができる。これは、複雑な生物環境における包括的な多パラメータ評価の要件を直接満たす。
* 全身毒性の低減と深部組織へのアクセス: 光ファイバー表面にセラノスティクス剤を固定化することにより、アプローチは「局所的封じ込めによるオフターゲット毒性を効果的に軽減する。」さらに、光ファイバーは「最小限の損失での終端から終端までの光伝送」を促進し、「深部腫瘍」のセンシングと治療を可能にし、従来の光セラノスティクス剤の限定的な光浸透深度を克服する。
代替案の却下
本稿は、閉ループ多機能腫瘍セラノスティクスの特定の問題に対する根本的な限界に基づいて、いくつかの代替アプローチを暗黙的かつ明示的に却下している。
* ファイバーあたりの単一機能実装: これらは、多パラメータモニタリングと治療のために複数のファイバーを必要とし、「拡大切開、繰り返しの侵襲的処置」およびデバイス剛性の増加につながるため、不十分と見なされた。目標は断片化された機能ではなく、統合セラノスティクスであった。
* マルチファイバー構成: 多重化を提供するものの、これらは「デバイスの剛性と寸法の増加」といった固有の物理的限界のために却下され、低侵襲処置との互換性を損ない、組織損傷のリスクを高めた。
* 機能間クロストークに悩まされるアプローチ: 機能性試薬が「吸収または発光帯のスペクトル重複」を持つ方法は、問題があると明示的に特定された。著者による重複しない帯域を持つ試薬の慎重な選択とWDM戦略は、この失敗点を直接解決し、信号整合性を保証する。
* ナノマテリアル依存戦略(ファイバー統合なし): 結論は、「ナノマテリアル依存戦略」と比較して、この光ファイバーアプローチは「光浸透深度と全身毒性の限界を効果的に対処する」と強調している。これは、浮遊またはファイバー統合されていないナノマテリアルのみに依存すると、効果的な腫瘍光熱療法に必要な深部組織アクセスと局所的で無毒な送達を提供できないことを示唆している。
数学的・論理的メカニズム
マスター方程式
このセラノスティックプローブのセンシング能力の中核には、ボルツマンシグモイドモデルがあり、これはpHや温度のような意味のある生理学的パラメータに比率蛍光信号を変換するための基本的な変換ロジックとして機能する。光熱療法コンポーネントは直接的な光から熱への変換を含むが、その正確な制御とモニタリングは、これらのセンシングメカニズムによって提供される正確な読み取りに完全に依存している。
本稿でpHと温度センシングの両方に採用されているボルツマン方程式の一般的な形式は、次のように表すことができる:
$$ y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}} $$
ここで:
* pHセンシングの場合(図2fより導出):
$$
R_{pH} = 0.97 - \frac{0.78}{1 + e^{(pH - 7.07)/0.87}}
$$
ここで、$y$ は蛍光強度比 $R_{pH} = I_{520}(450nm) / I_{520}(405nm)$ であり、$x$ はpH値である。
- 温度センシングの場合(図3gより導出):
$$ R_{Temp} = 1.55 - \frac{0.81}{1 + e^{(Temp - 65.74)/10.71}} $$
ここで、$y$ は蛍光強度比 $R_{Temp} = I_{618} / I_{546}$ であり、$x$ は摂氏温度である。
これらの式は、プローブが受け取る光学信号を定量的に解釈することを可能にする中核となる数学的エンジンであり、閉ループセラノスティクスのための重要なフィードバックを提供する。
用語ごとの解剖
一般的なボルツマン方程式 $y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}}$ を分解して、各コンポーネントの役割を理解しよう:
-
$y$ (蛍光強度比、$R_{pH}$ または $R_{Temp}$)
- 数学的定義: これは従属変数であり、無次元の蛍光強度比を表す。pHセンシングの場合、それは450 nmで励起されたときの520 nmでの発光強度と405 nmで励起されたときのそれとの比率 ($I_{520}(450nm) / I_{520}(405nm)$) である。温度センシングの場合、それは295 nm励起下での618 nmと546 nmの発光強度との比率 ($I_{618} / I_{546}$) である。
- 物理的/論理的役割: この項は、光学測定システムの直接的な出力である。比率を使用することにより、著者らは光退色、指示薬濃度の変動、およびファイバー形態の変化といった一般的な誤差源を巧妙に軽減している。この正規化により、信号は堅牢で信頼性の高いものとなり、ターゲットパラメータとともに予測可能に変化する主要な観測値として機能する。
- なぜ比率/減算/除算なのか: 比率は、自己参照し、共通モードノイズをキャンセルするための比率センシングにおける標準的な技術である。シグモイド形状全体(減算と除算を含む)は、連続変数に応答して指示薬が二つの状態(例:プロトン化/脱プロトン化、または異なるエネルギー移動状態)間で遷移する化学的または物理的プロセスから自然に生じ、両極端で飽和を示す。
-
$x$ (生理学的パラメータ、$pH$ または $Temp$)
- 数学的定義: これは独立変数であり、測定されている環境条件(pHまたは温度(℃))を表す。
- 物理的/論理的役割: これはシステムが検出しモニタリングするように設計されている実際の物理量である。これは、システムが決定しようとしている「真の値」である。
- なぜ独立変数なのか: それは原因であり、$y$ は結果である。キャリブレーションプロセスは、この入力と測定された出力比率との間の機能的関係を確立する。
-
$C_1$ (上限漸近線)
- 数学的定義: $x$ が正の無限大に近づくにつれて(この特定の減少シグモイド形式において)、シグモイド曲線の上のプラトーを表す定数係数。
- 物理的/論理的役割: pHの場合、$C_1 = 0.97$ は、HPTS-IP指示薬が主にそのプロトン化状態の一つ(例:高pHで完全に脱プロトン化)にあるときの最大蛍光比を表す。温度の場合、$C_1 = 1.55$ は、高温度でのLnMOFの最大比率を表す。これはセンサーのダイナミックレンジの一方の極限を定義し、$x$ のさらなる増加が指示薬の状態をそれ以上有意に変化させない飽和点を示す。
- なぜ定数なのか: これは指示薬とその環境との相互作用の特性であり、平衡がほぼ一方の側に完全にシフトした極端な条件下での最大可能な応答を反映している。
-
$C_2$ (範囲スケーリング係数)
- 数学的定義: シグモイド遷移の大きさのスケールを決定する定数係数。これは、下限漸近線から上限漸近線までの $y$ の全変化量を示す。
- 物理的/論理的役割: pHの場合、$C_2 = 0.78$ は、pHが感応範囲にわたって変化するにつれて蛍光比の変化の全体的な範囲を決定する。温度の場合、$C_2 = 0.81$ は、温度についても同様である。この項は、センサーの応答の「高さ」を定義し、センサーの応答の全ダイナミックレンジを示す。
- なぜ定数なのか: これは指示薬と環境との相互作用の固有の特性であり、比率信号の最大可能な変化を反映している。
-
$C_3$ (中間点または遷移の中心)
- 数学的定義: 応答が漸近限界の中間にある(または傾きが最大である)ときの $x$ 値を表す定数係数。
- 物理的/論理的役割: pHの場合、$C_3 = 7.07$ は、HPTS-IP指示薬が最も変化に敏感なpH値を示し、しばしばそのpKaに対応する。温度の場合、$C_3 = 65.74$ °C は、LnMOFのエネルギー移動メカニズムが最も急激な変化を示す温度を示す。このパラメータは、センサーの動作範囲と最適な感度を定義する上で重要である。
- なぜ定数なのか: これは、指示薬によって監視されている化学的または物理的プロセスの固有の特性である。
-
$C_4$ (傾きパラメータ)
- 数学的定義: シグモイド曲線の最大傾きに反比例する定数係数。$C_4$ の絶対値が小さいほど、曲線は急になる。
- 物理的/論理的役割: pHの場合、$C_4 = 0.87$ は、pH応答曲線の急峻さを定量化する。温度の場合、$C_4 = 10.71$ は、温度についても同様である。このパラメータは、センサーの感度に直接関係している:$C_4$ が小さいほど、$C_3$ 周辺の $x$ の変化に対する蛍光比のより急速な変化を意味する。
- なぜ定数なのか: これは、指示薬の遷移の固有の応答性と協同性を反映している。
-
$e$ (ネイピア数)
- 数学的定義: 自然対数の底である数学定数で、約2.71828。
- 物理的/論理的役割: 指数関数に不可欠であり、ここではシグモイド遷移をモデル化するために使用される。このような遷移は、しばしば統計力学または化学平衡方程式(pHのヘンダーソン・ハッセルバルヒ方程式や、エネルギー状態のボルツマン分布など)から生じる。そこでは、状態の確率は駆動力の指数関数的に変化する。
- なぜ指数関数なのか: 指数項は、多くの物理的および化学的システムが平衡に近づくにつれて観察される非線形で飽和する挙動を自然に記述する。
-
指数 $(x - C_3)/C_4$
- 数学的定義: 指数関数の引数。
- 物理的/論理的役割: この項は、現在の入力 $x$ と中間点 $C_3$ との差を傾きパラメータ $C_4$ で正規化する。これは、システムが半遷移点からどれだけ離れているかを決定する、入力のスケールを指数関数的減衰または成長に適合させる。
-
$(1 + e^{(x - C_3)/C_4})$ による除算
- 数学的定義: この特定の形式は、シグモイド形状の核心であり、しばしばロジスティック関数またはフェルミ・ディラック分布と呼ばれる。
- 物理的/論理的役割: この項は、$x$ が変化するにつれて出力 $y$ が漸近線の間をスムーズに遷移することを保証する。これは、指示薬の状態が一方の極端から他方への状態が徐々にシフトするのをモデル化する。
-
減算 $C_1 - \frac{C_2}{...}$
- 数学的定義: この操作は、上限漸近線とスケール化されたシグモイド項を組み合わせる。
- 物理的/論理的役割: 本稿で使用されている特定の形式では、この減算は、$C_2$ が正の場合、減少シグモイドを作成する。これは、$x$ が増加するにつれて比率 $y$ が $C_1 - C_2$ に向かって高く始まり減少することを意味する。しかし、グラフ(図2fおよび3g)はpH/温度の増加に伴う増加比率を示している。これは、著者らの適合方程式 $y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}}$ が、実際には $C_1$ が上限漸近線であり、$C_1 - C_2$ が下限漸近線である増加シグモイドであることを示唆している。$x \to -\infty$ のとき、$e^{(x - C_3)/C_4} \to 0$ なので、$y \to C_1 - C_2$。$x \to +\infty$ のとき、$e^{(x - C_3)/C_4} \to \infty$ なので、$y \to C_1$。これは図と一致する。減算は、曲線の向きと範囲を定義する上で不可欠である。
ステップバイステップの流れ
セラノスティックプローブを、データ処理のための洗練されたミニチュア組立ラインとして想像してください。各ステップで、生の光学信号が実行可能な生理学的洞察に変換されます。
-
光入力と波長選択: プロセスは、チューニング可能な光源からの光がY字型光ファイバーに入ることから始まります。測定したいものに応じて、ツールボックスからツールを選ぶように、特定の波長が選択されます。pHセンシングの場合、システムは405 nmと450 nmの励起光の間を迅速に切り替えます。温度センシングの場合、295 nmの励起波長が使用されます。この波長分割多重(WDM)は、プローブの機能を決定する最初の「スイッチ」です。
-
エバネッセント場相互作用: 選択された光はファイバーを伝わり、そのテーパーチップに到達し、そこでエバネッセント場として周囲のハイドロゲルマトリックスに漏れ出します。この場は、共固定化された指示薬分子(pH用HPTS-IP、温度用LnMOF)と直接相互作用する微視的なネットとして機能します。指示薬はこれらの光を吸収し、エネルギーを得ます。
-
蛍光発光: 励起されると、エネルギーを得た指示薬分子は蛍光を発します。この発光の特性は、局所環境に敏感です。pHの場合、HPTS-IPは520 nmで蛍光を発しますが、405 nmまたは450 nmで励起されたかどうかに応じて、この波長での強度が変化し、局所的なプロトン化状態を反映します。温度の場合、LnMOFは2つの異なる波長、546 nmと618 nmで蛍光を発し、それらの相対強度はエネルギー移動ダイナミクスによる局所温度に応じて変化します。
-
信号収集: 発光された蛍光は、光ファイバーに効率的に収集され、組織から離れるように導かれます。
-
スペクトル分析: 収集された光は蛍光スペクトルアナライザー(FSA)に送られます。このデバイスは「光選別機」として機能し、関連する発光波長での蛍光の正確な強度を測定します。pHの場合、$I_{520}(450nm)$ と $I_{520}(405nm)$ を測定します。温度の場合、$I_{618}$ と $I_{546}$ を測定します。
-
比率計算: 計算ユニットが、これらの生の強度測定値から無次元の比率を計算します。pHの場合、$R_{pH} = I_{520}(450nm) / I_{520}(405nm)$ を計算します。温度の場合、$R_{Temp} = I_{618} / I_{546}$ を計算します。この比率は、数学的エンジンに入力される標準化された「データポイント」です。
-
ボルツマンモデル変換: 計算された比率($R_{pH}$ または $R_{Temp}$)は、事前にキャリブレーションされたボルツマン方程式に入力されます。「デコーダー」として機能する方程式は、非線形変換を実行し、実質的にキャリブレーション曲線を反転させて、実際の生理学的パラメータを導き出します。例えば、$R_{pH}$ がpHボルツマン方程式に入力されると、対応するpH値が出力されます。同様に、$R_{Temp}$ は温度を導き出します。
-
リアルタイムフィードバックとアクション: 導出されたpHと温度の値はリアルタイムで表示されます。これらの正確な読み取りは、重要なフィードバックとして機能します。光熱療法(PTT)中、温度読み取りは「熱線量制御」を可能にし、オペレーターがポンプレーザーの出力を調整して目標温度(例:ファイバーチップで65℃、腫瘍辺縁で45℃を確保)を維持できるようにします。治療後、pHモニタリングは、酸性腫瘍微小環境の逆転を追跡することによって有効性を評価します。この閉ループシステムは、患者のリアルタイム生理学的状態に基づいた治療が、単に提供されるだけでなく、継続的に最適化されることを保証します。
最適化ダイナミクス
このセラノスティックプローブの「最適化ダイナミクス」は、主にその初期キャリブレーションと、堅牢なリアルタイムフィードバック制御のための固有の設計にあり、機械学習における継続的な反復学習という意味ではありません。
-
初期「学習」としてのキャリブレーション:
- データ取得: 臨床応用前に、プローブは厳格なキャリブレーションプロセスを受けます。これには、制御された実験室環境で、プローブを既知のpH値(例:pH 4.0~9.0)および温度(例:30℃~100℃)の範囲に曝露することが含まれます。各既知のポイントで、対応する比率蛍光信号が測定されます。
- モデルフィッティング: これらの収集されたデータポイント(既知パラメータ $x$ 対測定比率 $y$)は、ボルツマンシグモイドモデルを「トレーニング」または「フィッティング」するために使用されます。このフィッティングプロセスは非線形回帰の一種であり、ボルツマン方程式の係数($C_1, C_2, C_3, C_4$)は、モデルが予測する比率と、各既知入力に対して実験的に観測された比率との差(例:二乗誤差の合計)を最小化するように、反復的に調整されます。これは、応答曲線を最もよく記述する最適な係数セットを見つけるために「損失ランドスケープ」をナビゲートすることに似ています。本稿では高い$R^2$値(pHで0.997、温度で0.997)を報告しており、これは優れたフィットを示しており、明確な最小値を持つ明確に定義された損失ランドスケープを示しています。
- パラメータ固定: これらの係数が決定されると、それらは固定されます。センサーは、動作中にこれらのパラメータを「学習」または更新しません。この一度限りのキャリブレーションにより、センサーの「知識」ベースが確立されます。
-
堅牢性のための比率設計(暗黙的最適化):
- 比率センシングの選択は、重要な設計「最適化」です。二つの蛍光強度(pHの場合は異なる励起波長、温度の場合は異なる発光波長)の比率を取ることにより、システムは本質的に多くの共通ノイズ源をキャンセルします。これには、励起光強度の変動、指示薬の光退色、指示薬濃度の変動、およびファイバーの光学特性や結合効率のわずかな変化も含まれます。
- このメカニズムにより、信号対雑音比(SNR)が高く保たれ、センサーの出力が安定して信頼性の高いものとなり、明示的なアルゴリズム更新なしに測定品質をリアルタイムで効果的に「最適化」します。安定性試験(図2g,h,i,jおよび図3j,k,l,n)は、標準偏差の最小化と浸出を示しており、この堅牢性を確認しています。
-
治療のための閉ループフィードバックによる最適化:
- 実際の光熱療法中、システムは閉ループ制御メカニズムとして機能します。センサーは継続的にリアルタイムの温度とpHの読み取りを提供します。
- これらの読み取りは、センサーの内部数学モデルを更新するために使用されるのではなく、外部治療入力を調整するために使用されます。例えば、監視温度が目標熱線量から逸脱した場合、ポンプレーザー出力(治療入力)がそれに応じて調整されます。これは古典的なフィードバックループです:感知(温度/pH)→評価(目標値との比較)→行動(レーザー出力調整)。
- リアルタイムセンサーデータに基づいた治療入力のこの反復調整は、治療自体が望ましい結果(例:腫瘍辺縁で45℃を確保するためにファイバーチップで65℃の腫瘍温度を維持する)を達成するために最適化される方法であり、副作用を最小限に抑えながら行われます。システムは、継続的なモニタリングと調整を通じて、目標治療状態に収束し、治療を正確かつ適応的にします。
本質的に、数学的エンジンはキャリブレーション中に一度その特性応答を「学習」し、その後その学習された関数を信頼性高く適用します。治療中のシステム全体の「最適化」は、センサーの正確で安定した測定を利用して治療介入を制御する、堅牢なリアルタイムフィードバックループを通じて達成されます。
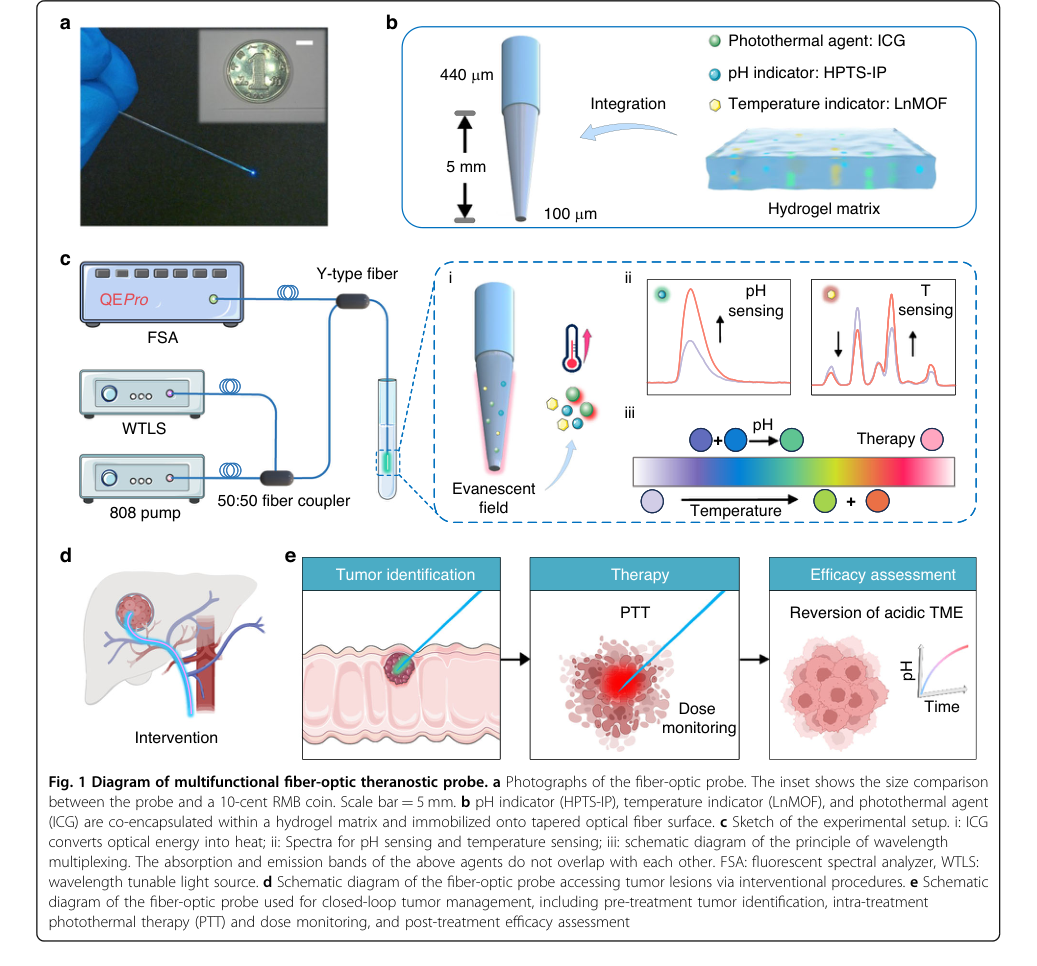 Figure 1. Diagram of multifunctional fiber-optic theranostic probe. a Photographs of the fiber-optic probe. The inset shows the size comparison between the probe and a 10-cent RMB coin. Scale bar = 5 mm. b pH indicator (HPTS-IP), temperature indicator (LnMOF), and photothermal agent (ICG) are co-encapsulated within a hydrogel matrix and immobilized onto tapered optical fiber surface. c Sketch of the experimental setup. i: ICG converts optical energy into heat; ii: Spectra for pH sensing and temperature sensing; iii: schematic diagram of the principle of wavelength multiplexing. The absorption and emission bands of the above agents do not overlap with each other. FSA: fluorescent spectral analyzer, WTLS: wavelength tunable light source. d Schematic diagram of the fiber-optic probe accessing tumor lesions via interventional procedures. e Schematic diagram of the fiber-optic probe used for closed-loop tumor management, including pre-treatment tumor identification, intra-treatment photothermal therapy (PTT) and dose monitoring, and post-treatment efficacy assessment
Figure 1. Diagram of multifunctional fiber-optic theranostic probe. a Photographs of the fiber-optic probe. The inset shows the size comparison between the probe and a 10-cent RMB coin. Scale bar = 5 mm. b pH indicator (HPTS-IP), temperature indicator (LnMOF), and photothermal agent (ICG) are co-encapsulated within a hydrogel matrix and immobilized onto tapered optical fiber surface. c Sketch of the experimental setup. i: ICG converts optical energy into heat; ii: Spectra for pH sensing and temperature sensing; iii: schematic diagram of the principle of wavelength multiplexing. The absorption and emission bands of the above agents do not overlap with each other. FSA: fluorescent spectral analyzer, WTLS: wavelength tunable light source. d Schematic diagram of the fiber-optic probe accessing tumor lesions via interventional procedures. e Schematic diagram of the fiber-optic probe used for closed-loop tumor management, including pre-treatment tumor identification, intra-treatment photothermal therapy (PTT) and dose monitoring, and post-treatment efficacy assessment
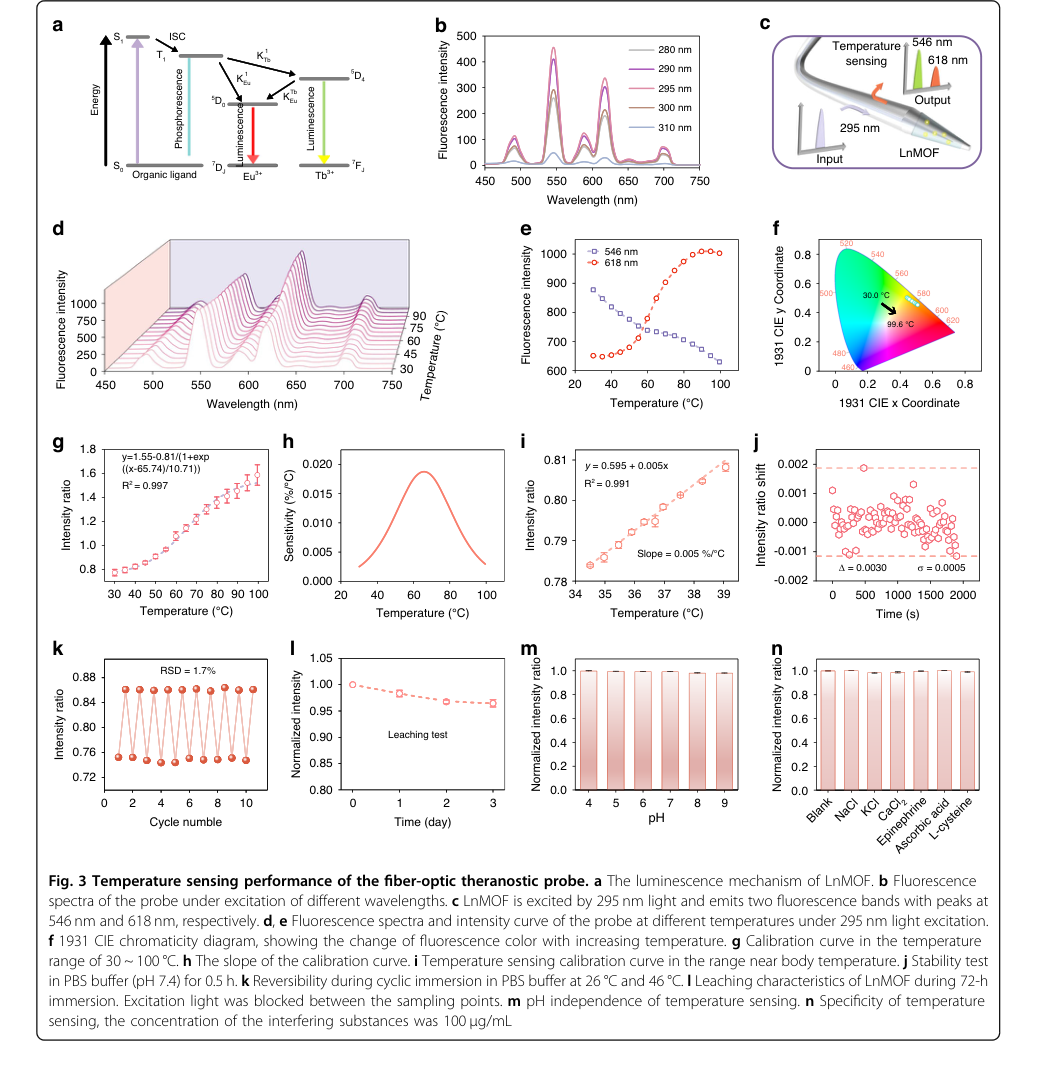 Figure 3. Temperature sensing performance of the fiber-optic theranostic probe. a The luminescence mechanism of LnMOF. b Fluorescence spectra of the probe under excitation of different wavelengths. c LnMOF is excited by 295 nm light and emits two fluorescence bands with peaks at 546 nm and 618 nm, respectively. d, e Fluorescence spectra and intensity curve of the probe at different temperatures under 295 nm light excitation. f 1931 CIE chromaticity diagram, showing the change of fluorescence color with increasing temperature. g Calibration curve in the temperature range of 30 ~ 100 °C. h The slope of the calibration curve. i Temperature sensing calibration curve in the range near body temperature. j Stability test in PBS buffer (pH 7.4) for 0.5 h. k Reversibility during cyclic immersion in PBS buffer at 26 °C and 46 °C. l Leaching characteristics of LnMOF during 72-h immersion. Excitation light was blocked between the sampling points. m pH independence of temperature sensing. n Specificity of temperature sensing, the concentration of the interfering substances was 100 μg/mL
Figure 3. Temperature sensing performance of the fiber-optic theranostic probe. a The luminescence mechanism of LnMOF. b Fluorescence spectra of the probe under excitation of different wavelengths. c LnMOF is excited by 295 nm light and emits two fluorescence bands with peaks at 546 nm and 618 nm, respectively. d, e Fluorescence spectra and intensity curve of the probe at different temperatures under 295 nm light excitation. f 1931 CIE chromaticity diagram, showing the change of fluorescence color with increasing temperature. g Calibration curve in the temperature range of 30 ~ 100 °C. h The slope of the calibration curve. i Temperature sensing calibration curve in the range near body temperature. j Stability test in PBS buffer (pH 7.4) for 0.5 h. k Reversibility during cyclic immersion in PBS buffer at 26 °C and 46 °C. l Leaching characteristics of LnMOF during 72-h immersion. Excitation light was blocked between the sampling points. m pH independence of temperature sensing. n Specificity of temperature sensing, the concentration of the interfering substances was 100 μg/mL
結果、限界、および結論
実験デザインとベースライン
研究者たちは、革新的な光ファイバーセラノスティックプローブの多機能能力と治療効果を厳密に検証するために、実験を細心の注意を払って設計した。彼らの実験アーキテクチャの中核は、単一光ファイバーを使用して、pHセンシング、温度センシング、および光熱療法(PTT)という3つの異なる機能を実行するプローブの能力を実証することを中心に展開された。波長分割多重(WDM)を活用してクロストークを防いだ。
pHセンシングについて、HPTS-IPで機能化されたプローブは、室温で広範囲のpH(4.0~9.0)のリン酸緩衝生理食塩水(PBS)溶液でテストされた。その安定性は、pH 7.4 PBS中での150秒間の連続スペクトル記録によって評価された。pH 4.0と9.0のバッファーへの交互浸漬を5サイクル繰り返すことで、可逆性が証明された。浸出特性は、pH 7.4 PBS中での72時間で評価された。複雑な生物環境での信頼性を確認するために、プローブの特異性は、NaCl、KCl、CaCl₂、エピネフリン、アスコルビン酸、L-システインといった一般的な干渉物質に対してテストされた。特に、pHを変化させながら温度を26~41℃に変化させた際の温度クロストークが評価された。
温度センシングはLnMOFを使用し、広範囲(30~100℃)、特に生理学的に関連性の高い範囲(34.5~39℃)で評価された。安定性はpH 7.4 PBS中での0.5時間テストされ、可逆性は26℃と46℃のPBSへの交互浸漬による10サイクルで実証された。浸出は72時間モニタリングされ、pH 4.0~9.0のバッファーでのテストによりpH非依存性が確認された。干渉物質に対する特異性も評価された。
光熱変換について、ICG機能化プローブは、808 nmポンプレーザーを使用したin vitroテストにかけられ、様々なポンプ出力(最大267 mW)での最大温度を測定した。光熱安定性は5回の加熱/冷却サイクルで評価され、ICG浸出は72時間モニタリングされた。ここでの「犠牲者」は、従来のナノマテリアルベースのPTTシステムで一般的に必要とされる高ポンプ出力(しばしば1 Wを超える)であった。
最終的な検証は、BALB/cヌードマウスの皮下大腸がん異種移植モデルを使用した_in vivo_実験によってもたらされた。介入前に腫瘍は約100 mm³に達するようにした。
* 腫瘍同定は、プローブを腫瘍組織、隣接する正常組織、腫瘍表面、および正常組織に挿入し、測定されたpH値を比較することによって厳密にテストされた。
* PTTと線量モニタリングは、プローブを腫瘍中心に挿入し、ファイバー温度を65℃に15分間維持し、熱画像で腫瘍辺縁が有効な治療温度45℃に達することを確認した。
* 有効性評価は多角的であった:治療後30分および24時間での腫瘍微小環境(TME)におけるリアルタイムpHモニタリング、および20日間隔で3日ごとの腫瘍体積と体重の長期モニタリング。ここでの「犠牲者」は、未治療の対照群マウスであり、その腫瘍は進行性の成長を示し、体積が2000 mm³を超えると安楽死に至った。
* 生体適合性は、HCT116細胞をプローブ浸出液(24時間)で培養し、CCK-8アッセイとライブデッド染色を実施したin vitroテストによって評価された。in vivoでは、治療後24時間での臓器生体適合性(心臓、肝臓、脾臓、肺、腎臓)は、移植群(ファイバーのみ)と治療群の両方で、対照群と比較してH&E染色によって評価された。腫瘍組織の組織学的および免疫組織化学的分析(カスパーゼ-3、HIF-1α、Ki67)は、治療後24時間で実施され、シャム治療群(レーザー励起なしのファイバー移植)を比較のベースラインとして使用した。
証拠が証明すること
本稿で提示された証拠は、リアルタイムフィードバックを伴う閉ループ腫瘍光熱療法を実行できる多機能光ファイバーセラノスティックプローブの、革新的な開発と機能性を決定的に証明している。
非重複励起帯域のための波長分割多重(WDM)という中核となる数学的主張は、HPTS-IP(405 nm、450 nm)、LnMOF(295 nm)、およびICG(790 nm)の異なる吸収スペクトルによって、徹底的に証明された(図2bおよび図S7)。このスペクトル分離は、機能間クロストークを排除する、つまり以前のマルチエージェントシステムにおける重大な限界を排除する、オンデマンドで機能を切り替えるための基本メカニズムが機能したという否定できない証拠である。
pHセンシングについて、プローブは優れた性能を示した:
* 6.0~8.0の線形範囲内で0.013 pH単位という高い分解能を達成し、これは正常組織と腫瘍組織の生理学的pH値を区別するために重要である。これはボルツマンモデルフィット(図2f)と、標準偏差($\sigma$)が0.0009(図2g)を示す安定性試験から導出された。
* 5サイクルにわたる相対標準偏差(RSD)0.8%(図2h)で優れた可逆性が確認され、一貫した性能を示した。
* HPTS-IPの最小限の浸出(72時間で蛍光強度の1.6%低下、図2i)と様々な干渉物質に対する優れた選択性(図2j)は、複雑な生物環境での信頼性をさらに検証した。
* 決定的に、pH 4.0~7.0の範囲で無視できる温度クロストークが観察され、pH > 7.0では、プローブの統合温度モニタリング機能が組み込み補償を提供し、正確なpHセンシングを保証した(図2k)。
温度センシングもまた、堅牢な性能を示した:
* Tb³⁺からEu³⁺への熱増強エネルギー移動(図3a, c)を活用した比率アプローチにより、正確なモニタリングが可能になった。
* 0.3℃の分解能が達成され、in vivoモニタリング要件を満たし、生理学的に関連性の高い範囲(34.5~39℃)で線形関係が観察された(図3i)。
* 高い可逆性(10サイクルでRSD 1.7%、図3k)と最小限のLnMOF浸出(72時間で3.5%低下、図3l)が実証された。
* 証拠はまた、そのpH非依存性(図3m)と優れた特異性(図3n)を証明し、pH変動や他の生物学的干渉物質に関係なく正確な温度読み取りを保証した。
プローブの光熱変換能力は決定的に確立された:
* わずか267 mWの励起下で、プローブはin vitroで102.9℃まで加熱された(図4b, c)。これは効率的な光熱変換を確認するものである。これは、通常1 Wを超えるポンプ出力を必要とする従来のナノマテリアルベースのシステムよりも大幅な進歩であり、このアプローチはより費用対効果が高く、潜在的な副作用を低減する。
* 5回の加熱/冷却サイクルにわたる安定した温度上昇により、優れた光熱安定性が示され(図4d)、ICG浸出は最小限(72時間で5.9%低下、図4g, h)であり、長期的な性能を保証した。
* in vivo実験では、ポンプ出力の増加に伴う腫瘍領域での温度上昇が確認された(図4e, f)。
_in vivo_検証は、プローブの実際の有用性に対する最も説得力のある証拠を提供した:
* 腫瘍辺縁同定は、健康組織と腫瘍組織の間(p < 0.0001)、および腫瘍表面と正常組織の間(p < 0.01)で測定されたpH値の統計的に有意な差によって、紛れもなく証明された(図5a, b)。これは、その診断能力の決定的な証拠である。
* PTT中の正確な熱線量制御は、ファイバー温度を65℃に維持することによって実証され、腫瘍辺縁が有効な治療温度45℃に達することを保証した(図5c)。
* 迅速な有効性評価は、治療後のTMEにおけるpHの有意な上昇(30分以内に0.12~0.22単位増加、24時間でp < 0.01)によって検証され、治療応答の信頼できるバイオマーカーとして機能した(図5d, e, f)。
* 抗腫瘍効果の究極の証明は、腫瘍体積モニタリングから得られた:治療されたマウスの4頭中3頭が完全な腫瘍退縮を示し、残りのマウスでは有意な成長抑制が見られた一方、対照群は進行性の腫瘍成長を示した(図5g, h, i, j)。
* 優れた生体適合性と生物学的安全性は、すべてマウスの体重安定性(図5k)、H&E染色された臓器における有意なアポトーシス/壊死領域または炎症細胞浸潤の欠如(図S10)、およびin vitro浸出試験での高い細胞生存率(図S9、図6c)によって確認された。
* 最後に、多面的な抗腫瘍効果は、組織学的分析(図6a)によって裏付けられ、治療された腫瘍における多巣性壊死および出血領域が明らかになった。免疫組織化学は、カスパーゼ-3(アポトーシスバイオマーカー)のアップレギュレーション、Ki67(増殖バイオマーカー)のダウンレギュレーション、およびHIF-1αのダウンレギュレーションを示し、MRI(図6b、図S8)によってさらに裏付けられた腫瘍低酸素症の改善を示唆した。この包括的な証拠は、プローブの中核メカニズムが実際に現実世界で機能し、効果的な腫瘍アブレーションとTMEリモデリングにつながったことを否定できないほど証明している。
限界と将来の方向性
提示された光ファイバーセラノスティックプローブは顕著な能力を示しているが、いくつかの限界を認識し、将来の開発の方向性を考慮することが重要である。
光ファイバー設計によって軽減されているものの、固有の限界の一つは光浸透深度である。エバネッセント場は局所的なセンシングを可能にするが、浅い浸透深度(図S5)を持つため、プローブは主にその表面の近傍をセンシングおよび治療する。これは正確な局所的介入に適しているが、TMEのより広範な体積マッピングには、複数のプローブまたはより高度な光学戦略が必要になる可能性がある。pHセンシング(減少時最大12.8秒)および温度センシング(増加時最大2.0秒)の応答時間は、多くのアプリケーションには良好であるが、極めて急速なミリ秒スケールの生理学的ダイナミクスを捉えるには限界となる可能性がある。
もう一つの実用的な考慮事項は浸出である。本稿ではHPTS-IP(1.6%)、LnMOF(3.5%)、ICG(5.9%)の72時間での最小限の浸出を報告しているが、ゼロではない。長期埋め込み型デバイスの場合、最小限の慢性浸出でさえ、数週間または数ヶ月で蓄積したり、免疫応答を引き起こしたりする可能性があり、プローブ性能と患者安全性の両方に影響を与える可能性がある。光退色を最小限に抑えるためにサンプリングポイント間の励起光を遮断することへの言及(図2i、3lキャプション)は、比率検出が役立つ一方で、光退色は長時間の連続モニタリングに影響を与える可能性のある要因であり続けることを示唆している。さらに、単一コーティング層の選択は、SNRと応答時間の両方を最適化する一方で、トレードオフを意味する。厚い膜は信号を強化できるが、応答速度の犠牲を伴う。pHセンシングにおける温度クロストークはpH > 7.0では補償されたが、pH範囲全体で完全に無視できるわけではなく、将来的にさらに洗練された補償アルゴリズムが必要となる可能性のある微妙な相互作用を示唆している。
将来を見据えると、本稿自体がいくつかのエキサイティングな方向性を提案している。統合戦略は、機械的コンプライアンスと生体適合性を向上させるために、柔軟なポリマーおよびハイドロゲル光ファイバーに翻訳でき、長期埋め込み型デバイスへの道を開く。スペクトルリソースを活用し、多ピークフィッティングアルゴリズムを採用することで、より多くの機能が統合されるにつれて、発光帯域の重複の可能性に対処し、機能容量をさらに強化できる。著者らはまた、腫瘍辺縁のより正確な温度モニタリングのために、MRI温度測定との統合を提案しており、これは現在の熱画像処理がこれなしでは空間分解能または深度に限界がある可能性を示唆している。
本稿の明示的な提案を超えて、さらなる開発と進化のためのいくつかの議論トピックが浮上する:
-
高度な多パラメータ統合とAI駆動フィードバック: WDMまたは他の多重化技術を使用して、信号整合性を損なうことなく、またはデバイスの複雑性を増加させることなく、単一ファイバーにさらに多くのTMEパラメータ(例:酸素飽和度、グルコースレベル、特定の酵素活性、薬物濃度)を同時に統合できるか?そのようなプローブからのリアルタイムデータは、人工知能(AI)または機械学習(ML)モデルにフィードされ、進化するTMEに基づいてレーザー出力、期間、または薬物送達さえも動的に調整する、真にアダプティブでパーソナライズされた治療プロトコルを作成できるか?これは単純なフィードバックループを超えて、予測的で最適化された治療へと移行する可能性がある。
-
長期的な生体安定性と免疫調節: 短期的な生体適合性は証明されているが、数ヶ月または数年にわたる慢性的な埋め込みの長期的な影響はどうなるか?生体付着、宿主組織による被包化、または慢性炎症反応は、プローブのセンシング精度と治療効果にどのように影響するか?ゾルゲルマトリックスは、抗炎症薬または成長因子を放出することにより、積極的に統合を促進し、有害反応を最小限に抑えるために、免疫調節特性を持つようにさらに設計できるか?
-
スケーラビリティ、小型化、および臨床ワークフロー統合: 現在のプローブは直径440 µm、チップ径100 µmである。これをさらに小型化して、より低侵襲な処置を可能にできるか、またはより大きなまたは多焦点腫瘍のためにそのようなプローブのアレイを開発できるか?広範な臨床使用のために生産をスケールアップするための製造上の課題とコストは何か?そのような洗練されたデバイスは、専門的なトレーニング、機器、およびデータ解釈の必要性を考慮して、既存の臨床ワークフローにどのように統合されるか?
-
非侵襲的ガイダンスと補完的療法: この閉ループセラノスティックシステムの原理を、非侵襲的療法のガイダンスまたは強化に適合させることができるか?例えば、プローブのより低侵襲なバージョンは、単にPTTを実行するのではなく、外部放射線療法、集束超音波、または全身化学療法の最適化のためにリアルタイムTMEフィードバックを提供できるか?これはその適用範囲を直接腫瘍アブレーションを超えて広げるだろう。
-
倫理的考慮事項と患者体験: これらのデバイスがより洗練され、埋め込み可能になるにつれて、データプライバシー、患者の自律性、および継続的で適応的な治療からの過剰治療または意図しない副作用の可能性に関する倫理的考慮事項は何であるか?埋め込み型デバイスと頻繁なモニタリングに関連する不快感と心理的負担を最小限に抑えながら、患者体験を最適化するにはどうすればよいか?
これらの議論は、この技術の広大な可能性を強調すると同時に、その完全な実現と腫瘍学における広範な影響のために対処されなければならない複雑で学際的な課題を浮き彫りにしている。
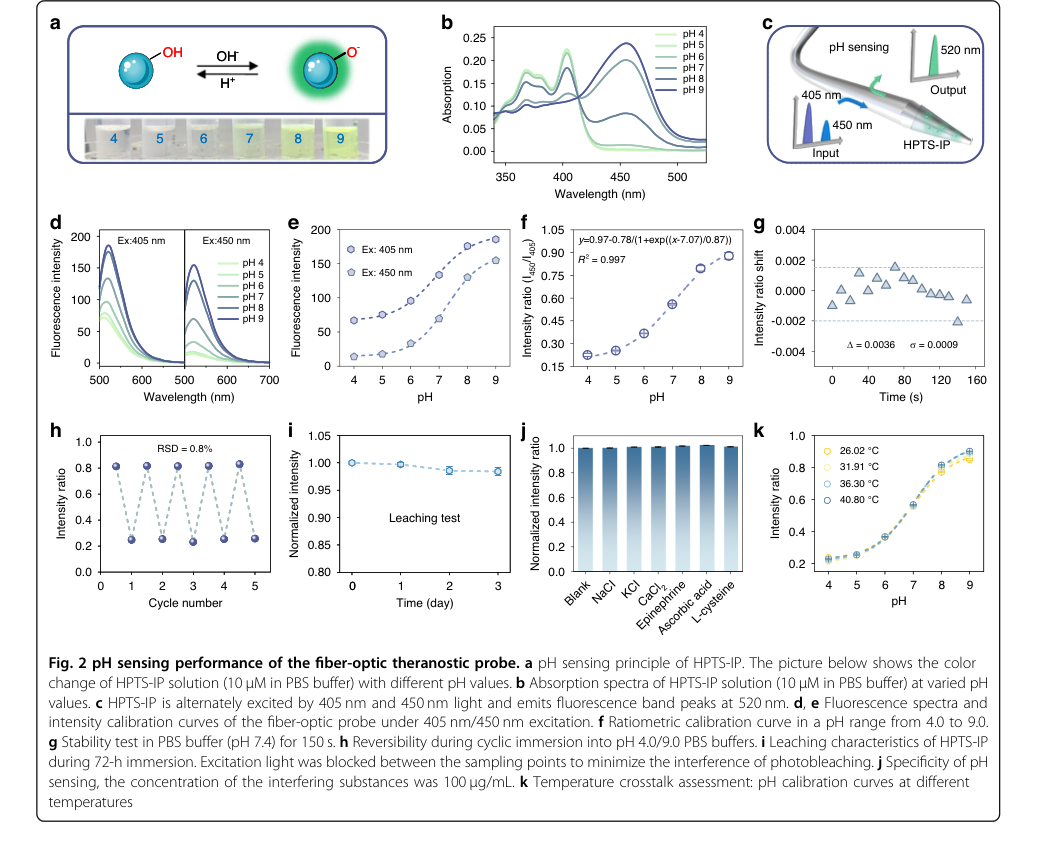 Figure 2. pH sensing performance of the fiber-optic theranostic probe. a pH sensing principle of HPTS-IP. The picture below shows the color change of HPTS-IP solution (10 μM in PBS buffer) with different pH values. b Absorption spectra of HPTS-IP solution (10 μM in PBS buffer) at varied pH values. c HPTS-IP is alternately excited by 405 nm and 450 nm light and emits fluorescence band peaks at 520 nm. d, e Fluorescence spectra and intensity calibration curves of the fiber-optic probe under 405 nm/450 nm excitation. f Ratiometric calibration curve in a pH range from 4.0 to 9.0. g Stability test in PBS buffer (pH 7.4) for 150 s. h Reversibility during cyclic immersion into pH 4.0/9.0 PBS buffers. i Leaching characteristics of HPTS-IP during 72-h immersion. Excitation light was blocked between the sampling points to minimize the interference of photobleaching. j Specificity of pH sensing, the concentration of the interfering substances was 100 μg/mL. k Temperature crosstalk assessment: pH calibration curves at different temperatures
Figure 2. pH sensing performance of the fiber-optic theranostic probe. a pH sensing principle of HPTS-IP. The picture below shows the color change of HPTS-IP solution (10 μM in PBS buffer) with different pH values. b Absorption spectra of HPTS-IP solution (10 μM in PBS buffer) at varied pH values. c HPTS-IP is alternately excited by 405 nm and 450 nm light and emits fluorescence band peaks at 520 nm. d, e Fluorescence spectra and intensity calibration curves of the fiber-optic probe under 405 nm/450 nm excitation. f Ratiometric calibration curve in a pH range from 4.0 to 9.0. g Stability test in PBS buffer (pH 7.4) for 150 s. h Reversibility during cyclic immersion into pH 4.0/9.0 PBS buffers. i Leaching characteristics of HPTS-IP during 72-h immersion. Excitation light was blocked between the sampling points to minimize the interference of photobleaching. j Specificity of pH sensing, the concentration of the interfering substances was 100 μg/mL. k Temperature crosstalk assessment: pH calibration curves at different temperatures
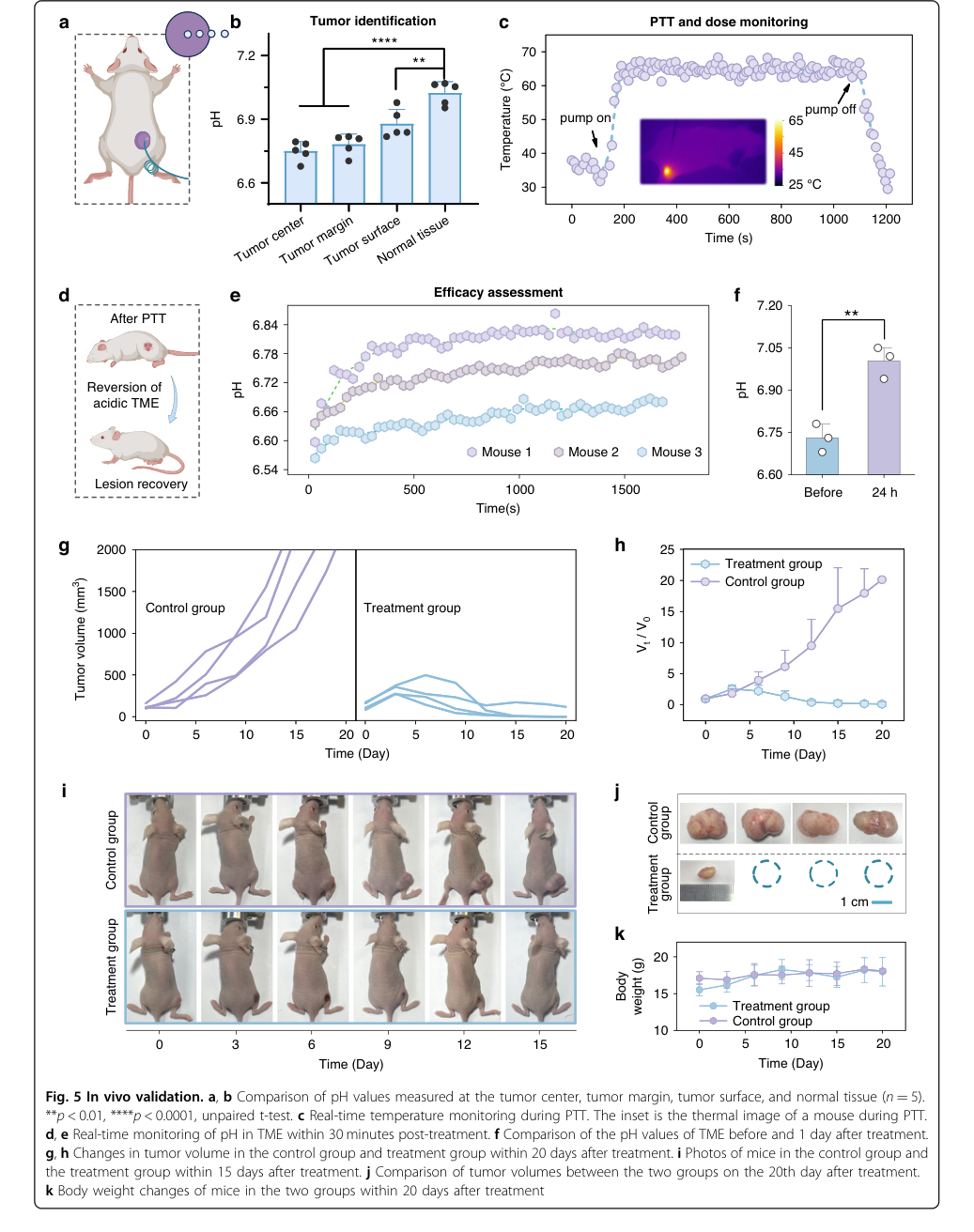 Figure 5. In vivo validation. a, b Comparison of pH values measured at the tumor center, tumor margin, tumor surface, and normal tissue (n = 5). **p < 0.01, ****p < 0.0001, unpaired t-test. c Real-time temperature monitoring during PTT. The inset is the thermal image of a mouse during PTT. d, e Real-time monitoring of pH in TME within 30 minutes post-treatment. f Comparison of the pH values of TME before and 1 day after treatment. g, h Changes in tumor volume in the control group and treatment group within 20 days after treatment. i Photos of mice in the control group and the treatment group within 15 days after treatment. j Comparison of tumor volumes between the two groups on the 20th day after treatment. k Body weight changes of mice in the two groups within 20 days after treatment
Figure 5. In vivo validation. a, b Comparison of pH values measured at the tumor center, tumor margin, tumor surface, and normal tissue (n = 5). **p < 0.01, ****p < 0.0001, unpaired t-test. c Real-time temperature monitoring during PTT. The inset is the thermal image of a mouse during PTT. d, e Real-time monitoring of pH in TME within 30 minutes post-treatment. f Comparison of the pH values of TME before and 1 day after treatment. g, h Changes in tumor volume in the control group and treatment group within 20 days after treatment. i Photos of mice in the control group and the treatment group within 15 days after treatment. j Comparison of tumor volumes between the two groups on the 20th day after treatment. k Body weight changes of mice in the two groups within 20 days after treatment
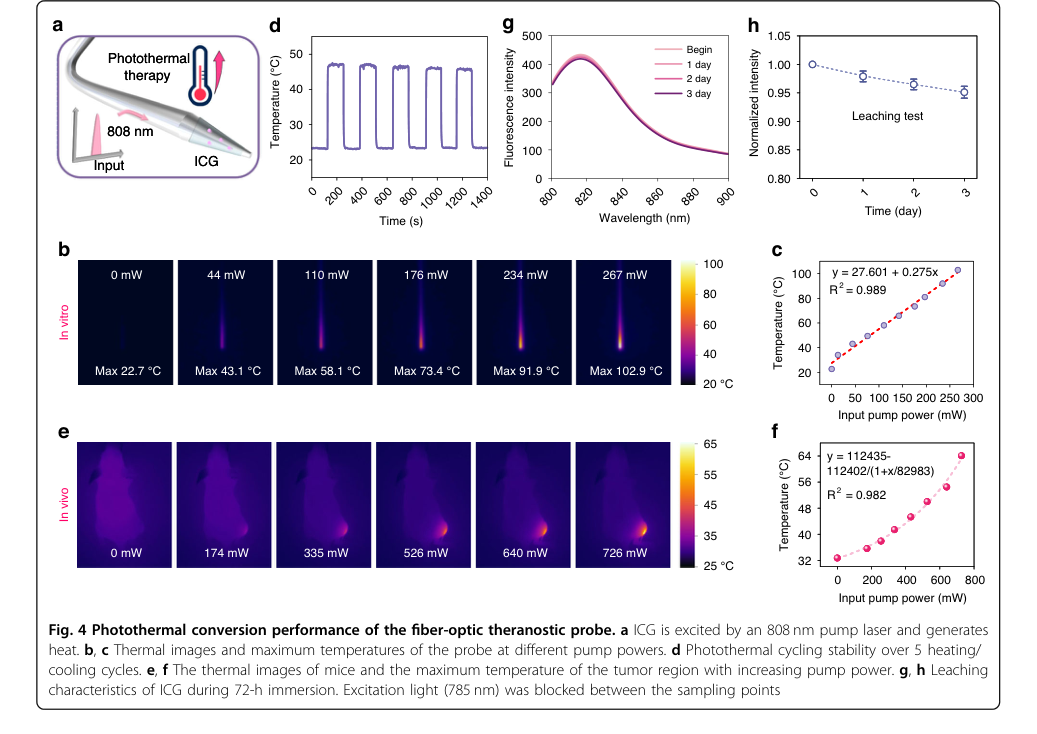 Figure 4. Photothermal conversion performance of the fiber-optic theranostic probe. a ICG is excited by an 808 nm pump laser and generates heat. b, c Thermal images and maximum temperatures of the probe at different pump powers. d Photothermal cycling stability over 5 heating/ cooling cycles. e, f The thermal images of mice and the maximum temperature of the tumor region with increasing pump power. g, h Leaching characteristics of ICG during 72-h immersion. Excitation light (785 nm) was blocked between the sampling points
Figure 4. Photothermal conversion performance of the fiber-optic theranostic probe. a ICG is excited by an 808 nm pump laser and generates heat. b, c Thermal images and maximum temperatures of the probe at different pump powers. d Photothermal cycling stability over 5 heating/ cooling cycles. e, f The thermal images of mice and the maximum temperature of the tumor region with increasing pump power. g, h Leaching characteristics of ICG during 72-h immersion. Excitation light (785 nm) was blocked between the sampling points
