多功能光纤诊疗探针用于闭环肿瘤光热治疗
The combination of optical fiber and phototheranostic agents has emerged as a promising strategy to address the challenges of limited light penetration depth and systemic toxicity of nanomaterials.
背景与学术渊源
起源与学术渊源
本文所解决的问题源于癌症这一严峻的全球健康挑战,每年导致数百万人患病和死亡。这一严峻形势促使人们投入大量研究,以开发更精确、更有效的诊断和治疗方法。在此背景下,“诊疗一体化”(theranostics)的概念应运而生,旨在将诊断和治疗功能整合到单一、空间共定位的平台中,以实现即时、靶向治疗和实时监测。
特别是光诊疗(photo-theranostics),它利用光进行诊断和治疗,因其高特异性、时空可控性和非电离性而备受关注。然而,其临床转化面临两大主要障碍:光在生物组织中的穿透深度本身就有限(由于散射和吸收,通常小于10毫米),以及作为诊疗剂的纳米材料在健康组织中的非特异性累积导致的全身毒性。
将光纤与光诊疗剂相结合被认为是克服这些限制的有前途的策略。光纤能够有效地将光传输到深部肿瘤,并允许治疗剂的局部限制,从而减轻全身毒性。尽管有这些优点,但以往的光纤探针设计却存在显著的“痛点”。大多数现有方法仅限于每根光纤实现单一功能,或由于光谱重叠导致功能间串扰。这通常需要多光纤配置,从而增加了器件的刚性、尺寸,并导致更具侵入性的操作,以及缺乏实时的治疗反馈。这些问题共同增加了组织损伤和治疗后炎症的风险,阻碍了广泛的临床应用。本文直接解决了这些根本性限制,提出了一种受波分复用(WDM)技术启发的、新颖的单光纤多功能集成方案,以实现具有实时反馈的闭环肿瘤光热治疗。
直观领域术语
- 诊疗一体化 (Theranostics):想象一个高度先进的医疗工具,它就像一个“诊断-治疗”超级英雄。它能立即告诉医生你体内哪里出了问题,然后立即将正确的治疗送到那个精确的位置,一气呵成。它是诊断和治疗的结合。
- 光热治疗 (Photothermal Therapy, PTT):将其视为使用一个微小、超聚焦的激光束来温和地加热并摧毁不需要的细胞,就像放大镜如何集中阳光来烧焦叶子上的一个小点一样。“光”(photo)部分意味着使用光,“热”(thermal)部分意味着产生热量。
- 波分复用 (Wavelength Division Multiplexing, WDM):想象一条非常繁忙的高速公路,但它承载的不是汽车,而是不同类型的信息,每种信息都以独特的光“颜色”传输。这使得许多不同的信号可以在同一根光纤上同时传输而不会相互干扰,从而大大提高了公路的效率。
- 肿瘤微环境 (Tumor Microenvironment, TME):这指的是肿瘤的直接周围环境,包括所有支持其生长的细胞、血管和化学信号。它就像肿瘤为自己创造的特定“社区”,可能与健康组织截然不同,通常更具酸性。
- 比率荧光探针 (Ratiometric Fluorescent Probes):考虑一个智能光传感器,它不仅测量一种颜色的光的亮度,还测量两种不同颜色的光的亮度并比较它们的比率。这使得测量更加可靠和准确,即使整体亮度因外部因素而变化,这类似于比较两个数字比仅依赖一个数字能提供更稳定的结果。
符号表
| 符号 | 描述 |
|---|---|
| $I_{450}/I_{405}$ | 450 nm 和 405 nm 处的荧光强度比,用于 pH 传感。 |
| $R$ | pH 分辨率,表示可可靠检测的最小 pH 变化。 |
| $s$ | 灵敏度,表示 pH 校准曲线的斜率。 |
| $T_1$ | pH 或温度传感值增加时的响应时间。 |
| $T_2$ | pH 或温度传感值减小时的响应时间。 |
| $I_{618}/I_{546}$ | 618 nm 和 546 nm 处的荧光强度比,用于温度传感。 |
| $p$ | p 值,用于确定实验结果显著性的统计量。 |
| $V/V_0$ | 归一化肿瘤体积,表示肿瘤体积相对于其初始体积的比值。 |
| $\sigma$ | 标准差,用于衡量一组数值的变异性或离散度。 |
问题定义与约束
核心问题表述与困境
本文解决的根本问题源于对有效且微创的癌症诊疗一体化——一种结合了诊断和治疗的方法——的迫切需求。当前的方法面临着阻碍其临床转化的重大限制。
输入/当前状态可由以下几个缺点表征:
1. 有限的光穿透深度与全身毒性:传统的光诊疗剂,通常基于纳米材料,由于散射和吸收,其在组织中的光穿透深度本身就有限(通常小于10毫米)。此外,它们在正常组织和器官中的非特异性累积会导致全身毒性。
2. 低估光纤的多路复用潜力:虽然光纤提供了接触深部肿瘤和局部限制药物的优势,但其在单一平台集成多种功能方面的潜力在很大程度上未被充分利用。
3. 功能间串扰与器件复杂性:先前的手持式光纤探针要么仅限于每根光纤实现单一功能,要么在尝试集成多种功能时,会遭受功能间串扰。这种串扰主要源于不同功能试剂吸收或发射光谱的重叠。为规避此问题,研究人员通常诉诸于多光纤配置,这不可避免地增加了器件的刚性和尺寸,使其与微创介入技术兼容性降低,并增加了组织损伤和治疗后炎症的风险。
4. 缺乏实时治疗反馈:现有方法通常缺乏对治疗剂量和疗效的实时监测能力,阻碍了闭环控制和个性化精准医疗。
期望的终点(输出/目标状态)是一个紧凑、多功能的单光纤光诊疗探针,能够:
1. 闭环肿瘤光热治疗 (PTT):这包括在单一平台上集成诊断和治疗功能,以实现实时反馈。
2. 多参数监测:探针应能够同时监测关键的肿瘤微环境 (TME) 参数,特别是 pH 和温度。
3. 微创介入:器件应紧凑(例如,作者实现的直径为440 µm),以便通过介入手术进入肿瘤病灶,避免扩大切口和重复侵入性操作。
4. 治疗前肿瘤识别:通过揭示肿瘤 pH 梯度来精确识别肿瘤边缘。
5. 治疗中热剂量控制:在 PTT 期间通过同时监测温度来精确控制热剂量。
6. 治疗后疗效评估:通过监测酸性 TME 的逆转来快速评估治疗疗效。
7. 克服光穿透与毒性:解决与纳米材料策略相关的光穿透深度和全身毒性限制。
本文试图弥合的确切缺失环节或数学鸿沟是开发一种稳健的单光纤平台,该平台能够同时执行多种诊疗功能(pH 传感、温度传感和光热治疗),且无功能间串扰,同时提供实时反馈。核心的数学/设计挑战在于选择并共固定多种功能性试剂(pH 指示剂、温度指示剂、光热剂),使其激发和发射光谱足够分离,以便在单根光纤上实现波分复用 (WDM)。这使得特定的功能可以在特定波长下按需激活,从而有效地消除了先前单光纤多路复用尝试中困扰的频谱重叠问题。本文的解决方案涉及仔细选择 HPTS-IP、LnMOF 和 ICG,它们的吸收带(HPTS-IP 为 405/450 nm,LnMOF 为 295 nm,ICG 为 790 nm)不重叠,从而实现了 WDM。
困扰先前研究人员的痛苦权衡或困境是功能多路复用与器件简单性/性能之间的固有冲突。为了实现多种功能,要么必须:
* 增加器件复杂性:使用多根光纤,导致笨重、刚性的器件不适合微创手术,并增加了患者风险。
* 牺牲功能完整性:尝试将多种试剂集成到单根光纤上,却因光谱重叠而遇到严重的功能间串扰,使得多功能性不可靠或不准确。这意味着改进一个方面(例如,增加更多功能)会直接破坏另一个方面(例如,信号完整性或器件尺寸)。
约束与失效模式
开发多功能光纤诊疗探针的问题极其困难,因为作者们遇到了几个严峻的现实障碍:
-
物理约束:
- 有限的光穿透深度:光在生物组织中的固有散射和吸收严重限制了其穿透深度,通常小于10毫米。这使得治疗深部肿瘤的光热疗法具有挑战性。
- 全身毒性:诊疗纳米材料在正常组织和器官中的非特异性累积会导致不良的全身毒性,这是临床转化的主要障碍。
- 器件刚性和尺寸:对于微创手术,探针必须灵活且紧凑。多光纤设计增加了刚性和尺寸,使其与介入技术不兼容,并增加了组织损伤的风险。
- 锥形光纤设计限制:锥形光纤的几何形状至关重要。过短的锥形会导致光泄漏并降低信噪比 (SNR),而过长的锥形则不适合局部传感和治疗。尖端直径影响了倏逝场强度(从而影响荧光激发/收集效率)以及指示剂固定可用的表面积,需要仔细优化(例如,发现 100 µm 是最优的)。
- 水凝胶薄膜完整性:用于封装功能性试剂的溶胶-凝胶基质必须稳定且生物相容。纯四乙基原硅酸酯 (TEOS) 薄膜容易出现严重裂纹,导致薄膜均匀性差和浸出率高,从而损害了传感器的稳定性和生物相容性。添加共前驱体如 GLYMO 和表面活性剂如 Triton X-100 是减轻这种情况所必需的。
-
数据驱动与性能约束:
- 功能间串扰:在单根光纤上实现多路复用的主要挑战是防止不同功能试剂(pH 指示剂、温度指示剂、光热剂)的吸收和发射光谱重叠。这种重叠会导致读数不准确,无法区分来自不同功能的信号。
- 实时延迟要求:对于闭环治疗和实时监测,传感器必须具有足够快的响应时间。本文报告的 pH 传感响应时间为 3.2 秒(pH 升高)和 12.8 秒(pH 降低),温度传感响应时间为 2.0 秒(温度升高)和 0.6 秒(温度降低),这被认为对于体内监测是可接受的。
- 传感器稳定性和可靠性:功能性试剂必须在生理环境中随时间保持稳定,并且不显著从光纤表面浸出。浸出测试显示荧光强度仅略有下降(72 小时内 HPTS-IP 下降 1.6%,LnMOF 下降 3.5%),表明稳定性良好。
- 生理因素干扰:传感性能必须能够抵抗复杂生理环境中存在的各种干扰物质,以及光漂白、指示剂浓度变化和光纤形态变化。使用比率荧光探针和仔细选择试剂有助于缓解这些问题。
- 组织自发荧光:组织内源性荧光会干扰探针的信号,降低传感精度和特异性。倏逝场的浅穿透深度,其中指示剂浓度较高,有助于维持高 SNR。
- 精确热剂量控制:在光热治疗过程中,在不引起相邻正常组织过度加热的情况下,递送有效热剂量至关重要。过热会导致组织损伤、血管塌陷和血流灌注受损。这需要精确的实时温度监测。
为什么选择这种方法
选择的必然性
作者选择采用单光纤多功能集成策略,利用波分复用(WDM)技术,这不仅仅是一种改进,而是由现有方法固有的局限性驱动的必然选择。本文明确指出了传统“最先进”(SOTA)方法不足的精确时刻:“尽管近期取得了进展,但光纤探针的多路复用潜力仍被低估。当前研究仍局限于每根光纤实现单一功能,或遭受功能间串扰,这主要源于所用功能试剂吸收或发射光谱的重叠。”这种光谱重叠问题意味着实现多参数监测或集成诊疗通常需要多光纤配置。然而,这种设置“不可避免地增加了器件的刚性和尺寸,降低了与微创介入技术的兼容性,并增加了组织损伤和治疗后炎症的风险。”鉴于这些关键缺点——缺乏实时反馈、侵入性以及功能串扰——需要范式转变。基于 WDM 的单光纤方法成为克服这些根本性挑战的唯一可行解决方案,它能够在单一、紧凑的平台上实现多种功能,而不会发生光谱干扰。
比较优势
除了简单的性能指标外,该方法还提供了深远的定性优势,主要通过其结构设计。核心优势在于利用波分复用技术将多种功能(pH 传感、温度监测和光热治疗)集成到单根光纤上。这种结构创新本质上最大限度地减少了功能间串扰,这是先前多试剂系统中一个严重的问题,其中光谱重叠会降低信号完整性。通过仔细选择具有“不重叠吸收带”的试剂(HPTS-IP、LnMOF、ICG),探针确保了每个参数的准确可靠测量。
此外,所选的 pH 和温度传感比率荧光探针提供了关键的定性优势。这种比率检测策略“减轻了光漂白、指示剂浓度变化和光纤形态变化对传感结果的干扰,便于获取准确可靠的信号。”这比强度测量有了显著改进,强度测量极易受到噪声和环境波动的影响。紧凑的单光纤设计还大大减小了与多光纤束相比的物理占地面积和刚性,使其在微创介入方面具有压倒性优势。它还局部化了诊疗剂,有效地减轻了游离纳米材料引起的全身毒性。
与约束的契合
所选方法完美契合了先进诊疗应用的严格约束。
- 微创性:使用单根柔性光纤(直径 = 440 µm,尖端直径 = 100 µm)允许“通过介入手术进入肿瘤病灶”,与多光纤或大型探针设计相比,大大降低了侵入性。这直接解决了最小化组织损伤和治疗后炎症的约束。
- 实时反馈与闭环治疗:将 pH 和温度指示剂与光热剂集成到单一平台上,实现了“具有实时反馈的闭环肿瘤光热治疗”。这意味着探针可以进行治疗前肿瘤识别(通过 pH 梯度)、治疗中剂量控制(在 PTT 期间通过温度监测)以及治疗后疗效评估(通过 TME pH 逆转),满足了动态、自适应治疗的关键需求。
- 多参数监测:波分复用方案允许在单根光纤上同时监测 pH 和温度,以及光热治疗。这直接满足了在复杂生物环境中进行全面多参数评估的要求。
- 降低全身毒性与深层组织接触:通过将光热剂固定在光纤表面,该方法“通过局部限制有效地减轻了脱靶毒性”。此外,光纤促进了“端到端的无损光传输”,能够传感和治疗“深部肿瘤”,从而克服了传统光诊疗剂有限的光穿透深度。
替代方案的拒绝
本文基于其在闭环、多功能肿瘤诊疗方面的根本性局限性,隐式和显式地拒绝了几种替代方案。
- 每根光纤单一功能实现:这些被认为不足,因为它们需要多根光纤来进行多参数监测和治疗,导致“扩大切口、重复侵入性操作”以及器件刚性增加。目标是集成诊疗,而不是碎片化的功能。
- 多光纤配置:虽然提供了多路复用,但由于其固有的物理限制(如“器件刚性和尺寸增加”)而被拒绝,这会损害与微创介入技术的兼容性并增加组织损伤的风险。
- 遭受功能间串扰的方案:明确指出功能试剂具有“吸收或发射光谱重叠”的方法是有问题的。作者仔细选择具有不重叠光谱的试剂以及 WDM 策略直接解决了这一失败点,确保了信号完整性。
- 依赖纳米材料的策略(无光纤集成):结论强调,与“依赖纳米材料的策略”相比,这种光纤方法“有效地解决了光穿透深度和全身毒性的限制。”这暗示仅依赖自由漂浮或非光纤集成的纳米材料将无法提供有效肿瘤光热治疗所需的深层组织接触和局部、无毒递送。
数学与逻辑机制
主方程
该诊疗探针传感能力的核心在于玻尔兹曼 S 型模型,它作为将比率荧光信号转化为有意义的生理参数(如 pH 和温度)的根本转换逻辑。虽然光热治疗部分涉及直接的光热转换,但其精确控制和监测完全依赖于这些传感机制提供的准确读数。
本文用于 pH 和温度传感的玻尔兹曼方程的通用形式可表示为:
$$ y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}} $$
其中:
- 对于 pH 传感(源自图 2f):
$$
R_{pH} = 0.97 - \frac{0.78}{1 + e^{(pH - 7.07)/0.87}}
$$
此处,$y$ 是荧光强度比 $R_{pH} = I_{520}(450nm) / I_{520}(405nm)$,而 $x$ 是 pH 值。
- 对于温度传感(源自图 3g):
$$ R_{Temp} = 1.55 - \frac{0.81}{1 + e^{(Temp - 65.74)/10.71}} $$
此处,$y$ 是荧光强度比 $R_{Temp} = I_{618} / I_{546}$,而 $x$ 是摄氏温度值。
这些方程是使探针能够定量解释其接收到的光学信号的核心数学引擎,为闭环诊疗提供关键反馈。
各项逐一剖析
让我们剖析通用玻尔兹曼方程 $y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}}$ 来理解每个组成部分的作用:
-
$y$ (荧光强度比,$R_{pH}$ 或 $R_{Temp}$)
- 数学定义:这是因变量,代表一个无量纲的荧光强度比。对于 pH 传感,它是当在 450 nm 激发时在 520 nm 处的发射强度与在 405 nm 激发时在 520 nm 处的发射强度之比 ($I_{520}(450nm) / I_{520}(405nm)$)。对于温度传感,它是 295 nm 激发下 618 nm 处发射强度与 546 nm 处发射强度之比 ($I_{618} / I_{546}$)。
- 物理/逻辑作用:该项是光学测量系统的直接输出。通过使用比率,作者巧妙地减轻了光漂白、指示剂浓度变化和光纤形态变化等常见误差源。这种归一化使得信号稳健可靠,充当了随目标参数可预测变化的初级可观测量。
- 为何使用比率/减法/除法:比率是比率传感中的标准技术,用于自参照和消除共模噪声。涉及减法和除法的整体 S 型形状自然源于化学或物理过程,其中指示剂响应连续变量在两种状态之间转换(例如,质子化/去质子化,或不同的能量转移状态),在两个极端都表现出饱和。
-
$x$ (生理参数,$pH$ 或 $Temp$)
- 数学定义:这是自变量,代表正在测量的环境条件(pH 或温度,单位为 °C)。
- 物理/逻辑作用:这是诊疗探针旨在检测和监测的实际物理量。它是系统旨在确定的“真实”值。
- 为何是自变量:它是原因,而 $y$ 是结果。校准过程建立了此输入与测量输出比率之间的函数关系。
-
$C_1$ (上限渐近线)
- 数学定义:一个常数系数,表示当 $x$ 趋近于正无穷时 S 型曲线的上限平台(对于这种形式的递减 S 型)。
- 物理/逻辑作用:对于 pH,$C_1 = 0.97$ 代表当 HPTS-IP 指示剂主要处于其质子化状态之一时(例如,在高 pH 下完全去质子化)达到的最大荧光比。对于温度,$C_1 = 1.55$ 代表在高温下 LnMOF 的最大比率。它定义了传感器动态范围的一个极端,表明当 $x$ 进一步增加时,平衡几乎完全移向一侧,指示剂状态不再显著改变。
- 为何是常数:它是指示剂及其与环境相互作用的固有特性,反映了指示剂在极端条件下可能发生的最大变化。
-
$C_2$ (范围缩放因子)
- 数学定义:一个常数系数,用于缩放 S 型转换的幅度。它代表了从下渐近线到上渐近线的 $y$ 的总变化量。
- 物理/逻辑作用:对于 pH,$C_2 = 0.78$ 决定了随着 pH 在敏感范围内变化,荧光比变化的总体跨度。对于温度,$C_2 = 0.81$ 对温度也做同样的事情。该项本质上定义了传感器响应的“高度”,表明了传感器响应的总动态范围。
- 为何是常数:它是指示剂固有特性的反映,反映了比率信号可能发生的最大变化。
-
$C_3$ (中点或转换中心)
- 数学定义:一个常数系数,表示响应位于渐近极限之间一半处的 $x$ 值(或斜率最大处)。
- 物理/逻辑作用:对于 pH,$C_3 = 7.07$ 表明 HPTS-IP 指示剂最敏感的 pH 值,通常对应于其 pKa。对于温度,$C_3 = 65.74$ °C 标志着 LnMOF 的能量转移机制表现出最陡峭变化时的温度。该参数对于定义传感器的有效范围和最佳灵敏度至关重要。
- 为何是常数:它是被指示剂监测的化学或物理过程的内在特性。
-
$C_4$ (斜率参数)
- 数学定义:一个常数系数,与 S 型曲线的最大斜率成反比。$C_4$ 的绝对值越小,曲线越陡峭。
- 物理/逻辑作用:对于 pH,$C_4 = 0.87$ 量化了 pH 响应曲线的陡峭程度。对于温度,$C_4 = 10.71$ 对温度也做同样的事情。该参数直接关系到传感器的灵敏度:在 $C_3$ 中点附近,对于 $x$ 的给定变化,较小的 $C_4$ 意味着荧光比的变化更快。
- 为何是常数:它反映了指示剂转换的固有响应性和协同性。
-
$e$ (欧拉数)
- 数学定义:一个数学常数,自然对数的底,约等于 2.71828。
- 物理/逻辑作用:它是指数函数的基础,指数函数在这里用于模拟 S 型转换。这种转换通常源于统计力学或化学平衡方程(如 Henderson-Hasselbalch 方程用于 pH,或玻尔兹曼分布用于能量状态),其中状态的概率随驱动力呈指数级变化。
- 为何是指数:指数项自然地描述了许多物理和化学系统在接近平衡时观察到的非线性、饱和行为。
-
指数 $(x - C_3)/C_4$
- 数学定义:指数函数的参数。
- 物理/逻辑作用:该项通过斜率参数 $C_4$ 将当前输入 $x$ 与中点 $C_3$ 之间的差值进行归一化。它有效地缩放输入以适应指数衰减或增长,确定系统距离其半转换点的距离。
-
除以 $(1 + e^{(x - C_3)/C_4})$
- 数学定义:这种特定形式是 S 型的核心,通常称为 Logistic 函数或 Fermi-Dirac 分布。
- 物理/逻辑作用:该项确保输出 $y$ 随着 $x$ 的变化在两个渐近线之间平滑过渡。它模拟了指示剂状态从一个极端到另一个极端的渐进转变。
-
减法 $C_1 - \frac{C_2}{...}$
- 数学定义:此操作将上限渐近线与缩放的 S 型项组合。
- 物理/逻辑作用:对于本文使用的特定形式,此减法创建了一个递减的 S 型曲线,如果 $C_2$ 为正,则意味着随着 $x$ 的增加,比率 $y$ 从高值开始下降到 $C_1 - C_2$。然而,图表(图 2f 和 3g)显示比率随 pH/温度的增加而增加。这表明作者拟合的方程 $y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}}$ 实际上是一个递增的 S 型曲线,其中 $C_1$ 是上限渐近线,$C_1 - C_2$ 是下限渐近线。当 $x \to -\infty$ 时,$e^{(x - C_3)/C_4} \to 0$,因此 $y \to C_1 - C_2$。当 $x \to +\infty$ 时,$e^{(x - C_3)/C_4} \to \infty$,因此 $y \to C_1$。这与图表一致。减法对于定义曲线的方向和范围至关重要。
分步流程
将诊疗探针想象成一个复杂的、微型的装配线,用于数据处理,其中每一步都将原始光学信号转化为可操作的生理见解。
-
光输入与波长选择:过程始于光源发出的光进入 Y 型光纤。根据所需的测量,选择特定的波长,就像从工具箱中选择工具一样。对于 pH 传感,系统在 405 nm 和 450 nm 激发光之间快速切换。对于温度传感,使用 295 nm 激发波长。这种波分复用 (WDM) 是决定探针功能的初始“开关”。
-
倏逝场相互作用:选定的光沿着光纤传输到其锥形尖端,在那里它作为“倏逝场”逸出到周围的水凝胶基质中。这个场像一个微观的网,直接与共固定的指示剂分子(pH 传感的 HPTS-IP,温度传感的 LnMOF)相互作用。指示剂吸收这些光而变得活跃。
-
荧光发射:被激发后,活跃的指示剂分子发出荧光。这种发射光的特性对局部环境敏感。对于 pH,HPTS-IP 在 520 nm 处发出荧光,但其在该波长下的强度取决于它是被 405 nm 还是 450 nm 激发,这反映了局部质子化状态。对于温度,LnMOF 在两个不同的波长 546 nm 和 618 nm 处发出荧光,由于能量转移动力学,它们的相对强度会根据局部温度而变化。
-
信号收集:然后,发射的荧光被高效地收集回同一根光纤,就像吸尘器吸入光一样,并从组织中引导出去。
-
光谱分析:收集到的光传输到荧光光谱分析仪 (FSA)。该设备充当“光分拣器”,测量相关发射波长处荧光的精确强度。对于 pH,它测量 $I_{520}(450nm)$ 和 $I_{520}(405nm)$。对于温度,它测量 $I_{618}$ 和 $I_{546}$。
-
比率计算:然后,一个计算单元从这些原始强度测量值中计算出一个无量纲比率。对于 pH,它计算 $R_{pH} = I_{520}(450nm) / I_{520}(405nm)$。对于温度,它计算 $R_{Temp} = I_{618} / I_{546}$。这个比率是输入到数学引擎的标准化的“数据点”。
-
玻尔兹曼模型转换:计算出的比率 ($R_{pH}$ 或 $R_{Temp}$) 然后输入到预先校准的玻尔兹曼方程中。该方程充当“解码器”,执行非线性转换,有效地反转校准曲线以产生实际的生理参数。例如,如果 $R_{pH}$ 被输入到 pH 玻尔兹曼方程中,它将输出相应的 pH 值。类似地,$R_{Temp}$ 输出温度。
-
实时反馈与行动:导出的 pH 和温度值实时显示。这些精确的读数作为关键反馈。在光热治疗 (PTT) 期间,温度读数允许“热剂量控制”,使操作员能够调整 808 nm 泵激光器的功率以维持目标温度(例如,在光纤尖端为 65 °C,确保肿瘤边缘达到 45 °C)。治疗后,通过监测肿瘤微环境 (TME) 酸性环境的逆转来评估疗效。这种闭环系统确保治疗不仅被递送,而且基于患者的实时生理状态持续优化。
优化动力学
该诊疗探针的“优化动力学”主要在于其初始校准以及其为稳健、实时反馈控制而设计的固有特性,而不是机器学习意义上的连续迭代学习。
-
校准作为初始“学习”:
- 数据采集:在临床应用之前,探针会经历严格的校准过程。这包括在受控实验室环境中将传感器暴露于一系列已知的 pH 值(例如,pH 4.0 至 9.0)和温度(例如,30 °C 至 100 °C)。在每个已知点,都会测量相应的比率荧光信号。
- 模型拟合:这些收集到的数据点(已知参数 $x$ 与测量比率 $y$)随后用于“训练”或“拟合”玻尔兹曼 S 型模型。这种拟合过程是一种非线性回归,其中玻尔兹曼方程的系数($C_1, C_2, C_3, C_4$)被迭代调整,以最小化模型预测比率与每个已知输入的可实验观察到的比率之间的差异(例如,平方误差和)。这类似于在“损失景观”中导航,以找到最能描述传感器响应曲线的最优参数集。本文报告了高 $R^2$ 值(pH 为 0.997,温度为 0.997),表明拟合效果极佳,因此损失景观清晰,具有明确的最小值。
- 参数固定:一旦确定了这些系数,它们就会被固定。传感器在运行期间不会“学习”或更新这些参数。这种一次性校准建立了传感器的“知识”库。
-
比率设计以实现稳健性(隐含优化):
- 选择比率传感是一项关键的设计“优化”。通过取两个荧光强度(用于 pH 的不同激发波长或用于温度的不同发射波长)的比率,系统会固有地消除许多常见噪声源。这包括激发光强度波动、指示剂光漂白、指示剂浓度变化以及光纤光学特性或耦合效率的微小变化。
- 这种机制确保信噪比 (SNR) 保持较高,并且传感器的输出稳定可靠,从而在没有明确算法更新的情况下有效地“优化”测量质量。稳定性测试(图 2g,h,i,j 和图 3j,k,l,n)证实了这种稳健性,显示了最小的标准差和浸出。
-
闭环反馈以优化治疗:
- 在实际的光热治疗过程中,系统作为一个闭环控制机制运行。传感器持续提供实时的温度和 pH 读数。
- 这些读数不用于更新传感器内部的数学模型,而是用于调整外部治疗输入。例如,如果监测到的温度偏离目标热剂量,则相应地调整泵激光器的功率(治疗输入)。这是一个经典反馈回路:传感(温度/pH)$\rightarrow$ 评估(与目标对比)$\rightarrow$ 行动(调整激光功率)。
- 这种基于实时传感器数据的治疗输入迭代调整是治疗本身如何优化以实现期望结果(例如,在光纤尖端将肿瘤温度维持在 65 °C,以确保肿瘤边缘达到 45 °C)同时最小化副作用的方式。系统通过持续监测和调整趋向于目标治疗状态,使治疗精确且自适应。
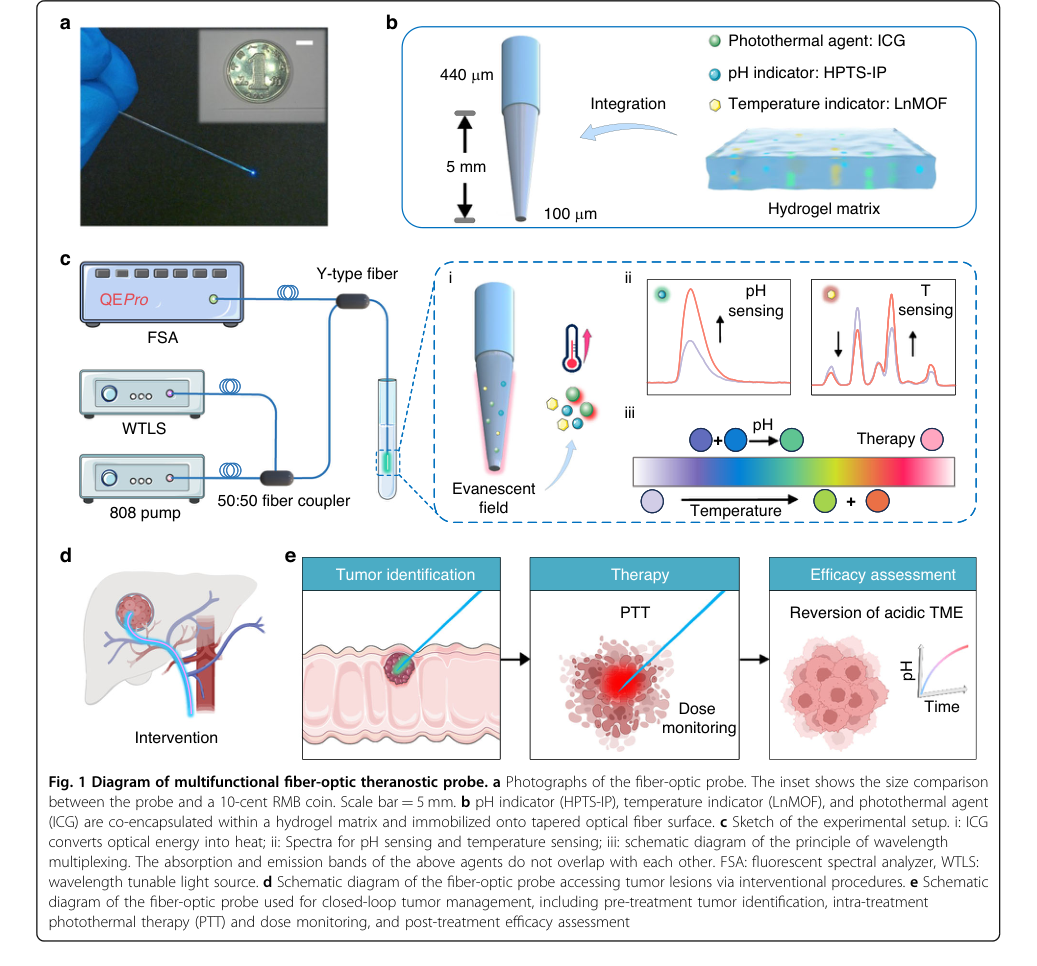 Figure 1. Diagram of multifunctional fiber-optic theranostic probe. a Photographs of the fiber-optic probe. The inset shows the size comparison between the probe and a 10-cent RMB coin. Scale bar = 5 mm. b pH indicator (HPTS-IP), temperature indicator (LnMOF), and photothermal agent (ICG) are co-encapsulated within a hydrogel matrix and immobilized onto tapered optical fiber surface. c Sketch of the experimental setup. i: ICG converts optical energy into heat; ii: Spectra for pH sensing and temperature sensing; iii: schematic diagram of the principle of wavelength multiplexing. The absorption and emission bands of the above agents do not overlap with each other. FSA: fluorescent spectral analyzer, WTLS: wavelength tunable light source. d Schematic diagram of the fiber-optic probe accessing tumor lesions via interventional procedures. e Schematic diagram of the fiber-optic probe used for closed-loop tumor management, including pre-treatment tumor identification, intra-treatment photothermal therapy (PTT) and dose monitoring, and post-treatment efficacy assessment
Figure 1. Diagram of multifunctional fiber-optic theranostic probe. a Photographs of the fiber-optic probe. The inset shows the size comparison between the probe and a 10-cent RMB coin. Scale bar = 5 mm. b pH indicator (HPTS-IP), temperature indicator (LnMOF), and photothermal agent (ICG) are co-encapsulated within a hydrogel matrix and immobilized onto tapered optical fiber surface. c Sketch of the experimental setup. i: ICG converts optical energy into heat; ii: Spectra for pH sensing and temperature sensing; iii: schematic diagram of the principle of wavelength multiplexing. The absorption and emission bands of the above agents do not overlap with each other. FSA: fluorescent spectral analyzer, WTLS: wavelength tunable light source. d Schematic diagram of the fiber-optic probe accessing tumor lesions via interventional procedures. e Schematic diagram of the fiber-optic probe used for closed-loop tumor management, including pre-treatment tumor identification, intra-treatment photothermal therapy (PTT) and dose monitoring, and post-treatment efficacy assessment
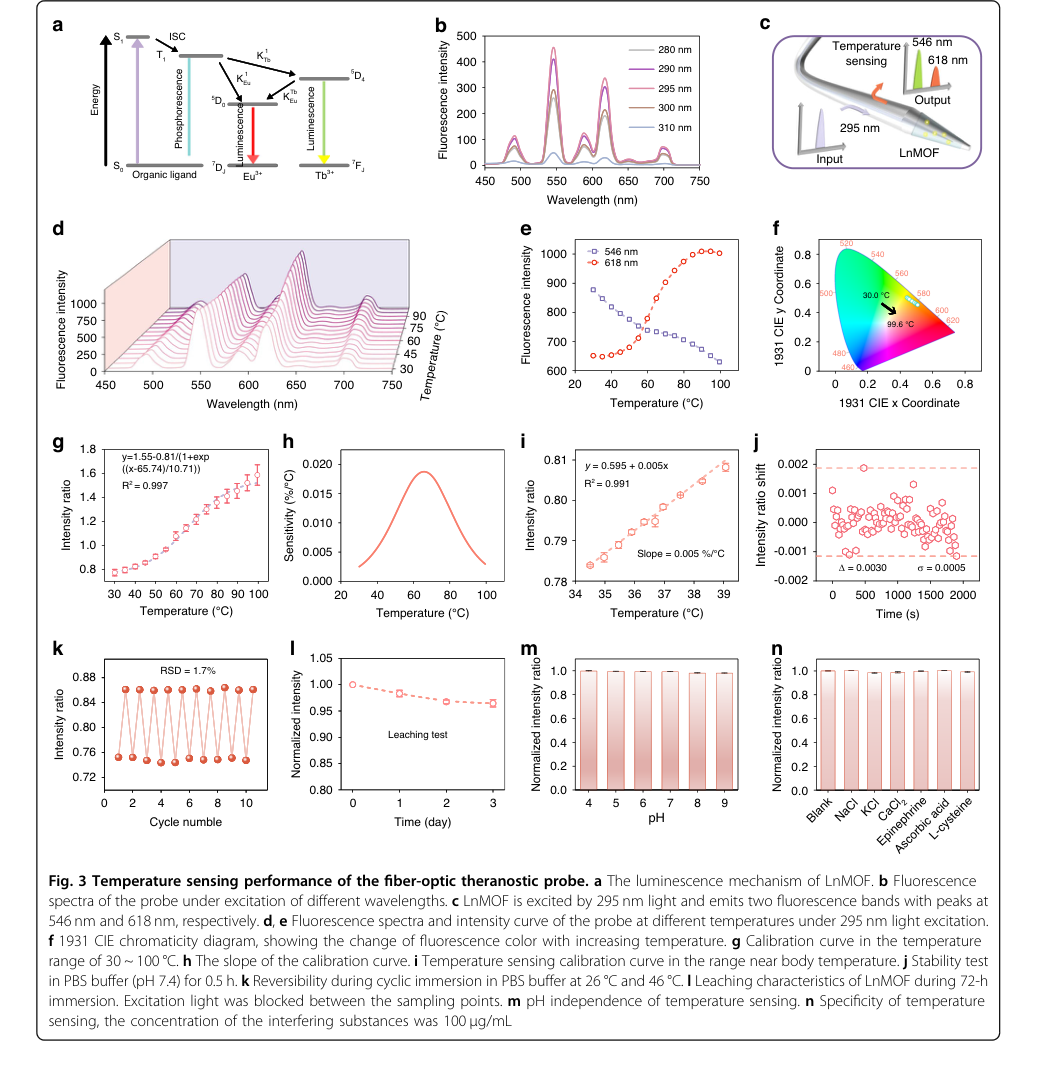 Figure 3. Temperature sensing performance of the fiber-optic theranostic probe. a The luminescence mechanism of LnMOF. b Fluorescence spectra of the probe under excitation of different wavelengths. c LnMOF is excited by 295 nm light and emits two fluorescence bands with peaks at 546 nm and 618 nm, respectively. d, e Fluorescence spectra and intensity curve of the probe at different temperatures under 295 nm light excitation. f 1931 CIE chromaticity diagram, showing the change of fluorescence color with increasing temperature. g Calibration curve in the temperature range of 30 ~ 100 °C. h The slope of the calibration curve. i Temperature sensing calibration curve in the range near body temperature. j Stability test in PBS buffer (pH 7.4) for 0.5 h. k Reversibility during cyclic immersion in PBS buffer at 26 °C and 46 °C. l Leaching characteristics of LnMOF during 72-h immersion. Excitation light was blocked between the sampling points. m pH independence of temperature sensing. n Specificity of temperature sensing, the concentration of the interfering substances was 100 μg/mL
Figure 3. Temperature sensing performance of the fiber-optic theranostic probe. a The luminescence mechanism of LnMOF. b Fluorescence spectra of the probe under excitation of different wavelengths. c LnMOF is excited by 295 nm light and emits two fluorescence bands with peaks at 546 nm and 618 nm, respectively. d, e Fluorescence spectra and intensity curve of the probe at different temperatures under 295 nm light excitation. f 1931 CIE chromaticity diagram, showing the change of fluorescence color with increasing temperature. g Calibration curve in the temperature range of 30 ~ 100 °C. h The slope of the calibration curve. i Temperature sensing calibration curve in the range near body temperature. j Stability test in PBS buffer (pH 7.4) for 0.5 h. k Reversibility during cyclic immersion in PBS buffer at 26 °C and 46 °C. l Leaching characteristics of LnMOF during 72-h immersion. Excitation light was blocked between the sampling points. m pH independence of temperature sensing. n Specificity of temperature sensing, the concentration of the interfering substances was 100 μg/mL
结果、局限性与结论
实验设计与基线
研究人员精心设计了实验,以严格验证其新型光纤诊疗探针的多功能能力和治疗效果。其实验架构的核心是证明探针能够利用单根光纤实现三种不同的功能——pH 传感、温度传感和光热治疗 (PTT),并利用波分复用 (WDM) 来防止串扰。
对于pH 传感,功能化了 HPTS-IP 的探针在室温下,在宽 pH 范围(4.0 至 9.0)的磷酸盐缓冲盐水 (PBS) 溶液中进行了测试。在 pH 7.4 PBS 中连续记录 150 秒光谱来评估其稳定性。通过在五个周期内交替浸入 pH 4.0 和 9.0 的缓冲液来证明其可逆性。在 pH 7.4 PBS 中浸泡 72 小时来评估浸出特性。为确认在复杂生物环境中的可靠性,探针的特异性针对常见的干扰物质如 NaCl、KCl、CaCl₂、肾上腺素、抗坏血酸和 L-半胱氨酸进行了测试。至关重要的是,通过在 26 至 41 °C 之间改变温度来测量 pH 来评估温度串扰。
温度传感利用了 LnMOF,并在宽范围(30-100 °C)内进行了评估,特别是在生理相关范围(34.5-39 °C)内。在 pH 7.4 PBS 中进行了 0.5 小时的稳定性测试,并通过在 26 °C 和 46 °C 的 PBS 中交替浸泡 10 个周期来证明其可逆性。在 72 小时内监测了浸出情况,并通过在 pH 4.0 至 9.0 的缓冲液中进行测试来确认其 pH 独立性。还评估了对干扰物质的特异性。
对于光热转换,经过 ICG 功能化的探针在体外使用 808 nm 泵激光器进行了测试,测量了在不同泵功率(高达 267 mW)下的最高温度。通过五个加热/冷却周期评估了光热稳定性,并在 72 小时内监测了 ICG 浸出情况。这里的“受害者”是传统纳米材料基 PTT 系统通常需要高泵功率(通常超过 1 W)的要求,这使得该方法更具成本效益并减少了潜在的副作用。
最终的验证是通过使用 BALB/c nude 小鼠皮下结直肠癌异种移植模型进行的体内实验。在干预前,肿瘤被允许生长至约 100 mm³。
- 肿瘤识别通过将探针插入肿瘤组织、相邻正常组织、肿瘤表面和正常组织,并比较测量的 pH 值来严格测试。
- PTT 和剂量监测涉及将探针插入肿瘤中心,并在 15 分钟内主动将光纤温度维持在 65 °C,热成像证实肿瘤边缘达到了有效的治疗温度 45 °C。
- 疗效评估是多方面的:治疗后(30 分钟和 24 小时)肿瘤微环境 (TME) 的实时 pH 监测,以及 20 天内每 3 天对肿瘤体积和体重进行长期监测。在这种情况下,“受害者”是没有接受治疗的对照组小鼠,它们的肿瘤表现出进行性生长,当体积超过 2000 mm³ 时被安乐死。
- 生物相容性通过体外培养 HCT116 细胞与探针浸出液(24 小时)并进行 CCK-8 测定和活/死染色来评估。体内,通过治疗后 24 小时在植入(仅光纤植入)和治疗组中的 H&E 染色来评估器官生物相容性(心脏、肝脏、脾脏、肺、肾脏),并与对照组进行比较。肿瘤组织在治疗后 24 小时的组织学和免疫组织化学分析(Caspase-3、HIF-1α、Ki67)进行了评估,并以假处理组(仅光纤植入,无激光激发)作为比较基线。
证据证明了什么
本文提供的证据明确证明了多功能光纤诊疗探针的成功开发和功能,该探针能够实现具有实时反馈的闭环肿瘤光热治疗。
波分复用 (WDM) 用于非重叠激发带的核心数学声明,通过 HPTS-IP(405 nm、450 nm)、LnMOF(295 nm)和 ICG(790 nm)的明显吸收光谱被无情地证明(如图 2b 和图 S7 所示)。这种光谱分离是核心机制能够按需切换功能的明确证据,有效地消除了先前多试剂系统中存在的、功能间串扰这一重大限制。
对于pH 传感,探针表现出卓越的性能:
- 在 6.0 至 8.0 的线性范围内,它实现了 0.013 pH 单位的高分辨率,这对于区分正常和肿瘤组织中的生理 pH 值至关重要。这源于玻尔兹曼模型拟合(图 2f)和显示标准差 ($\sigma$) 为 0.0009 的稳定性测试(图 2g)。
- 在五个周期内,相对标准差 (RSD) 为 0.8%,证明了出色的可逆性(图 2h),表明性能一致。
- HPTS-IP 的浸出量极少(72 小时内荧光强度下降 1.6%,图 2i)以及对各种干扰物质的优异选择性(图 2j)进一步验证了其在复杂生物环境中的可靠性。
- 至关重要的是,在 pH 范围 4.0 至 7.0 内观察到可忽略的温度串扰,并且对于 pH > 7.0,探针集成的温度监测能力提供了内置补偿,确保了准确的 pH 传感(图 2k)。
温度传感也表现出稳健的性能:
- 比率方法利用了 Tb³⁺ 到 Eu³⁺ 的热增强能量转移(图 3a, c),实现了精确监测。
- 在生理相关范围(34.5-39 °C)内观察到线性关系,实现了 0.3 °C 的分辨率,满足了体内监测要求(图 3i)。
- 高可逆性(10 个周期内 RSD 为 1.7%,图 3k)和极少的 LnMOF 浸出(72 小时内下降 3.5%,图 3l)得到了证明。
- 证据还证明了其 pH 独立性(图 3m)和优异的特异性(图 3n),确保了无论 pH 波动或其他生物干扰物如何,都能获得准确的温度读数。
光热转换能力得到了明确确立:
- 在仅 267 mW 的激发下,探针体外加热至 102.9 °C(图 4b, c),证实了高效的光热转换。这与传统纳米材料基系统通常需要大于 1 W 的泵功率相比,是一个显著的胜利,使得该方法更具成本效益并减少了潜在的副作用。
- 在五个加热/冷却周期中温度稳定升高,显示了出色的光热稳定性(图 4d),并且极少的 ICG 浸出(72 小时内下降 5.9%,图 4g, h)确保了长期性能。
- 体内实验证实了随着泵功率的升高,肿瘤区域的温度逐渐升高(图 4e, f)。
体内验证为探针的实际应用提供了最令人信服的证据:
- 肿瘤边缘识别通过健康组织和肿瘤组织之间测量的 pH 值存在统计学上的显著差异(p < 0.0001),以及肿瘤表面和正常组织之间(p < 0.01)(图 5a, b)得到了明确证明。这是其诊断能力的明确证据。
- 在 PTT 期间,通过将光纤温度主动维持在 65 °C,实现了精确的热剂量控制,这确保了肿瘤边缘达到有效的治疗温度 45 °C(图 5c)。
- 快速疗效评估通过治疗后 TME 中 pH 的显著升高(30 分钟内增加 0.12-0.22 单位,24 小时时 p < 0.01)(图 5d, e, f)得到了验证,这作为治疗反应的可靠生物标志物。
- 抗肿瘤疗效的最终证明来自于肿瘤体积监测:4 只接受治疗的小鼠中有 3 只显示肿瘤完全消退,其余一只小鼠的肿瘤生长受到显著抑制,而“受害者”对照组则表现出进行性肿瘤生长(图 5g, h, i, j)。
- 优异的生物相容性和生物安全性通过所有小鼠体重的稳定(图 5k)、H&E 染色器官中没有显著的凋亡/坏死区域或炎症细胞浸润(图 S10),以及体外浸出液测试中的高细胞活力(图 S9, 图 6c)得到了证实。
- 最后,多模式抗肿瘤作用通过组织学分析(图 6a)得到证实,显示治疗后的肿瘤中存在多灶性坏死和出血区域。免疫组织化学显示凋亡生物标志物 Caspase-3 上调,增殖生物标志物 Ki67 下调,以及 HIF-1α 下调,表明肿瘤缺氧得到缓解,这通过 MRI 得到了进一步证实(图 6b, 图 S8)。这些全面的证据无可辩驳地证明了探针的核心机制在现实中确实有效,从而实现了有效的肿瘤消融和 TME 重塑。
局限性与未来方向
尽管所提出的光纤诊疗探针展现了卓越的能力,但承认其某些局限性并考虑未来发展的方向至关重要。
一个固有的局限性,尽管通过光纤设计得到了缓解,是光穿透深度。倏逝场虽然实现了局部传感,但穿透深度很浅(图 S5),这意味着探针主要感知和治疗其表面的直接邻近区域。虽然这适用于精确的局部干预,但更广泛的 TME 体积映射可能需要多个探针或更先进的光学策略。pH 传感(降低时高达 12.8 秒)和温度传感(升高时高达 2.0 秒)的响应时间对于许多应用来说是良好的,但对于捕捉极其快速的、毫秒级的生理动态可能是一个限制。
另一个实际考虑是浸出。尽管本文报告了 HPTS-IP(1.6%)、LnMOF(3.5%)和 ICG(5.9%)在 72 小时内的浸出量极少,但这并非为零。对于可长期植入的设备,即使是极少的慢性浸出也可能在数周或数月内累积或引发免疫反应,可能影响探针性能和患者安全。提及在采样点之间阻挡激发光以尽量减少光漂白(图 2i, 3l 标题)表明,虽然比率检测有所帮助,但光漂白仍然是一个可能影响超长期连续监测的因素。此外,虽然 pH 传感的温度串扰在 pH > 7.0 时得到了补偿,但在整个 pH 范围内并非完全可忽略,这表明一种微妙的相互作用,未来可能需要更复杂的补偿算法。选择单一涂层,虽然优化了 SNR 和响应时间,但意味着一种权衡;更厚的薄膜可以增强信号,但会以牺牲响应速度为代价。
展望未来,本文本身就提出了几个令人兴奋的方向。集成策略可以转化为柔性聚合物和水凝胶光纤,以增强机械顺应性和生物相容性,为长期植入设备铺平道路。利用光谱资源并采用多峰拟合算法可以通过解决更多功能集成时可能出现的发射带重叠问题,进一步增强功能容量。作者还建议将系统与MRI 温热学集成,以实现对肿瘤边缘更精确的温度监测,这意味着在没有这种补充的情况下,当前的红外成像可能在空间分辨率或深度方面存在局限性。
除了本文的明确建议外,还出现了几个讨论话题以供进一步发展和演变:
-
高级多参数集成与 AI 驱动反馈:通过 WDM 或其他多路复用技术,还能将多少个 TME 参数(例如,氧饱和度、葡萄糖水平、特定酶活性、药物浓度)同时集成到单根光纤中,而不损害信号完整性或增加设备复杂性?能否将来自这种探针的实时数据输入人工智能 (AI) 或机器学习 (ML) 模型,以创建真正自适应的个性化治疗方案,根据不断演变 TME 动态调整激光功率、持续时间甚至药物递送?这可以超越简单的反馈回路,实现预测性、优化的治疗。
-
长期生物稳定性和免疫调节:虽然短期生物相容性已得到证明,但慢性植入的长期影响是什么?生物污垢、宿主组织包膜或慢性炎症反应如何影响探针在数月或数年内的传感精度和治疗效果?是否可以通过释放抗炎药物或生长因子来主动促进整合并最小化不良反应,从而对溶胶-凝胶基质进行免疫调节?
-
可扩展性、小型化和临床工作流程集成:目前的探针直径为 440 µm,尖端直径为 100 µm。能否进一步小型化以实现更微创的手术,或者能否开发这种探针的阵列来治疗更大或多灶性肿瘤?扩大生产以供广泛临床使用存在哪些制造挑战和成本?这种复杂的设备如何与现有临床工作流程集成,考虑到对专业培训、设备和数据解释的需求?
-
非侵入性引导和辅助疗法:能否将这种闭环诊疗系统的原理改编为引导或增强非侵入性疗法?例如,一种侵入性较小的探针版本能否提供实时的 TME 反馈,以优化外部放疗、聚焦超声或全身化疗,而不是仅执行 PTT?这将拓宽其应用范围,超越直接肿瘤消融。
-
伦理考量和患者体验:随着这些设备变得越来越复杂和可植入,关于数据隐私、患者自主权以及持续、自适应治疗可能带来的过度治疗或意外副作用的风险,存在哪些伦理考量?如何优化患者体验,最大限度地减少与植入设备和频繁监测相关的身体不适和心理负担?
这些讨论突显了这项技术的巨大潜力,同时也强调了为其充分实现和广泛的肿瘤学影响所必须应对的复杂、多学科挑战。
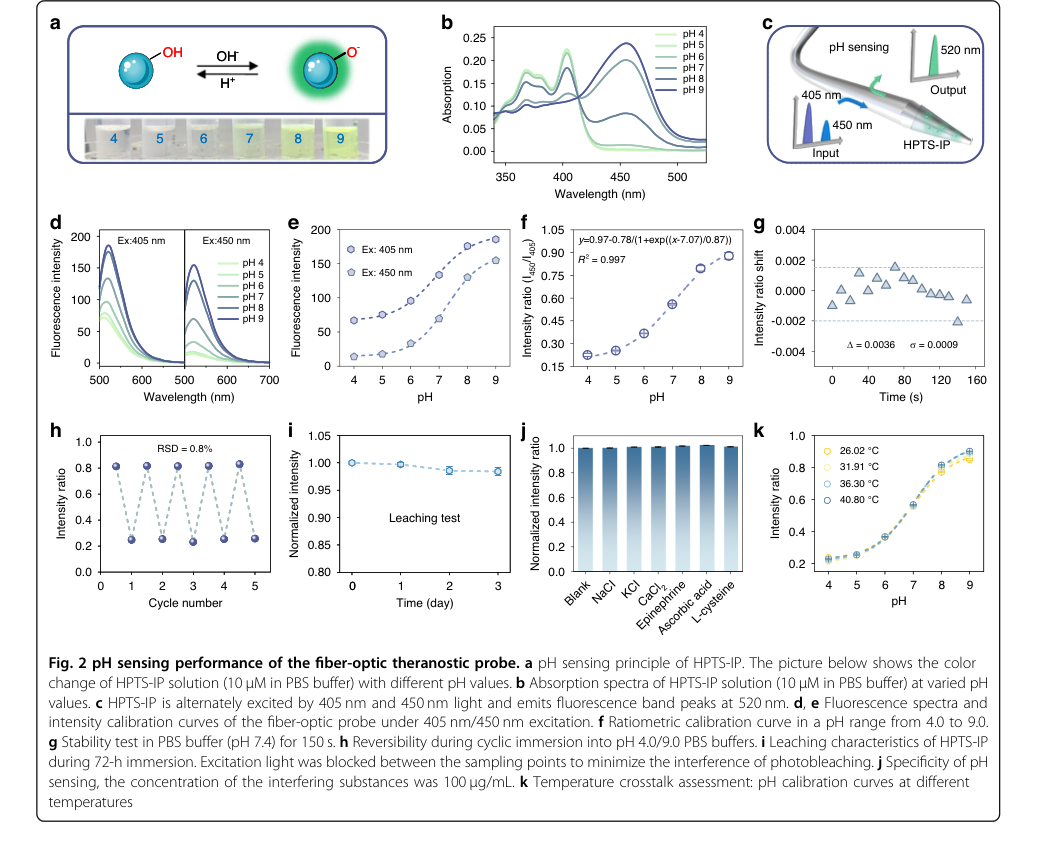 Figure 2. pH sensing performance of the fiber-optic theranostic probe. a pH sensing principle of HPTS-IP. The picture below shows the color change of HPTS-IP solution (10 μM in PBS buffer) with different pH values. b Absorption spectra of HPTS-IP solution (10 μM in PBS buffer) at varied pH values. c HPTS-IP is alternately excited by 405 nm and 450 nm light and emits fluorescence band peaks at 520 nm. d, e Fluorescence spectra and intensity calibration curves of the fiber-optic probe under 405 nm/450 nm excitation. f Ratiometric calibration curve in a pH range from 4.0 to 9.0. g Stability test in PBS buffer (pH 7.4) for 150 s. h Reversibility during cyclic immersion into pH 4.0/9.0 PBS buffers. i Leaching characteristics of HPTS-IP during 72-h immersion. Excitation light was blocked between the sampling points to minimize the interference of photobleaching. j Specificity of pH sensing, the concentration of the interfering substances was 100 μg/mL. k Temperature crosstalk assessment: pH calibration curves at different temperatures
Figure 2. pH sensing performance of the fiber-optic theranostic probe. a pH sensing principle of HPTS-IP. The picture below shows the color change of HPTS-IP solution (10 μM in PBS buffer) with different pH values. b Absorption spectra of HPTS-IP solution (10 μM in PBS buffer) at varied pH values. c HPTS-IP is alternately excited by 405 nm and 450 nm light and emits fluorescence band peaks at 520 nm. d, e Fluorescence spectra and intensity calibration curves of the fiber-optic probe under 405 nm/450 nm excitation. f Ratiometric calibration curve in a pH range from 4.0 to 9.0. g Stability test in PBS buffer (pH 7.4) for 150 s. h Reversibility during cyclic immersion into pH 4.0/9.0 PBS buffers. i Leaching characteristics of HPTS-IP during 72-h immersion. Excitation light was blocked between the sampling points to minimize the interference of photobleaching. j Specificity of pH sensing, the concentration of the interfering substances was 100 μg/mL. k Temperature crosstalk assessment: pH calibration curves at different temperatures
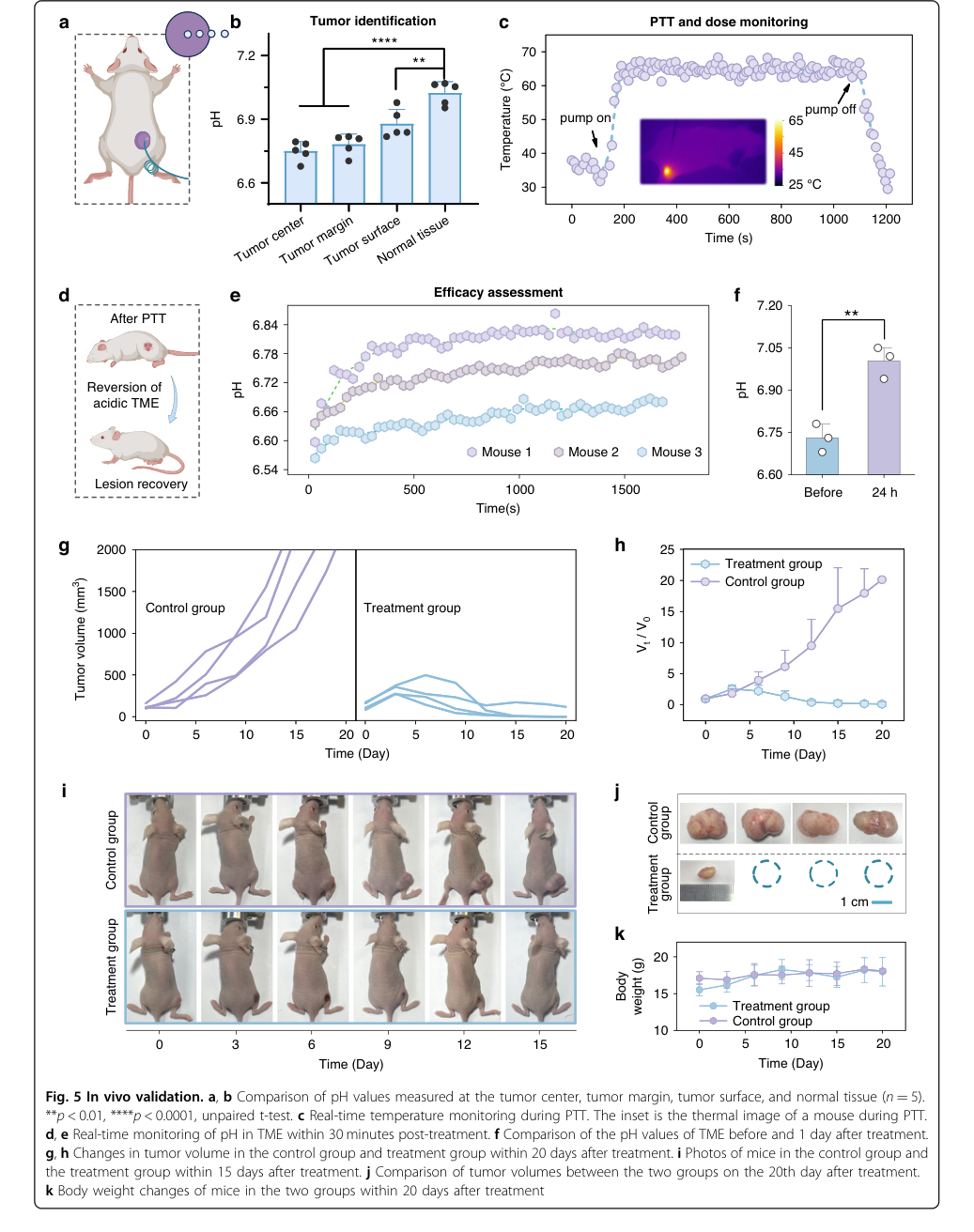 Figure 5. In vivo validation. a, b Comparison of pH values measured at the tumor center, tumor margin, tumor surface, and normal tissue (n = 5). **p < 0.01, ****p < 0.0001, unpaired t-test. c Real-time temperature monitoring during PTT. The inset is the thermal image of a mouse during PTT. d, e Real-time monitoring of pH in TME within 30 minutes post-treatment. f Comparison of the pH values of TME before and 1 day after treatment. g, h Changes in tumor volume in the control group and treatment group within 20 days after treatment. i Photos of mice in the control group and the treatment group within 15 days after treatment. j Comparison of tumor volumes between the two groups on the 20th day after treatment. k Body weight changes of mice in the two groups within 20 days after treatment
Figure 5. In vivo validation. a, b Comparison of pH values measured at the tumor center, tumor margin, tumor surface, and normal tissue (n = 5). **p < 0.01, ****p < 0.0001, unpaired t-test. c Real-time temperature monitoring during PTT. The inset is the thermal image of a mouse during PTT. d, e Real-time monitoring of pH in TME within 30 minutes post-treatment. f Comparison of the pH values of TME before and 1 day after treatment. g, h Changes in tumor volume in the control group and treatment group within 20 days after treatment. i Photos of mice in the control group and the treatment group within 15 days after treatment. j Comparison of tumor volumes between the two groups on the 20th day after treatment. k Body weight changes of mice in the two groups within 20 days after treatment
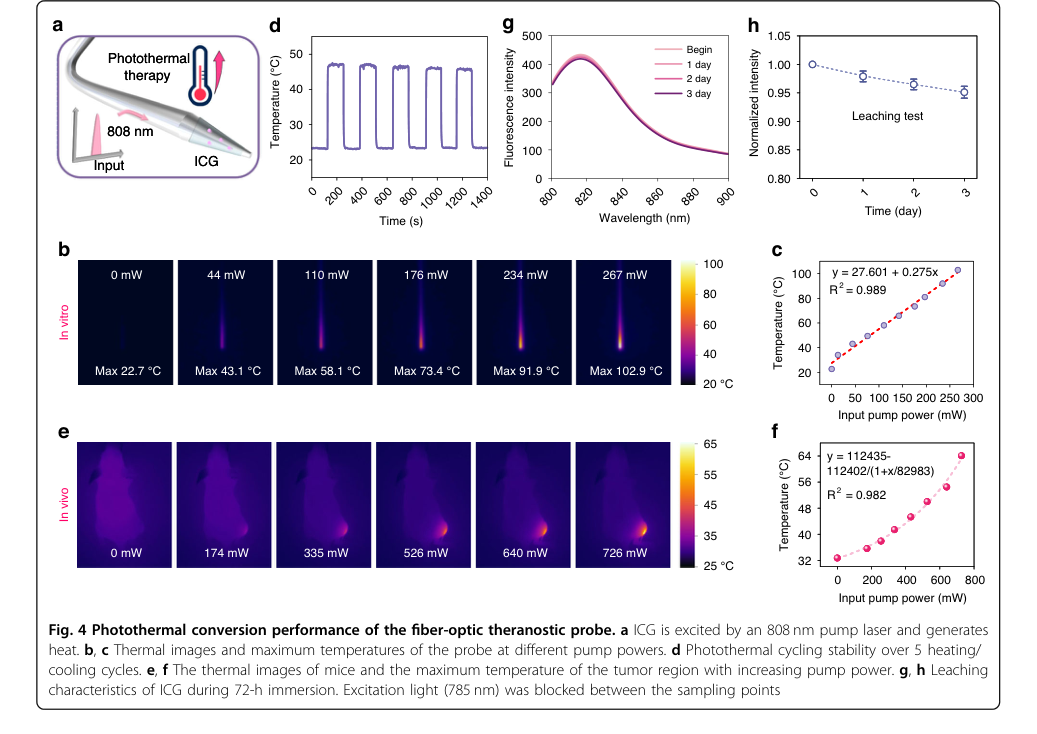 Figure 4. Photothermal conversion performance of the fiber-optic theranostic probe. a ICG is excited by an 808 nm pump laser and generates heat. b, c Thermal images and maximum temperatures of the probe at different pump powers. d Photothermal cycling stability over 5 heating/ cooling cycles. e, f The thermal images of mice and the maximum temperature of the tumor region with increasing pump power. g, h Leaching characteristics of ICG during 72-h immersion. Excitation light (785 nm) was blocked between the sampling points
Figure 4. Photothermal conversion performance of the fiber-optic theranostic probe. a ICG is excited by an 808 nm pump laser and generates heat. b, c Thermal images and maximum temperatures of the probe at different pump powers. d Photothermal cycling stability over 5 heating/ cooling cycles. e, f The thermal images of mice and the maximum temperature of the tumor region with increasing pump power. g, h Leaching characteristics of ICG during 72-h immersion. Excitation light (785 nm) was blocked between the sampling points
与其他领域的同构性
结构骨架
一个系统,利用不同的光谱通道同时感知多个环境参数,并提供靶向干预,具有实时反馈以实现自适应控制。
