폐쇄 루프 종양 광열 치료를 위한 다기능 광섬유 치료 진단 프로브
The combination of optical fiber and phototheranostic agents has emerged as a promising strategy to address the challenges of limited light penetration depth and systemic toxicity of nanomaterials.
배경 및 학문적 계보
기원 및 학술적 계보
본 논문에서 다루는 문제는 매년 수백만 건의 신규 환자와 사망자를 발생시키는 암으로 인한 심각한 전 지구적 건강 문제에서 비롯된다. 이러한 절박한 상황은 보다 정확하고 효과적인 진단 및 치료법 개발을 위한 광범위한 연구를 촉발시켰다. 이러한 맥락에서 "테라노스틱스(theranostics)"라는 개념이 등장했으며, 이는 진단 및 치료 기능을 단일의 공간적으로 공존하는 플랫폼에 통합하여 즉각적이고 표적화된 치료와 실시간 모니터링을 가능하게 하는 것을 목표로 한다.
특히, 진단과 치료 모두에 빛을 활용하는 광-테라노스틱스(photo-theranostics)는 높은 특이성, 시공간적 제어, 비이온화 특성으로 인해 상당한 주목을 받았다. 그러나 임상적 적용에는 두 가지 주요 난관에 직면했다: 생체 조직 내 빛의 고유한 투과 깊이 제한(산란 및 흡수로 인해 일반적으로 10 mm 미만)과 테라노스틱스 시약으로 사용되는 나노물질이 정상 조직에 비특이적으로 축적되어 발생하는 전신 독성이다.
광섬유와 광-테라노스틱스 시약을 결합하는 것이 이러한 한계를 극복하기 위한 유망한 전략으로 확인되었다. 광섬유는 심부 종양으로의 효율적인 빛 전달을 촉진하고 치료제를 국소적으로 제한할 수 있어 전신 독성을 완화한다. 이러한 장점에도 불구하고, 기존의 광섬유 프로브 설계는 상당한 "고충점(pain points)"을 겪었다. 대부분의 기존 접근 방식은 섬유당 단일 기능 구현에 국한되거나 시약 간의 스펙트럼 중첩으로 인한 기능 간 간섭을 경험했다. 이는 종종 다중 섬유 구성을 필요로 하여 장치 강성 증가, 치수 확대, 보다 침습적인 시술, 실시간 치료 피드백 부족으로 이어졌다. 이러한 문제들은 복합적으로 조직 손상 및 치료 후 염증의 위험을 증가시켜 광범위한 임상 채택을 방해했다. 본 논문은 파장 분할 다중화(WDM) 기술에서 영감을 받은 새로운 단일 섬유 다기능 통합 방안을 제안함으로써 이러한 근본적인 한계를 직접적으로 해결하고, 실시간 피드백을 갖춘 폐쇄 루프 종양 광열 치료를 가능하게 한다.
직관적인 분야 용어
- 테라노스틱스 (Theranostics): 진단과 치료를 동시에 수행하는 "진단-치료" 슈퍼히어로와 같은 매우 발전된 의료 도구를 상상해 보라. 이 도구는 의사에게 신체 내부의 문제를 즉시 알려주고, 그 정확한 부위에 즉시 올바른 치료를 전달할 수 있다. 이는 진단과 치료의 결합이다.
- 광열 치료 (Photothermal Therapy, PTT): 마치 돋보기로 햇빛을 집중시켜 나뭇잎의 작은 부분을 태우는 것처럼, 작고 매우 집중된 레이저 빔을 사용하여 원치 않는 세포를 가열하여 파괴하는 것으로 생각할 수 있다. "광(photo)"은 빛이 사용됨을 의미하고, "열(thermal)"은 열이 발생함을 의미한다.
- 파장 분할 다중화 (Wavelength Division Multiplexing, WDM): 매우 바쁜 단일 고속도로를 상상하되, 자동차 대신 각기 다른 "색깔"의 빛을 타고 이동하는 다양한 종류의 정보가 전달되는 것이다. 이를 통해 여러 다른 신호가 서로 간섭하지 않고 동일한 섬유를 통해 동시에 전송될 수 있어 고속도로의 효율성을 크게 높인다.
- 종양 미세환경 (Tumor Microenvironment, TME): 이는 종양의 즉각적인 주변 환경을 의미하며, 종양의 성장을 지원하는 모든 세포, 혈관 및 화학 신호를 포함한다. 이는 종양이 스스로 만들어내는 특정 "이웃"과 같으며, 종종 더 산성인 건강한 조직과는 상당히 다를 수 있다.
- 비율 형광 프로브 (Ratiometric Fluorescent Probes): 단순히 한 가지 색깔의 빛의 밝기만을 측정하는 것이 아니라, 두 가지 다른 색깔의 밝기를 측정하고 그 비율을 비교하는 스마트한 광 센서를 고려해 보라. 이는 전체 밝기가 외부 요인으로 인해 변하더라도 측정을 훨씬 더 신뢰할 수 있고 정확하게 만든다. 이는 마치 하나의 숫자에만 의존하는 것보다 두 숫자를 비교하는 것이 더 안정적인 결과를 제공하는 것과 유사하다.
표기법 테이블
| 표기법 | 설명 |
|---|---|
| $I_{450}/I_{405}$ | 450 nm 및 405 nm에서의 형광 강도 비율, pH 감지에 사용됨. |
| $R$ | pH 해상도, 신뢰성 있게 감지할 수 있는 pH의 가장 작은 변화를 나타냄. |
| $s$ | 민감도, pH 보정 곡선의 기울기를 나타냄. |
| $T_1$ | 값이 증가할 때 pH 또는 온도 감지에 대한 응답 시간. |
| $T_2$ | 값이 감소할 때 pH 또는 온도 감지에 대한 응답 시간. |
| $I_{618}/I_{546}$ | 618 nm 및 546 nm에서의 형광 강도 비율, 온도 감지에 사용됨. |
| $p$ | p-값, 실험 결과의 유의성을 결정하는 데 사용되는 통계적 척도. |
| $V/V_0$ | 정규화된 종양 부피, 초기 부피에 대한 종양 부피를 나타냄. |
| $\sigma$ | 표준 편차, 값 집합의 변동 또는 분산 정도를 나타내는 척도. |
문제 정의 및 제약 조건
핵심 문제 공식화 및 딜레마
본 논문이 다루는 근본적인 문제는 효과적이고 최소 침습적인 암 테라노스틱스(진단 및 치료를 결합한 접근 방식)에 대한 절실한 필요성에서 비롯된다. 현재의 방법들은 임상 적용을 저해하는 상당한 한계에 직면해 있다.
입력/현재 상태는 여러 가지 단점으로 특징지을 수 있다:
1. 제한된 광 투과 깊이 및 전신 독성: 종종 나노물질 기반인 전통적인 광 테라노스틱스 제제는 산란 및 흡수로 인해 조직 내 광 투과 깊이가 본질적으로 제한적(일반적으로 10mm 미만)이다. 또한, 정상 조직 및 장기에 대한 비특이적 축적은 전신 독성을 유발한다.
2. 광섬유의 다중화 잠재력 과소평가: 광섬유는 깊숙이 위치한 종양 접근 및 국소화된 제제 봉쇄와 같은 장점을 제공하지만, 단일 플랫폼에 여러 기능을 통합할 수 있는 잠재력은 대체로 과소평가되어 왔다.
3. 기능 간 간섭 및 장치 복잡성: 이전의 광섬유 프로브는 단일 섬유당 단일 기능 구현으로 제한되거나, 여러 기능을 통합하려 할 때 기능 간 간섭으로 어려움을 겪었다. 이러한 간섭은 주로 서로 다른 기능 시약의 흡수 또는 방출 대역에서의 스펙트럼 중첩에서 발생했다. 이를 우회하기 위해 연구자들은 다중 섬유 구성을 자주 사용했지만, 이는 필연적으로 장치의 강성과 치수를 증가시켜 최소 침습적 중재 기술과의 호환성을 떨어뜨리고 조직 손상 및 치료 후 염증의 위험을 높였다.
4. 실시간 치료 피드백 부족: 기존 방법들은 치료 용량 및 효능에 대한 실시간 모니터링 기능이 부족하여 폐쇄 루프 제어 및 개인 맞춤형 정밀 의학을 방해한다.
바람직한 최종 상태(출력/목표 상태)는 다음과 같은 기능을 갖춘 단일의 컴팩트한 다기능 광섬유 테라노스틱 프로브이다:
1. 폐쇄 루프 종양 광열 치료(PTT): 실시간 피드백을 위해 진단 및 치료 기능을 단일 플랫폼에 통합하는 것을 포함한다.
2. 다중 매개변수 모니터링: 프로브는 종양 미세 환경(TME)의 주요 매개변수인 pH와 온도를 동시에 모니터링할 수 있어야 한다.
3. 최소 침습적 중재: 장치는 종양 병변에 중재 절차를 통해 접근할 수 있도록 컴팩트해야 한다(예: 저자들이 달성한 440 µm 직경) 이는 확대된 절개 및 반복적인 침습적 시술을 피한다.
4. 치료 전 종양 식별: 종양 pH 기울기를 드러내어 종양 경계를 정확하게 식별한다.
5. 치료 중 열량 제어: 온도를 동시에 모니터링하여 PTT 중 열량을 정밀하게 제어한다.
6. 치료 후 효능 평가: 산성 TME의 역전을 모니터링하여 치료 효능을 신속하게 평가한다.
7. 광 투과 및 독성 문제 극복: 나노물질 기반 전략과 관련된 광 투과 깊이 및 전신 독성의 한계를 해결한다.
본 논문이 연결하고자 하는 정확한 누락된 연결고리 또는 수학적 격차는 기능 간 간섭 없이 여러 테라노스틱 기능을 동시에 수행할 수 있는(pH 감지, 온도 감지, 광열 치료) 견고한 단일 섬유 플랫폼의 개발이며, 동시에 실시간 피드백을 제공하는 것이다. 핵심 수학적/설계 문제는 여러 기능성 시약(pH 지시약, 온도 지시약, 광열 시약)을 선택하고 공동 고정하여, 단일 섬유에서 파장 분할 다중화(WDM)를 허용할 만큼 여기 및 방출 스펙트럼이 충분히 분리되도록 하는 것이다. 이는 이전의 단일 섬유 다중화 시도를 괴롭혔던 스펙트럼 중첩 문제를 효과적으로 제거하면서, 특정 파장에 의해 온디맨드로 개별 기능이 활성화될 수 있도록 한다. 본 논문의 해결책은 HPTS-IP, LnMOF, ICG를 신중하게 선택하는 것으로, 이들의 흡수 대역(HPTS-IP의 경우 405/450 nm, LnMOF의 경우 295 nm, ICG의 경우 790 nm)이 중첩되지 않아 WDM을 가능하게 한다.
이전 연구자들이 갇혀 있던 고통스러운 절충 또는 딜레마는 기능적 다중화와 장치 단순성/성능 사이의 내재적 충돌이다. 여러 기능을 달성하기 위해 연구자들은 다음 중 하나를 선택해야 했다:
* 장치 복잡성 증가: 여러 개의 섬유를 사용하여 부피가 크고 강성이 높은 장치를 만들었으며, 이는 최소 침습적 시술에 부적합하고 환자 위험을 증가시켰다.
* 기능 무결성 손상: 단일 섬유에 여러 시약을 통합하려 했으나, 스펙트럼 중첩으로 인한 심각한 기능 간 간섭에 직면하여 다기능성이 신뢰할 수 없거나 부정확하게 되었다. 이는 한 측면(예: 기능 추가)을 개선하면 다른 측면(예: 신호 무결성 또는 장치 크기)이 직접적으로 손상됨을 의미했다.
제약 조건 및 실패 모드
다기능 광섬유 테라노스틱 프로브 개발 문제는 저자들이 직면한 여러 가혹하고 현실적인 장벽으로 인해 매우 어렵다:
-
물리적 제약:
- 제한된 광 투과 깊이: 생체 조직 내 빛의 고유한 산란 및 흡수는 투과 깊이를 심각하게 제한하며, 일반적으로 10mm 미만이다. 이는 광열 치료에서 깊숙이 위치한 종양 치료를 어렵게 만든다.
- 전신 독성: 테라노스틱 나노물질의 정상 조직 및 장기에 대한 비특이적 축적은 바람직하지 않은 전신 독성을 유발하며, 이는 임상 적용의 주요 장애물이다.
- 장치 강성 및 치수: 최소 침습적 시술을 위해서는 프로브가 유연하고 컴팩트해야 한다. 다중 섬유 설계는 강성과 치수를 증가시켜 중재 기술과의 호환성을 떨어뜨리고 조직 손상 위험을 높인다.
- 테이퍼진 섬유 설계의 한계: 테이퍼진 광섬유의 기하학적 구조는 매우 중요하다. 과도하게 짧은 테이퍼는 빛 누출 위험을 높이고 신호 대 잡음비(SNR)를 저하시키는 반면, 너무 긴 테이퍼는 국소화된 감지 및 치료에 부적합하다. 팁 직경은 에반센트 필드 강도(따라서 형광 여기/수집 효율)와 지시약 고정에 사용 가능한 표면적 모두에 영향을 미치므로 신중한 최적화가 필요하다(예: 100 µm가 최적으로 발견됨).
- 하이드로겔 필름 무결성: 기능성 시약을 캡슐화하는 데 사용되는 졸-겔 매트릭스는 안정적이고 생체 적합해야 한다. 순수한 테트라에틸 오르토실리케이트(TEOS) 필름은 심각한 균열이 발생하기 쉬워 필름 균일성이 낮고 용출률이 높아 센서 안정성과 생체 적합성을 저해한다. GLYMO와 같은 공동 전구체 및 Triton X-100과 같은 계면활성제의 첨가가 이를 완화하는 데 필요하다.
-
데이터 기반 및 성능 제약:
- 기능 간 간섭: 단일 섬유에서의 다중화에 대한 주요 과제는 서로 다른 기능성 시약(pH 지시약, 온도 지시약, 광열 시약)의 흡수 및 방출 대역 간의 스펙트럼 중첩을 방지하는 것이다. 이러한 중첩은 부정확한 판독을 유발하고 서로 다른 기능에서 오는 신호를 구별할 수 없게 만든다.
- 실시간 지연 요구 사항: 폐쇄 루프 치료 및 실시간 모니터링을 위해서는 센서가 충분히 빠른 응답 시간을 가져야 한다. 본 논문은 pH 감지 응답 시간 3.2초(pH 증가) 및 12.8초(pH 감소), 온도 감지 응답 시간 2.0초(온도 증가) 및 0.6초(온도 감소)를 보고하며, 이는 생체 내 모니터링에 허용 가능한 것으로 간주된다.
- 센서 안정성 및 신뢰성: 기능성 시약은 생리적 환경에서 시간이 지남에 따라 섬유 표면에서 크게 용출되지 않고 안정적으로 유지되어야 한다. 용출 테스트 결과, 형광 강도의 감소가 최소화되어(72시간 동안 HPTS-IP의 경우 1.6%, LnMOF의 경우 3.5%) 안정성이 우수함을 나타냈다.
- 생리적 요인으로부터의 간섭: 복잡한 생리적 환경에 존재하는 다양한 간섭 물질, 광표백, 지시약 농도 변화, 섬유 형태 변화에 대해 감지 성능이 견고해야 한다. 비율 형광 프로브 사용 및 신중한 시약 선택이 이러한 문제를 완화하는 데 도움이 된다.
- 조직 자가 형광: 조직의 내인성 형광은 프로브의 신호와 간섭하여 감지 정확도 및 특이도를 저하시킬 수 있다. 지시약 농도가 높은 에반센트 필드의 얕은 투과 깊이는 높은 SNR을 유지하는 데 도움이 된다.
- 정확한 열량 제어: 광열 치료 중, 주변 정상 조직에 과도한 열을 발생시키지 않고 효과적인 열량을 전달하는 것이 중요하다. 과열은 조직 손상, 혈관 붕괴, 혈류 관류 장애를 유발할 수 있다. 이를 위해서는 정확한 실시간 온도 모니터링이 필수적이다.
이 접근 방식은 왜
선택의 필연성
저자들이 파장 분할 다중화(WDM) 기술을 활용한 단일 광섬유 다기능 통합 전략을 추구하기로 결정한 것은 단순한 개선이 아니라 기존 접근 방식의 내재적 한계에 의해 추진된 필연적인 선택이었다. 본 논문은 전통적인 "최첨단"(SOTA) 방법이 부족했던 정확한 순간을 명확하게 식별한다: "최근의 발전에도 불구하고, 광섬유 프로브의 다중화 잠재력은 여전히 저평가되고 있다. 현재 연구는 단일 기능당 단일 광섬유 구현에 국한되거나, 주로 사용되는 기능성 시약 간의 흡수 또는 방출 대역에서의 스펙트럼 중첩에서 발생하는 기능 간 누화를 겪고 있다." 이러한 스펙트럼 중첩 문제는 다중 매개변수 모니터링 또는 통합 치료진단(theranostics)을 달성하기 위해 종종 다중 광섬유 구성이 필요함을 의미했다. 그러나 이러한 설정은 "필연적으로 장치의 경직성과 치수를 증가시켜, 중재 시술과의 호환성을 감소시키는 동시에 조직 손상 및 치료 후 염증의 위험을 높인다." 이러한 결정적인 단점들—실시간 피드백 부족, 침습성, 기능적 누화—은 패러다임 전환을 요구했다. WDM 기반 단일 광섬유 접근 방식은 스펙트럼 간섭 없이 단일의 소형 플랫폼에서 다중 기능을 가능하게 함으로써 이러한 근본적인 문제를 극복하는 유일하게 실행 가능한 해결책으로 부상했다.
비교 우위
단순한 성능 지표를 넘어서, 이 방법은 주로 구조 설계를 통해 심오한 질적 우수성을 제공한다. 핵심적인 장점은 파장 분할 다중화(WDM)를 사용하여 단일 광섬유에 다중 기능(pH 감지, 온도 모니터링, 광열 치료)을 통합할 수 있다는 점에 있다. 이러한 구조적 혁신은 스펙트럼 중첩으로 인해 신호 무결성이 저하되었던 이전의 다중 시약 시스템에서 중요한 문제였던 기능 간 누화를 본질적으로 최소화한다. "겹치지 않는 흡수 대역"을 가진 시약(HPTS-IP, LnMOF, ICG)을 신중하게 선택함으로써, 프로브는 각 매개변수의 정확하고 신뢰할 수 있는 측정을 보장한다.
더욱이, pH 및 온도 감지를 위해 선택된 비율 기반 형광 프로브는 중요한 질적 이점을 제공한다. 이 비율 기반 검출 전략은 "광표백, 지시약 농도 변화, 광섬유 형태 변화가 감지 결과에 미치는 간섭을 완화하여 정확하고 신뢰할 수 있는 신호 획득을 촉진한다." 이는 노이즈와 환경 변동에 매우 민감한 강도 기반 감지에 비해 상당한 개선이다. 소형의 단일 광섬유 설계는 또한 다중 광섬유 번들에 비해 물리적 공간과 경직성을 대폭 줄여, 최소 침습적 중재 시술에 압도적으로 우수하다. 또한 치료진단 시약을 국소화하여 유리 나노물질과 관련된 전신 독성을 효과적으로 완화한다.
제약 조건과의 정렬
선택된 방법은 고급 치료진단 응용 분야의 엄격한 제약 조건과 완벽하게 일치한다.
- 최소 침습성: 단일의 유연한 광섬유(직경 = 440 µm, 끝 직경 = 100 µm)의 사용은 "중재 시술을 통한 종양 병변 접근"을 가능하게 하여, 다중 광섬유 또는 더 큰 프로브 설계에 비해 침습성을 대폭 감소시킨다. 이는 조직 손상 및 치료 후 염증을 최소화하는 제약 조건을 직접적으로 해결한다.
- 실시간 피드백 및 폐쇄 루프 치료: pH 및 온도 지시계와 광열제를 단일 플랫폼에 통합하는 것은 "실시간 피드백을 통한 폐쇄 루프 종양 광열 치료"를 가능하게 한다. 이는 프로브가 치료 전 종양 식별(pH 기울기 이용), 치료 중 용량 제어(PTT 중 온도 모니터링 이용), 치료 후 효능 평가(TME pH 역전 이용)를 수행할 수 있음을 의미하며, 동적이고 적응적인 치료에 대한 중요한 요구를 충족시킨다.
- 다중 매개변수 모니터링: 파장 분할 다중화 방식은 단일 광섬유에서 광열 치료와 함께 pH 및 온도에 대한 동시 모니터링을 허용한다. 이는 복잡한 생물학적 환경에서 포괄적인 다중 매개변수 평가 요구 사항을 직접적으로 충족시킨다.
- 전신 독성 감소 및 심부 조직 접근: 광열진단 시약을 광섬유 표면에 고정함으로써, 이 접근 방식은 "국소화된 구속을 통해 표적 외 독성을 효과적으로 완화한다." 또한, 광섬유는 "최소 손실로 종단 간 빛 전달"을 촉진하여 "심부 종양"의 감지 및 치료를 가능하게 함으로써, 전통적인 광열진단 시약의 제한된 광 투과 깊이를 극복한다.
대안의 기각
본 논문은 폐쇄 루프, 다기능 종양 치료진단이라는 특정 문제에 대한 근본적인 한계에 기반하여 여러 대안적 접근 방식을 암묵적 및 명시적으로 기각한다.
- 단일 기능당 단일 광섬유 구현: 이러한 방식은 다중 매개변수 모니터링 및 치료를 위해 여러 개의 광섬유를 필요로 하여 "절개 부위 확대, 반복적인 침습 시술" 및 장치 경직성 증가로 이어지기 때문에 불충분한 것으로 간주되었다. 목표는 파편화된 기능이 아닌 통합된 치료진단이었다.
- 다중 광섬유 구성: 다중화를 제공함에도 불구하고, 이러한 방식은 "장치 경직성 및 치수 증가"와 같은 내재적인 물리적 한계로 인해 기각되었으며, 이는 최소 침습적 중재 시술과의 호환성을 저해하고 조직 손상 위험을 높인다.
- 기능 간 누화를 겪는 접근 방식: 기능성 시약이 "흡수 또는 방출 대역의 스펙트럼 중첩"을 갖는 방법은 문제점으로 명시적으로 식별되었다. 겹치지 않는 대역을 가진 시약의 신중한 선택과 WDM 전략은 이 실패 지점을 직접적으로 해결하여 신호 무결성을 보장한다.
- 나노물질 의존적 전략 (광섬유 통합 없음): 본 논문의 결론은 "나노물질 의존적 전략"과 비교하여, 이 광섬유 접근 방식이 "광 투과 깊이 및 전신 독성의 한계를 효과적으로 해결한다"고 강조한다. 이는 유리 부동 또는 비광섬유 통합 나노물질에만 의존하는 것이 효과적인 종양 광열 치료에 필요한 심부 조직 접근 및 국소화된 비독성 전달을 제공하지 못할 것임을 시사한다.
수학 및 논리 메커니즘
마스터 방정식
본 테라노스틱 프로브의 감지 능력의 핵심에는 볼츠만 시그모이드 모델이 자리 잡고 있으며, 이는 비율 형광 신호를 pH 및 온도와 같은 의미 있는 생리학적 매개변수로 변환하는 기본 변환 로직으로 작용한다. 광열 치료 구성 요소는 직접적인 빛-열 변환을 포함하지만, 그 정밀한 제어 및 모니터링은 이러한 감지 메커니즘이 제공하는 정확한 판독값에 전적으로 의존한다.
본 논문에서 pH 및 온도 감지에 모두 사용되는 볼츠만 방정식의 일반적인 형태는 다음과 같이 표현될 수 있다:
$$ y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}} $$
여기서:
- pH 감지 (그림 2f에서 파생):
$$
R_{pH} = 0.97 - \frac{0.78}{1 + e^{(pH - 7.07)/0.87}}
$$
여기서 $y$는 형광 강도 비율 $R_{pH} = I_{520}(450nm) / I_{520}(405nm)$이며, $x$는 pH 값이다.
- 온도 감지 (그림 3g에서 파생):
$$ R_{Temp} = 1.55 - \frac{0.81}{1 + e^{(Temp - 65.74)/10.71}} $$
여기서 $y$는 형광 강도 비율 $R_{Temp} = I_{618} / I_{546}$이며, $x$는 섭씨 단위의 온도 값이다.
이러한 방정식들은 프로브가 수신하는 광학 신호를 정량적으로 해석할 수 있게 하는 핵심 수학적 엔진으로서, 폐쇄 루프 테라노스틱스를 위한 중요한 피드백을 제공한다.
용어별 분석
각 구성 요소의 역할을 이해하기 위해 일반적인 볼츠만 방정식 $y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}}$을 분해해 보자:
-
$y$ (형광 강도 비율, $R_{pH}$ 또는 $R_{Temp}$)
- 수학적 정의: 이는 종속 변수로서, 형광 강도의 무차원 비율을 나타낸다. pH 감지의 경우, 450nm에서 여기되었을 때 520nm에서의 방출 강도와 405nm에서 여기되었을 때의 강도의 비율($I_{520}(450nm) / I_{520}(405nm)$)이다. 온도 감지의 경우, 295nm 여기 하에서 618nm와 546nm에서의 방출 강도의 비율($I_{618} / I_{546}$)이다.
- 물리적/논리적 역할: 이 항은 광학 측정 시스템의 직접적인 출력이다. 비율을 사용함으로써, 연구자들은 광표백, 지시약 농도의 변화, 섬유 형태의 변화와 같은 일반적인 오류 원인을 현명하게 완화한다. 이러한 정규화는 신호를 견고하고 신뢰할 수 있게 만들며, 대상 매개변수에 따라 예측 가능하게 변화하는 주요 관측치 역할을 한다.
- 비율/뺄셈/나눗셈을 사용하는 이유: 비율은 비율 감지에서 자체 참조하고 공통 모드 노이즈를 상쇄하는 표준 기술이다. 뺄셈과 나눗셈을 포함하는 전반적인 시그모이드 형태는 지시약이 연속 변수에 반응하여 두 상태(예: 양성자화/탈양성자화 또는 다른 에너지 전달 상태) 사이를 전환하고 양쪽 극한에서 포화되는 화학적 또는 물리적 과정에서 자연스럽게 발생한다.
-
$x$ (생리학적 매개변수, $pH$ 또는 $Temp$)
- 수학적 정의: 이는 측정되는 환경 조건(pH 또는 섭씨 온도)을 나타내는 독립 변수이다.
- 물리적/논리적 역할: 이는 테라노스틱 프로브가 감지하고 모니터링하도록 설계된 실제 물리적 양이다. 이는 시스템이 결정하고자 하는 "참값"이다.
- 독립 변수인 이유: 이는 원인이고, $y$는 결과이다. 보정 과정은 이 입력과 측정된 출력 비율 간의 함수적 관계를 확립한다.
-
$C_1$ (상부 점근선)
- 수학적 정의: $x$가 양의 무한대로 접근할 때 시그모이드 곡선의 상부 평탄부를 나타내는 상수 계수이다(이 특정 감소 시그모이드 형태의 경우).
- 물리적/논리적 역할: pH의 경우, $C_1 = 0.97$은 HPTS-IP 지시약이 주로 양성자화 상태 중 하나(예: 고pH에서 완전히 탈양성자화된 상태)에 있을 때 달성되는 최대 형광 비율을 나타낸다. 온도의 경우, $C_1 = 1.55$는 고온에서 LnMOF의 최대 비율을 나타낸다. 이는 센서의 동적 범위의 한 극한을 정의하며, $x$의 추가적인 증가는 지시약의 상태를 더 이상 크게 변경하지 않는 포화 지점을 나타낸다.
- 상수인 이유: 이는 지시약의 최대 가능한 응답을 반영하는 점근값으로, 평형이 거의 완전히 한쪽으로 이동한 극한 조건에서의 응답을 나타낸다.
-
$C_2$ (범위 스케일링 계수)
- 수학적 정의: 시그모이드 전이의 크기를 스케일링하는 상수 계수이다. 이는 하부 점근선에서 상부 점근선까지의 $y$의 총 변화량을 나타낸다.
- 물리적/논리적 역할: pH의 경우, $C_2 = 0.78$은 pH가 민감한 범위에 걸쳐 변함에 따라 형광 비율 변화의 전반적인 범위를 결정한다. 온도의 경우, $C_2 = 0.81$은 온도의 경우에도 동일한 역할을 한다. 이 항은 본질적으로 시그모이드 단계의 "높이"를 정의하며, 센서 응답의 총 동적 범위를 나타낸다.
- 상수인 이유: 이는 지시약과 환경과의 상호작용의 특성으로, 비율 신호의 최대 가능한 변화를 반영한다.
-
$C_3$ (중간점 또는 전이 중심)
- 수학적 정의: 응답이 점근 한계의 중간 지점(또는 기울기가 최대인 지점)에 있는 $x$ 값을 나타내는 상수 계수이다.
- 물리적/논리적 역할: pH의 경우, $C_3 = 7.07$은 HPTS-IP 지시약이 가장 민감한 pH 값으로, 종종 pKa에 해당한다. 온도의 경우, $C_3 = 65.74$ °C는 LnMOF의 에너지 전달 메커니즘이 가장 가파른 변화를 보이는 온도를 나타낸다. 이 매개변수는 센서의 작동 범위와 최적의 민감도를 정의하는 데 중요하다.
- 상수인 이유: 이는 지시약으로 모니터링되는 화학적 또는 물리적 과정의 고유한 속성이다.
-
$C_4$ (기울기 매개변수)
- 수학적 정의: 시그모이드 곡선의 최대 기울기에 반비례하는 상수 계수이다. $C_4$의 절대값이 작을수록 곡선이 더 가파르다.
- 물리적/논리적 역할: pH의 경우, $C_4 = 0.87$은 pH 응답 곡선의 가파른 정도를 정량화한다. 온도의 경우, $C_4 = 10.71$은 온도의 경우에도 동일한 역할을 한다. 이 매개변수는 센서의 민감도와 직접적으로 관련된다. 즉, $C_4$가 작을수록 중간점 $C_3$ 주변에서 $x$의 주어진 변화에 대해 형광 비율의 변화가 더 빠르다.
- 상수인 이유: 이는 지시약 전이의 고유한 반응성과 협동성을 반영한다.
-
$e$ (오일러 수)
- 수학적 정의: 자연 로그의 밑인 수학 상수이며, 약 2.71828이다.
- 물리적/논리적 역할: 이는 시그모이드 전이를 모델링하는 데 사용되는 지수 함수에 필수적이다. 이러한 전이는 종종 통계 역학 또는 화학 평형 방정식(pH의 경우 Henderson-Hasselbalch 방정식, 에너지 상태의 경우 볼츠만 분포)에서 발생하며, 여기서 상태의 확률은 구동력에 따라 지수적으로 변한다.
- 지수 함수인 이유: 지수 항은 시스템이 평형에 접근함에 따라 많은 물리적 및 화학적 시스템에서 관찰되는 비선형적이고 포화되는 거동을 자연스럽게 설명한다.
-
지수 $(x - C_3)/C_4$
- 수학적 정의: 지수 함수의 인수이다.
- 물리적/논리적 역할: 이 항은 현재 입력 $x$와 중간점 $C_3$ 간의 차이를 기울기 매개변수 $C_4$로 정규화한다. 이는 입력 값을 지수적 감소 또는 성장에 맞게 효과적으로 스케일링하여 시스템이 반전이 지점에서 얼마나 떨어져 있는지를 결정한다.
-
$(1 + e^{(x - C_3)/C_4})$로 나누기
- 수학적 정의: 이 특정 형태는 종종 로지스틱 함수 또는 페르미-디락 분포라고도 불리는 시그모이드 형태의 핵심이다.
- 물리적/논리적 역할: 이 항은 $x$가 변함에 따라 출력 $y$가 두 점근선 사이를 부드럽게 전환하도록 보장한다. 이는 지시약의 상태가 한 극한에서 다른 극한으로 점진적으로 전환되는 것을 모델링한다.
-
뺄셈 $C_1 - \frac{C_2}{...}$
- 수학적 정의: 이 연산은 상부 점근선과 스케일링된 시그모이드 항을 결합한다.
- 물리적/논리적 역할: 논문에서 사용된 특정 형태의 경우, 이 뺄셈은 $C_2$가 양수이면 감소하는 시그모이드를 생성한다. 이는 $x$가 증가함에 따라 비율 $y$가 높게 시작하여 $C_1 - C_2$로 감소함을 의미한다. 그러나 그래프(그림 2f 및 3g)는 pH/온도가 증가함에 따라 증가하는 비율을 보여준다. 이는 연구자들의 적합 방정식 $y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}}$이 실제로는 $C_1$이 상부 점근선이고 $C_1 - C_2$가 하부 점근선인 증가하는 시그모이드임을 시사한다. $x \to -\infty$일 때, $e^{(x - C_3)/C_4} \to 0$이므로, $y \to C_1 - C_2$이다. $x \to +\infty$일 때, $e^{(x - C_3)/C_4} \to \infty$이므로, $y \to C_1$이다. 이는 그림과 일치한다. 뺄셈은 곡선의 방향과 범위를 정의하는 데 필수적이다.
단계별 흐름
테라노스틱 프로브를 정교하고 소형화된 데이터 처리 조립 라인으로 상상해 보자. 각 단계는 원시 광학 신호를 실행 가능한 생리학적 통찰력으로 변환한다.
-
광 입력 및 파장 선택: 프로세스는 조절 가능한 광원에서 Y형 광섬유로 들어가는 빛으로 시작된다. 원하는 측정에 따라, 마치 도구 상자에서 도구를 선택하는 것처럼 특정 파장이 선택된다. pH 감지의 경우, 시스템은 405nm와 450nm 여기 광 사이를 빠르게 전환한다. 온도 감지의 경우, 295nm 여기 파장이 사용된다. 이러한 파장 분할 다중화(WDM)는 프로브의 기능을 결정하는 초기 "스위치"이다.
-
에반센트 필드 상호작용: 선택된 빛은 섬유를 따라 테이퍼진 끝으로 이동하여 "에반센트 필드"로 주변 하이드로겔 매트릭스로 빠져나간다. 이 필드는 미세한 그물처럼 작용하여 공동 고정된 지시약 분자(pH의 경우 HPTS-IP, 온도의 경우 LnMOF)와 직접 상호작용한다. 지시약은 이 빛을 흡수하여 에너지를 얻는다.
-
형광 방출: 여기되면, 에너지를 얻은 지시약 분자는 형광을 방출한다. 이 방출되는 빛의 특성은 국소 환경에 민감하다. pH의 경우, HPTS-IP는 520nm에서 형광을 방출하지만, 405nm 또는 450nm에서 여기되었는지에 따라 이 파장에서의 강도가 달라지며, 이는 국소 양성자화 상태를 반영한다. 온도의 경우, LnMOF는 두 개의 서로 다른 파장인 546nm와 618nm에서 형광을 방출하며, 에너지 전달 역학으로 인해 국소 온도에 따라 상대 강도가 변한다.
-
신호 수집: 방출된 형광은 다시 동일한 광섬유로 효율적으로 수집되어(빛을 빨아들이는 진공 청소기처럼) 조직에서 멀리 안내된다.
-
스펙트럼 분석: 수집된 빛은 형광 스펙트럼 분석기(FSA)로 이동한다. 이 장치는 "빛 분류기" 역할을 하여 관련 방출 파장에서의 형광 강도를 정확하게 측정한다. pH의 경우, $I_{520}(450nm)$와 $I_{520}(405nm)$를 측정한다. 온도의 경우, $I_{618}$와 $I_{546}$을 측정한다.
-
비율 계산: 계산 장치는 이러한 원시 강도 측정값에서 무차원 비율을 계산한다. pH의 경우, $R_{pH} = I_{520}(450nm) / I_{520}(405nm)$를 계산한다. 온도의 경우, $R_{Temp} = I_{618} / I_{546}$를 계산한다. 이 비율은 수학적 엔진에 공급될 표준화된 "데이터 포인트"이다.
-
볼츠만 모델 변환: 이 계산된 비율($R_{pH}$ 또는 $R_{Temp}$)은 사전 보정된 볼츠만 방정식에 입력된다. 이 방정식은 "디코더" 역할을 하여 비선형 변환을 수행하고, 보정 곡선을 효과적으로 반전시켜 실제 생리학적 매개변수를 얻는다. 예를 들어, pH 볼츠만 방정식에 $R_{pH}$가 입력되면 해당 pH 값을 출력한다. 마찬가지로, $R_{Temp}$는 온도를 산출한다.
-
실시간 피드백 및 조치: 파생된 pH 및 온도 값은 실시간으로 표시된다. 이러한 정확한 판독값은 중요한 피드백 역할을 한다. 광열 치료(PTT) 중, 온도 판독값은 "열 용량 제어"를 가능하게 하여, 작업자가 808nm 펌프 레이저 출력을 조정하여 목표 온도(예: 섬유 끝에서 65°C를 유지하여 종양 가장자리에서 45°C를 보장)를 유지할 수 있도록 한다. 치료 후, pH 모니터링은 산성 종양 미세 환경의 역전을 추적하여 효능을 평가한다. 이 폐쇄 루프 시스템은 치료가 전달될 뿐만 아니라 환자의 실시간 생리학적 상태에 기반하여 지속적으로 최적화되도록 보장한다.
최적화 동역학
이 테라노스틱 프로브의 "최적화 동역학"은 주로 초기 보정과 견고한 실시간 피드백 제어를 위한 고유한 설계에 있으며, 기계 학습의 의미에서의 지속적인 반복 학습보다는 이러한 특징에 기반한다.
-
초기 "학습"으로서의 보정:
- 데이터 획득: 임상 적용 전에, 프로브는 엄격한 보정 과정을 거친다. 여기에는 제어된 실험실 환경에서 프로브를 다양한 알려진 pH 값(예: pH 4.0 ~ 9.0) 및 온도(예: 30°C ~ 100°C)에 노출시키는 것이 포함된다. 각 알려진 지점에서 해당 비율 형광 신호가 측정된다.
- 모델 적합: 수집된 이 데이터 포인트(알려진 매개변수 $x$ 대 측정된 비율 $y$)는 볼츠만 시그모이드 모델을 "훈련"하거나 "적합"하는 데 사용된다. 이 적합 과정은 비선형 회귀의 한 형태로, 볼츠만 방정식의 계수($C_1, C_2, C_3, C_4$)가 각 알려진 입력에 대해 모델이 예측한 비율과 실험적으로 관찰된 비율 간의 차이(예: 제곱 오차의 합)를 최소화하도록 반복적으로 조정된다. 이는 센서의 응답 곡선을 가장 잘 설명하는 최적의 매개변수 집합을 찾기 위해 "손실 지형"을 탐색하는 것과 유사하다. 논문은 높은 $R^2$ 값(pH의 경우 0.997, 온도의 경우 0.997)을 보고하며, 이는 뛰어난 적합성과 따라서 명확한 최소값을 가진 잘 정의된 손실 지형을 나타낸다.
- 매개변수 고정: 이 계수들이 결정되면 고정된다. 센서는 작동 중에 이러한 매개변수를 "학습"하거나 업데이트하지 않는다. 이 일회성 보정은 센서의 "지식" 기반을 설정한다.
-
암시적 최적화로서의 비율 설계의 견고성:
- 비율 감지 선택은 중요한 설계 "최적화"이다. 두 형광 강도의 비율(pH의 경우 다른 여기 파장 또는 온도의 경우 다른 방출 파장)을 취함으로써, 시스템은 본질적으로 많은 일반적인 노이즈 소스를 상쇄한다. 여기에는 여기 광 강도의 변동, 지시약의 광표백, 지시약 농도의 변화, 심지어 광섬유의 광학적 특성 또는 커플링 효율의 사소한 변화도 포함된다.
- 이 메커니즘은 신호 대 잡음비(SNR)가 높게 유지되고 센서 출력이 안정적이고 신뢰할 수 있도록 보장하여, 명시적인 알고리즘 업데이트 없이 측정 품질을 효과적으로 "최적화"한다. 안정성 테스트(그림 2g,h,i,j 및 그림 3j,k,l,n)는 최소 표준 편차와 누출을 보여주며 이러한 견고성을 확인한다.
-
치료 최적화를 위한 폐쇄 루프 피드백:
- 실제 광열 치료 중, 시스템은 폐쇄 루프 제어 메커니즘으로 작동한다. 센서는 지속적으로 실시간 온도 및 pH 판독값을 제공한다.
- 이러한 판독값은 센서의 내부 수학적 모델을 업데이트하는 데 사용되지 않고, 외부 치료 입력을 조정하는 데 사용된다. 예를 들어, 모니터링된 온도가 목표 열 용량에서 벗어나면, 펌프 레이저 출력(치료 입력)이 그에 따라 조정된다. 이는 고전적인 피드백 루프이다: 감지 (온도/pH) $\rightarrow$ 평가 (목표 대비) $\rightarrow$ 조치 (레이저 출력 조정).
- 실시간 센서 데이터를 기반으로 치료 입력을 반복적으로 조정하는 것은 원하는 결과를 달성하기 위해 치료 자체를 최적화하는 방법이다(예: 종양 가장자리에서 45°C를 보장하기 위해 섬유 끝에서 종양 온도를 65°C로 유지). 이 시스템은 지속적인 모니터링 및 조정을 통해 목표 치료 상태로 수렴하여, 치료를 정확하고 적응적으로 만든다.
본질적으로, 수학적 엔진은 보정 중에 한 번 특성 응답을 "학습"한 다음, 이 학습된 함수를 안정적으로 적용한다. 치료 중 전체 시스템의 "최적화"는 센서의 정확하고 안정적인 측정을 활용하여 치료 개입을 제어하는 견고한 실시간 피드백 루프를 통해 달성된다.
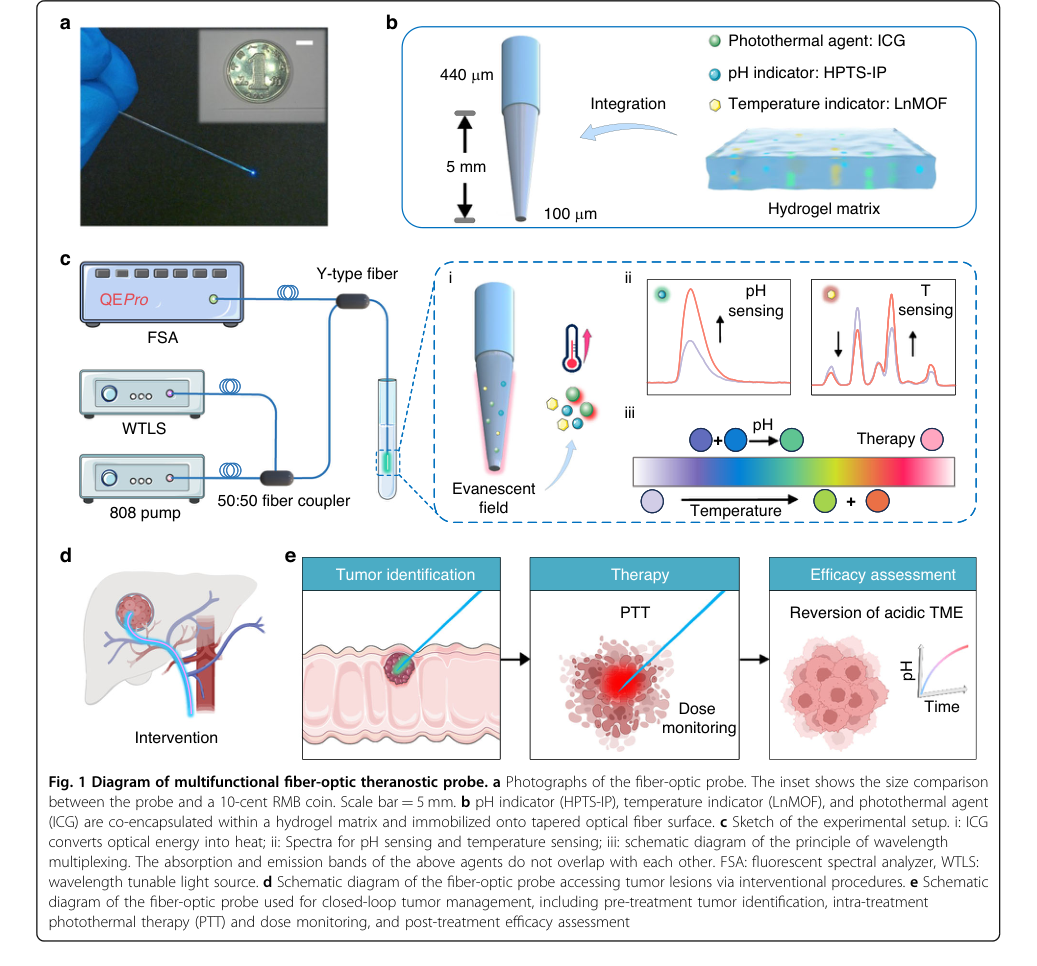 Figure 1. Diagram of multifunctional fiber-optic theranostic probe. a Photographs of the fiber-optic probe. The inset shows the size comparison between the probe and a 10-cent RMB coin. Scale bar = 5 mm. b pH indicator (HPTS-IP), temperature indicator (LnMOF), and photothermal agent (ICG) are co-encapsulated within a hydrogel matrix and immobilized onto tapered optical fiber surface. c Sketch of the experimental setup. i: ICG converts optical energy into heat; ii: Spectra for pH sensing and temperature sensing; iii: schematic diagram of the principle of wavelength multiplexing. The absorption and emission bands of the above agents do not overlap with each other. FSA: fluorescent spectral analyzer, WTLS: wavelength tunable light source. d Schematic diagram of the fiber-optic probe accessing tumor lesions via interventional procedures. e Schematic diagram of the fiber-optic probe used for closed-loop tumor management, including pre-treatment tumor identification, intra-treatment photothermal therapy (PTT) and dose monitoring, and post-treatment efficacy assessment
Figure 1. Diagram of multifunctional fiber-optic theranostic probe. a Photographs of the fiber-optic probe. The inset shows the size comparison between the probe and a 10-cent RMB coin. Scale bar = 5 mm. b pH indicator (HPTS-IP), temperature indicator (LnMOF), and photothermal agent (ICG) are co-encapsulated within a hydrogel matrix and immobilized onto tapered optical fiber surface. c Sketch of the experimental setup. i: ICG converts optical energy into heat; ii: Spectra for pH sensing and temperature sensing; iii: schematic diagram of the principle of wavelength multiplexing. The absorption and emission bands of the above agents do not overlap with each other. FSA: fluorescent spectral analyzer, WTLS: wavelength tunable light source. d Schematic diagram of the fiber-optic probe accessing tumor lesions via interventional procedures. e Schematic diagram of the fiber-optic probe used for closed-loop tumor management, including pre-treatment tumor identification, intra-treatment photothermal therapy (PTT) and dose monitoring, and post-treatment efficacy assessment
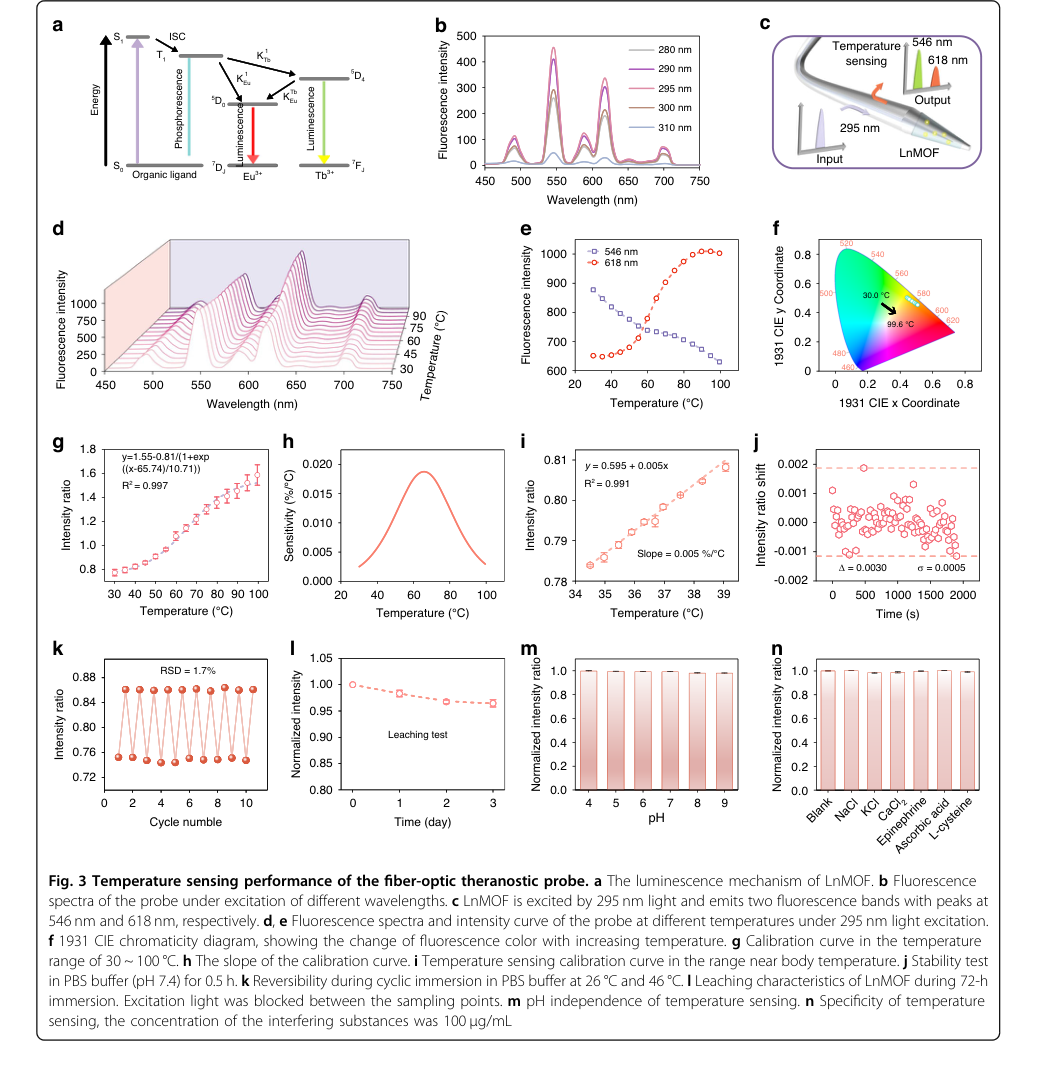 Figure 3. Temperature sensing performance of the fiber-optic theranostic probe. a The luminescence mechanism of LnMOF. b Fluorescence spectra of the probe under excitation of different wavelengths. c LnMOF is excited by 295 nm light and emits two fluorescence bands with peaks at 546 nm and 618 nm, respectively. d, e Fluorescence spectra and intensity curve of the probe at different temperatures under 295 nm light excitation. f 1931 CIE chromaticity diagram, showing the change of fluorescence color with increasing temperature. g Calibration curve in the temperature range of 30 ~ 100 °C. h The slope of the calibration curve. i Temperature sensing calibration curve in the range near body temperature. j Stability test in PBS buffer (pH 7.4) for 0.5 h. k Reversibility during cyclic immersion in PBS buffer at 26 °C and 46 °C. l Leaching characteristics of LnMOF during 72-h immersion. Excitation light was blocked between the sampling points. m pH independence of temperature sensing. n Specificity of temperature sensing, the concentration of the interfering substances was 100 μg/mL
Figure 3. Temperature sensing performance of the fiber-optic theranostic probe. a The luminescence mechanism of LnMOF. b Fluorescence spectra of the probe under excitation of different wavelengths. c LnMOF is excited by 295 nm light and emits two fluorescence bands with peaks at 546 nm and 618 nm, respectively. d, e Fluorescence spectra and intensity curve of the probe at different temperatures under 295 nm light excitation. f 1931 CIE chromaticity diagram, showing the change of fluorescence color with increasing temperature. g Calibration curve in the temperature range of 30 ~ 100 °C. h The slope of the calibration curve. i Temperature sensing calibration curve in the range near body temperature. j Stability test in PBS buffer (pH 7.4) for 0.5 h. k Reversibility during cyclic immersion in PBS buffer at 26 °C and 46 °C. l Leaching characteristics of LnMOF during 72-h immersion. Excitation light was blocked between the sampling points. m pH independence of temperature sensing. n Specificity of temperature sensing, the concentration of the interfering substances was 100 μg/mL
결과, 한계점 및 결론
실험 설계 및 기준선
연구자들은 새로운 광섬유 테라노스틱 프로브의 다기능성과 치료 효능을 엄격하게 검증하기 위해 실험을 세심하게 설계하였다. 실험 구조의 핵심은 단일 광섬유를 사용하여 pH 감지, 온도 감지, 광열 치료(PTT)의 세 가지 고유한 기능을 수행하는 프로브의 능력을 입증하는 데 집중되었으며, 파장 분할 다중화(WDM)를 활용하여 누화를 방지하였다.
pH 감지를 위해 HPTS-IP로 기능화된 프로브는 실온에서 넓은 pH 범위(4.0-9.0)의 인산염 완충 식염수(PBS) 용액에서 테스트되었다. pH 7.4 PBS에서 150초 동안 연속적인 스펙트럼 기록을 통해 안정성이 평가되었다. pH 4.0 및 9.0 완충액에 5회 주기적으로 번갈아 담그는 방식으로 가역성이 입증되었다. pH 7.4 PBS에서 72시간 동안 용출 특성이 평가되었다. 복잡한 생물학적 환경에서의 신뢰성을 확인하기 위해 프로브의 특이성은 NaCl, KCl, CaCl₂, 에피네프린, 아스코르브산, L-cysteine과 같은 일반적인 간섭 물질에 대해 테스트되었다. 결정적으로, pH를 측정하면서 온도를 26°C에서 41°C까지 변화시키면서 온도 누화가 평가되었다.
온도 감지는 LnMOF를 활용하였으며, 넓은 범위(30-100°C)와 특히 생리학적으로 관련된 범위(34.5-39°C)에서 평가되었다. pH 7.4 PBS에서 0.5시간 동안 안정성이 테스트되었고, 26°C 및 46°C PBS에 번갈아 담그는 10회 주기를 통해 가역성이 입증되었다. 72시간 동안 용출이 모니터링되었고, pH 4.0에서 9.0까지의 완충액에서 테스트하여 pH 독립성이 확인되었다. 간섭 물질에 대한 특이성도 평가되었다.
광열 변환을 위해 ICG 기능화된 프로브는 808 nm 펌프 레이저를 사용하여 in vitro 테스트를 거쳤으며, 다양한 펌프 전력(최대 267 mW)에서 최대 온도를 측정하였다. 광열 안정성은 5회의 가열/냉각 주기를 통해 평가되었고, ICG 용출은 72시간 동안 모니터링되었다. 여기서 "희생양"은 기존 나노물질 기반 PTT 시스템에서 요구되는 높은 펌프 전력으로, 종종 1 W를 초과한다는 점이었다.
궁극적인 검증은 BALB/c 누드 마우스의 피하 대장암 이종 이식 모델을 이용한 in vivo 실험을 통해 이루어졌다. 종양은 개입 전에 약 100 mm³에 도달하도록 하였다.
- 종양 식별은 프로브를 종양 조직, 인접 정상 조직, 종양 표면, 정상 조직에 삽입하고 측정된 pH 값을 비교함으로써 엄격하게 테스트되었다.
- PTT 및 용량 모니터링은 프로브를 종양 중심에 삽입하고 15분 동안 섬유 온도 65°C를 적극적으로 유지하는 것을 포함했으며, 열 영상은 종양 가장자리가 효과적인 치료 온도인 45°C에 도달했음을 확인하였다.
- 효능 평가는 다각적이었다: 치료 후(30분 및 24시간) 종양 미세 환경(TME)에서의 실시간 pH 모니터링, 그리고 20일 동안 3일마다 종양 부피와 체중을 장기적으로 모니터링하는 것이었다. 이 맥락에서 "희생양"은 치료받지 않은 대조군 마우스였으며, 이들의 종양은 점진적인 성장을 보였고, 부피가 2000 mm³를 초과하면 안락사로 이어졌다.
- 생체 적합성은 HCT116 세포를 프로브 용출액(24시간)으로 배양하고 CCK-8 분석 및 생존/사멸 염색을 수행하여 in vitro에서 평가되었다. in vivo에서는 심장, 간, 비장, 폐, 신장의 장기 생체 적합성이 대조군과 비교하여 이식군(레이저 없는 섬유 삽입) 및 치료군 모두에서 치료 24시간 후 H&E 염색을 통해 평가되었다. 종양 조직의 조직학적 및 면역 조직 화학적 분석(Caspase-3, HIF-1α, Ki67)은 치료 24시간 후 수행되었으며, 샴 처리군(레이저 여기 없는 섬유 이식)이 비교를 위한 기준선 역할을 하였다.
증거가 입증하는 바
본 논문에서 제시된 증거는 실시간 피드백을 통한 폐쇄 루프 종양 광열 치료가 가능한 다기능 광섬유 테라노스틱 프로브의 성공적인 개발 및 기능을 명확하게 입증한다.
비중첩 여기 대역을 위한 파장 분할 다중화(WDM)의 핵심 수학적 주장은 HPTS-IP(405 nm, 450 nm), LnMOF(295 nm), ICG(790 nm)의 뚜렷한 흡수 스펙트럼에 의해 무자비하게 입증되었으며, 이는 그림 2b 및 그림 S7에 나타나 있다. 이러한 스펙트럼 분리는 요구에 따라 기능을 전환하는 핵심 메커니즘이 작동한다는 부인할 수 없는 증거이며, 이전 다중 에이전트 시스템의 중요한 한계였던 기능 간 누화를 효과적으로 제거한다.
pH 감지에 대해 프로브는 뛰어난 성능을 보였다:
- 6.0에서 8.0까지의 선형 범위 내에서 0.013 pH 단위의 높은 해상도를 달성했으며, 이는 정상 및 종양 조직의 생리학적 pH 값을 구별하는 데 중요하다. 이는 볼츠만 모델 적합(그림 2f)과 표준 편차($\sigma$)가 0.0009인 안정성 테스트(그림 2g)에서 도출되었다.
- 5회 주기 동안 0.8%의 상대 표준 편차(RSD)로 우수한 가역성이 확인되었으며(그림 2h), 일관된 성능을 나타낸다.
- HPTS-IP의 최소 용출(72시간 동안 형광 강도 1.6% 감소, 그림 2i) 및 다양한 간섭 물질에 대한 우수한 선택성(그림 2j)은 복잡한 생물학적 환경에서의 신뢰성을 더욱 검증하였다.
- 결정적으로, pH 4.0-7.0 범위에서 무시할 수 있는 온도 누화가 관찰되었으며, pH > 7.0의 경우 프로브의 통합 온도 모니터링 기능이 내장된 보상을 제공하여 정확한 pH 감지를 보장한다(그림 2k).
온도 감지 또한 강력한 성능을 보였다:
- Tb³⁺에서 Eu³⁺로의 열 강화 에너지 전달을 활용하는 비율 접근 방식(그림 3a, c)은 정밀한 모니터링을 가능하게 하였다.
- 0.3°C의 해상도가 달성되어 in vivo 모니터링 요구 사항을 충족했으며, 생리학적으로 관련된 범위(34.5-39°C)에서 선형 관계가 관찰되었다(그림 3i).
- 높은 가역성(10회 주기 동안 RSD 1.7%, 그림 3k)과 최소한의 LnMOF 용출(72시간 동안 3.5% 감소, 그림 3l)이 입증되었다.
- 증거는 또한 pH 독립성(그림 3m)과 우수한 특이성(그림 3n)을 입증하여 pH 변동 또는 기타 생물학적 간섭 물질에 관계없이 정확한 온도 판독을 보장하였다.
프로브의 광열 변환 능력은 명확하게 확립되었다:
- 단 267 mW의 여기 하에서 프로브는 in vitro에서 102.9°C까지 가열되었으며(그림 4b, c), 효율적인 광열 변환을 확인하였다. 이는 일반적으로 1 W 이상의 펌프 전력을 요구하는 기존 나노물질 기반 시스템에 비해 상당한 이점으로, 이 접근 방식을 더 비용 효율적으로 만들고 잠재적인 부작용을 줄인다.
- 5회의 가열/냉각 주기 동안 안정적인 온도 상승(그림 4d)과 최소한의 ICG 용출(72시간 동안 5.9% 감소, 그림 4g, h)로 우수한 광열 안정성이 입증되어 장기적인 성능을 보장하였다.
- in vivo 실험은 펌프 전력 증가에 따른 종양 부위의 점진적인 온도 상승을 확인하였다(그림 4e, f).
in vivo 검증은 프로브의 실제 유용성에 대한 가장 설득력 있는 증거를 제공하였다:
- 종양 가장자리 식별은 건강한 조직과 종양 조직 간(p < 0.0001), 그리고 종양 표면과 정상 조직 간(p < 0.01)의 측정된 pH 값의 통계적으로 유의미한 차이에 의해 명백하게 입증되었다(그림 5a, b). 이는 진단 능력에 대한 결정적인 증거이다.
- PTT 중 정확한 열 용량 제어는 섬유 온도를 65°C로 적극적으로 유지함으로써 입증되었으며, 이는 종양 가장자리가 효과적인 치료 온도인 45°C에 도달하도록 보장하였다(그림 5c).
- 신속한 효능 평가는 치료 후 TME에서의 유의미한 pH 상승(30분 이내 0.12-0.22 단위 증가, 24시간 후 p < 0.01)으로 검증되었으며(그림 5d, e, f), 치료 반응에 대한 신뢰할 수 있는 바이오마커 역할을 하였다.
- 항종양 효능의 궁극적인 증거는 종양 부피 모니터링에서 나왔다: 치료된 마우스 4마리 중 3마리는 완전한 종양 퇴행을 보였고, 나머지 마우스는 유의미한 성장 억제를 보인 반면, "희생양" 대조군은 점진적인 종양 성장을 보였다(그림 5g, h, i, j).
- 우수한 생체 적합성 및 생체 안전성은 모든 마우스에서 안정적인 체중(그림 5k), H&E 염색된 장기에서 유의미한 세포 사멸/괴사 영역 또는 염증 세포 침윤 없음(그림 S10), 그리고 in vitro 용출 테스트에서의 높은 세포 생존율(그림 S9, 그림 6c)로 확인되었다.
- 마지막으로, 다중 모드 항종양 효과는 조직학적 분석(그림 6a)에 의해 입증되었으며, 치료된 종양에서 다초점 괴사 및 출혈 영역을 나타냈다. 면역 조직 화학은 Caspase-3(세포 사멸 바이오마커)의 상향 조절, Ki67(증식 바이오마커)의 하향 조절, 그리고 종양 저산소증 완화를 나타내는 HIF-1α의 하향 조절을 보여주었으며, 이는 MRI(그림 6b, 그림 S8)에 의해 더욱 뒷받침되었다. 이러한 포괄적인 증거는 프로브의 핵심 메커니즘이 실제로 현실에서 작동하여 효과적인 종양 제거 및 TME 리모델링으로 이어졌음을 부인할 수 없이 입증한다.
한계 및 향후 방향
제시된 광섬유 테라노스틱 프로브는 주목할 만한 능력을 보여주지만, 특정 한계를 인정하고 향후 개발 방향을 고려하는 것이 중요하다.
광섬유 설계에 의해 완화되었지만, 내재적인 한계는 광 투과 깊이이다. 발산장(evanescent field)은 국소 감지를 가능하게 하지만, 얕은 투과 깊이(그림 S5)를 가지므로 프로브는 주로 표면의 즉각적인 근처를 감지하고 치료한다. 이는 정밀하고 국소적인 개입에 적합하지만, TME의 더 넓고 부피적인 매핑은 여러 프로브 또는 더 발전된 광학 전략을 필요로 할 수 있다. pH 감지(감소 시 최대 12.8초) 및 온도 감지(증가 시 최대 2.0초)의 응답 시간은 많은 응용 분야에 적합하지만, 극도로 빠른 밀리초 규모의 생리학적 역학을 포착하는 데는 한계가 될 수 있다.
또 다른 실질적인 고려 사항은 용출이다. 본 논문은 72시간 동안 HPTS-IP(1.6%), LnMOF(3.5%), ICG(5.9%)에 대해 최소한의 용출을 보고했지만, 이는 0이 아니다. 장기간 이식 가능한 장치의 경우, 최소한의 만성 용출조차도 수 주 또는 수개월에 걸쳐 축적되거나 면역 반응을 유발할 수 있으며, 이는 프로브 성능과 환자 안전 모두에 영향을 미칠 수 있다. 광표백을 최소화하기 위해 샘플링 지점 간에 여기광을 차단한다는 언급(그림 2i, 3l 캡션)은 비율 감지가 도움이 되지만, 광표백이 매우 장기간의 연속 모니터링에 영향을 미칠 수 있는 요인으로 남아 있음을 시사한다. 또한, pH 감지에 대한 온도 누화는 pH > 7.0 범위에서 보상되었지만, 전체 pH 범위에서 완전히 무시할 수는 없었으며, 이는 향후 더 정교한 보상 알고리즘을 필요로 할 수 있는 미묘한 상호 작용을 나타낸다. 단일 코팅층의 선택은 SNR과 응답 시간 모두를 최적화하는 동안 절충을 의미한다. 더 두꺼운 필름은 신호를 향상시킬 수 있지만 응답 속도를 희생해야 한다.
미래를 내다볼 때, 본 논문 자체는 몇 가지 흥미로운 방향을 제시한다. 통합 전략은 유연한 폴리머 및 하이드로겔 광섬유에 적용되어 기계적 순응성과 생체 적합성을 향상시켜 장기간 이식 가능한 장치를 위한 길을 열 수 있다. 스펙트럼 자원을 활용하고 다중 피크 피팅 알고리즘을 사용하면 더 많은 기능이 통합됨에 따라 잠재적인 방출 대역 중첩을 해결하여 기능 용량을 더욱 향상시킬 수 있다. 저자들은 또한 종양 가장자리의 더 정확한 온도 모니터링을 위해 시스템을 MRI 온도 측정과 통합할 것을 제안하며, 이는 현재의 열 영상이 이러한 보완 없이는 공간 해상도 또는 깊이에 한계가 있을 수 있음을 시사한다.
논문의 명시적인 제안을 넘어서, 추가 개발 및 발전을 위한 몇 가지 논의 주제가 등장한다:
-
고급 다중 매개변수 통합 및 AI 기반 피드백: WDM 또는 기타 다중화 기술을 사용하여 신호 무결성을 손상시키거나 장치 복잡성을 증가시키지 않고 단일 섬유에 얼마나 더 많은 TME 매개변수(예: 산소 포화도, 포도당 수치, 특정 효소 활성, 약물 농도)를 동시에 통합할 수 있는가? 이러한 프로브의 실시간 데이터는 인공 지능(AI) 또는 기계 학습(ML) 모델에 공급되어 진화하는 TME를 기반으로 레이저 전력, 지속 시간 또는 약물 전달을 동적으로 조정하는 진정한 적응형 개인 맞춤형 치료 프로토콜을 생성할 수 있는가? 이는 단순한 피드백 루프를 넘어 예측적이고 최적화된 치료로 나아갈 수 있다.
-
장기 생체 안정성 및 면역 조절: 단기 생체 적합성은 입증되었지만, 만성 이식의 장기적인 영향은 무엇인가? 생체 오염, 숙주 조직의 캡슐화 또는 만성 염증 반응은 수개월 또는 수년에 걸쳐 프로브의 감지 정확도와 치료 효능에 어떤 영향을 미치는가? 졸-겔 매트릭스는 항염증제 또는 성장 인자를 방출하여 통합을 적극적으로 촉진하고 부작용을 최소화하기 위해 면역 조절 특성을 갖도록 추가로 설계될 수 있는가?
-
확장성, 소형화 및 임상 워크플로우 통합: 현재 프로브는 직경 440 µm, 끝단 100 µm이다. 더 최소 침습적인 절차를 위해 이를 더 작게 만들 수 있는가, 또는 더 크거나 다중 초점 종양을 위해 이러한 프로브의 배열을 개발할 수 있는가? 광범위한 임상 사용을 위한 생산 확대를 위한 제조 과제와 비용은 무엇인가? 이러한 정교한 장치는 전문 교육, 장비 및 데이터 해석의 필요성을 고려할 때 기존 임상 워크플로우에 어떻게 통합될 것인가?
-
비침습적 유도 및 보완 치료: 이 폐쇄 루프 테라노스틱 시스템의 원리를 비침습적 치료를 유도하거나 향상시키는 데 적용할 수 있는가? 예를 들어, 프로브의 덜 침습적인 버전은 외부 방사선 치료, 집속 초음파 또는 전신 화학 요법을 최적화하기 위해 실시간 TME 피드백을 제공하여 단순히 PTT를 수행하는 것 이상으로 적용 범위를 넓힐 수 있는가?
-
윤리적 고려 사항 및 환자 경험: 이러한 장치가 더욱 정교해지고 이식 가능해짐에 따라 데이터 개인 정보 보호, 환자 자율성, 그리고 지속적이고 적응적인 치료로 인한 과잉 치료 또는 의도하지 않은 부작용의 가능성에 대한 윤리적 고려 사항은 무엇인가? 환자 경험을 최적화하고, 이식형 장치 및 빈번한 모니터링과 관련된 불편함과 심리적 부담을 최소화할 수 있는 방법은 무엇인가?
이러한 논의는 이 기술의 방대한 잠재력을 강조하는 동시에, 종양학에서 완전한 실현과 광범위한 영향을 위해 해결해야 할 복잡하고 다학제적인 과제를 강조한다.
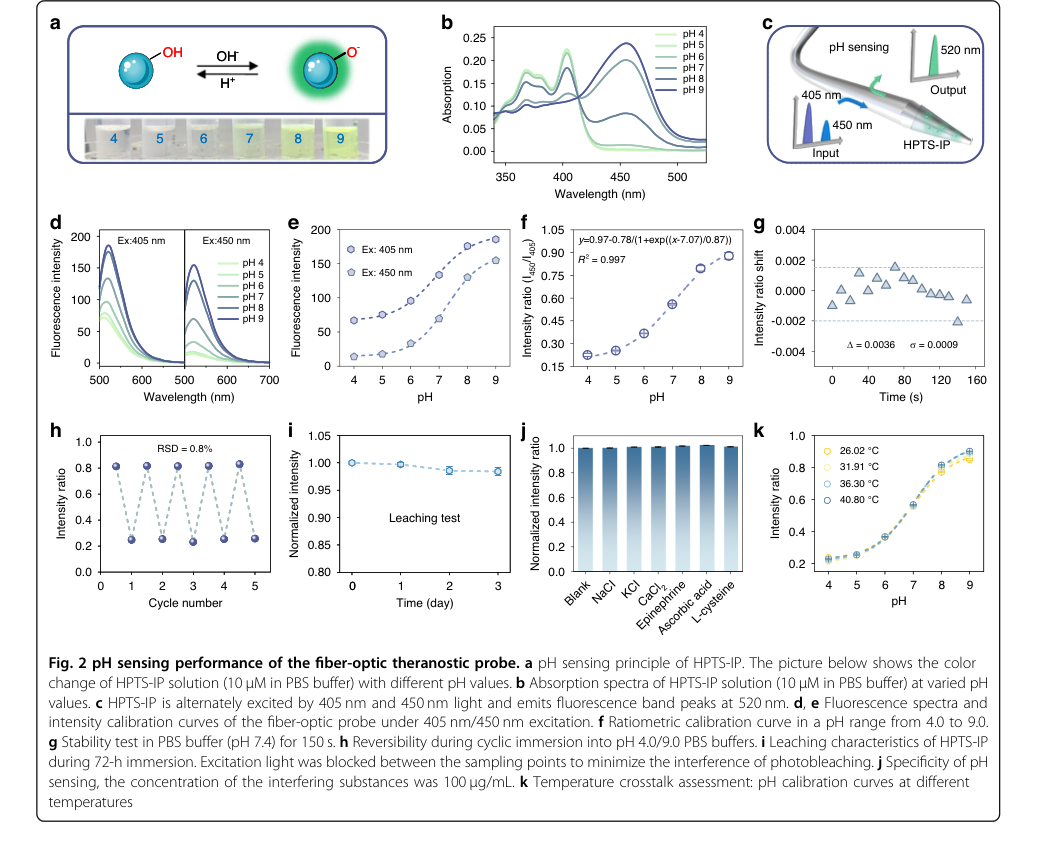 Figure 2. pH sensing performance of the fiber-optic theranostic probe. a pH sensing principle of HPTS-IP. The picture below shows the color change of HPTS-IP solution (10 μM in PBS buffer) with different pH values. b Absorption spectra of HPTS-IP solution (10 μM in PBS buffer) at varied pH values. c HPTS-IP is alternately excited by 405 nm and 450 nm light and emits fluorescence band peaks at 520 nm. d, e Fluorescence spectra and intensity calibration curves of the fiber-optic probe under 405 nm/450 nm excitation. f Ratiometric calibration curve in a pH range from 4.0 to 9.0. g Stability test in PBS buffer (pH 7.4) for 150 s. h Reversibility during cyclic immersion into pH 4.0/9.0 PBS buffers. i Leaching characteristics of HPTS-IP during 72-h immersion. Excitation light was blocked between the sampling points to minimize the interference of photobleaching. j Specificity of pH sensing, the concentration of the interfering substances was 100 μg/mL. k Temperature crosstalk assessment: pH calibration curves at different temperatures
Figure 2. pH sensing performance of the fiber-optic theranostic probe. a pH sensing principle of HPTS-IP. The picture below shows the color change of HPTS-IP solution (10 μM in PBS buffer) with different pH values. b Absorption spectra of HPTS-IP solution (10 μM in PBS buffer) at varied pH values. c HPTS-IP is alternately excited by 405 nm and 450 nm light and emits fluorescence band peaks at 520 nm. d, e Fluorescence spectra and intensity calibration curves of the fiber-optic probe under 405 nm/450 nm excitation. f Ratiometric calibration curve in a pH range from 4.0 to 9.0. g Stability test in PBS buffer (pH 7.4) for 150 s. h Reversibility during cyclic immersion into pH 4.0/9.0 PBS buffers. i Leaching characteristics of HPTS-IP during 72-h immersion. Excitation light was blocked between the sampling points to minimize the interference of photobleaching. j Specificity of pH sensing, the concentration of the interfering substances was 100 μg/mL. k Temperature crosstalk assessment: pH calibration curves at different temperatures
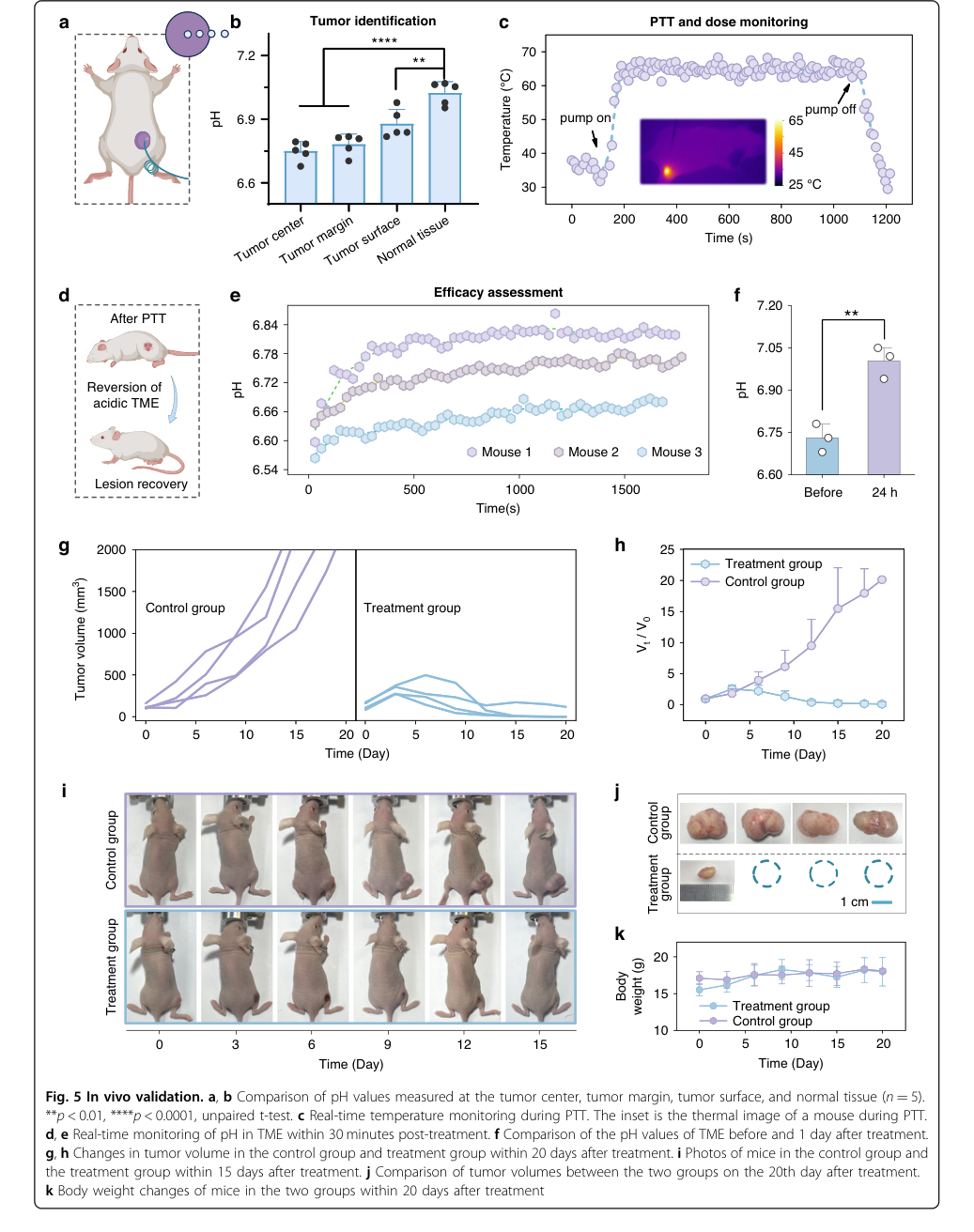 Figure 5. In vivo validation. a, b Comparison of pH values measured at the tumor center, tumor margin, tumor surface, and normal tissue (n = 5). **p < 0.01, ****p < 0.0001, unpaired t-test. c Real-time temperature monitoring during PTT. The inset is the thermal image of a mouse during PTT. d, e Real-time monitoring of pH in TME within 30 minutes post-treatment. f Comparison of the pH values of TME before and 1 day after treatment. g, h Changes in tumor volume in the control group and treatment group within 20 days after treatment. i Photos of mice in the control group and the treatment group within 15 days after treatment. j Comparison of tumor volumes between the two groups on the 20th day after treatment. k Body weight changes of mice in the two groups within 20 days after treatment
Figure 5. In vivo validation. a, b Comparison of pH values measured at the tumor center, tumor margin, tumor surface, and normal tissue (n = 5). **p < 0.01, ****p < 0.0001, unpaired t-test. c Real-time temperature monitoring during PTT. The inset is the thermal image of a mouse during PTT. d, e Real-time monitoring of pH in TME within 30 minutes post-treatment. f Comparison of the pH values of TME before and 1 day after treatment. g, h Changes in tumor volume in the control group and treatment group within 20 days after treatment. i Photos of mice in the control group and the treatment group within 15 days after treatment. j Comparison of tumor volumes between the two groups on the 20th day after treatment. k Body weight changes of mice in the two groups within 20 days after treatment
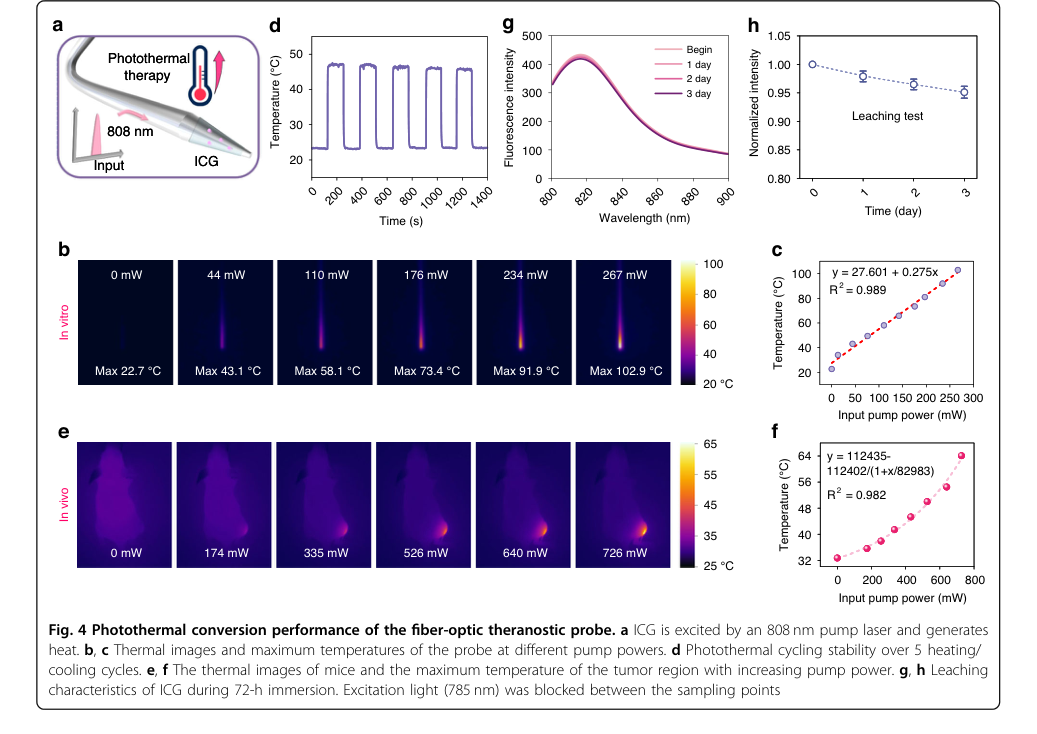 Figure 4. Photothermal conversion performance of the fiber-optic theranostic probe. a ICG is excited by an 808 nm pump laser and generates heat. b, c Thermal images and maximum temperatures of the probe at different pump powers. d Photothermal cycling stability over 5 heating/ cooling cycles. e, f The thermal images of mice and the maximum temperature of the tumor region with increasing pump power. g, h Leaching characteristics of ICG during 72-h immersion. Excitation light (785 nm) was blocked between the sampling points
Figure 4. Photothermal conversion performance of the fiber-optic theranostic probe. a ICG is excited by an 808 nm pump laser and generates heat. b, c Thermal images and maximum temperatures of the probe at different pump powers. d Photothermal cycling stability over 5 heating/ cooling cycles. e, f The thermal images of mice and the maximum temperature of the tumor region with increasing pump power. g, h Leaching characteristics of ICG during 72-h immersion. Excitation light (785 nm) was blocked between the sampling points
다른 필드와의 동형 사상
구조적 골격
다중 환경 변수를 동시에 감지하고 실시간 피드백을 통한 적응형 제어를 제공하는 표적 개입을 위해 고유한 스펙트럼 채널을 활용하는 시스템.
