Многофункциональный волоконно-оптический тераностический зонд для фототермической терапии опухолей в замкнутом контуре
Проблема, рассматриваемая в данной статье, коренится в критической глобальной проблеме здравоохранения, связанной с раком, который ежегодно уносит миллионы жизней и приводит к такому же количеству новых случаев...
Предыстория и академическая родословная
Истоки и академическая родословная
Проблема, рассматриваемая в данной статье, коренится в критической глобальной проблеме здравоохранения, связанной с раком, который ежегодно уносит миллионы жизней и приводит к такому же количеству новых случаев заболевания. Эта мрачная ситуация стимулировала обширные исследования, направленные на разработку более точных и эффективных методов диагностики и терапии. В этом контексте возникла концепция "тераностики", направленная на интеграцию диагностических и терапевтических функций в единую пространственно ко-локализованную платформу для обеспечения немедленной, целенаправленной терапии и мониторинга в реальном времени.
В частности, фототераностика, использующая свет как для диагностики, так и для терапии, привлекла значительное внимание благодаря своей высокой специфичности, пространственно-временному контролю и неионизирующей природе. Однако ее клиническое применение столкнулось с двумя основными препятствиями: изначально ограниченной глубиной проникновения света в биологические ткани (обычно менее 10 мм из-за рассеяния и поглощения) и системной токсичностью, вызванной неспецифическим накоплением наноматериалов, используемых в качестве тераностических агентов, в здоровых тканях.
Комбинация оптических волокон с фототераностическими агентами была определена как перспективная стратегия для преодоления этих ограничений. Оптические волокна обеспечивают эффективную передачу света к глубоко расположенным опухолям и позволяют локализовать терапевтические агенты, тем самым снижая системную токсичность. Несмотря на эти преимущества, предыдущие конструкции волоконно-оптических зондов страдали от существенных "болевых точек". Большинство существующих подходов ограничивались реализацией одной функции на волокно или испытывали перекрестные помехи между функциями из-за спектрального перекрытия агентов. Это часто требовало конфигураций с несколькими волокнами, что приводило к увеличению жесткости устройства, большим размерам, более инвазивным процедурам и отсутствию обратной связи в реальном времени о терапии. Эти проблемы в совокупности увеличивали риск повреждения тканей и пост-терапевтического воспаления, препятствуя широкому клиническому применению. Данная статья напрямую решает эти фундаментальные ограничения, предлагая новую схему многофункциональной интеграции на одном волокне, вдохновленную технологией мультиплексирования с разделением по длине волны (WDM), для обеспечения фототермической терапии опухолей в замкнутом контуре с обратной связью в реальном времени.
Интуитивно понятные термины предметной области
- Тераностика: Представьте себе высокотехнологичный медицинский инструмент, который действует как супергерой "диагностика и лечение". Он может мгновенно сообщить врачу, что не так внутри вашего тела, а затем немедленно доставить нужное лечение в это точное место, и все это за один раз. Это комбинация диагностики и терапии.
- Фототермическая терапия (ФТТ): Думайте об этом как об использовании крошечного, сверхфокусированного лазерного луча для мягкого нагрева и уничтожения нежелательных клеток, подобно тому, как увеличительное стекло может концентрировать солнечный свет, чтобы сжечь небольшое пятно на листе. Часть "фото" означает, что используется свет, а "термическая" означает, что генерируется тепло.
- Мультиплексирование с разделением по длине волны (WDM): Представьте себе одну, очень оживленную магистраль, но вместо автомобилей она несет различные типы информации, каждый из которых движется по отдельному "цвету" света. Это позволяет многим различным сигналам одновременно передаваться по одному и тому же волокну, не мешая друг другу, что делает магистраль гораздо более эффективной.
- Опухолевое микроокружение (ОМО): Это относится к непосредственному окружению опухоли, включая все клетки, кровеносные сосуды и химические сигналы, которые поддерживают ее рост. Это похоже на специфический "район", который опухоль создает для себя, который может сильно отличаться от здоровой ткани, часто будучи более кислым.
- Ратиометрические флуоресцентные зонды: Рассмотрите умный световой датчик, который не просто измеряет яркость одного цвета света, а измеряет яркость двух разных цветов и сравнивает их соотношение. Это делает измерение гораздо более надежным и точным, даже если общая яркость изменяется из-за внешних факторов, подобно тому, как сравнение двух чисел может дать более стабильный результат, чем полагаться только на одно.
Таблица обозначений
| Обозначение | Описание |
|---|---|
| $I_{450}/I_{405}$ | Соотношение флуоресцентных интенсивностей при 450 нм и 405 нм, используемое для определения pH. |
| $R$ | Разрешение по pH, указывающее наименьшее изменение pH, которое может быть надежно обнаружено. |
| $s$ | Чувствительность, представляющая наклон калибровочной кривой pH. |
| $T_1$ | Время отклика для определения pH или температуры при увеличении значения. |
| $T_2$ | Время отклика для определения pH или температуры при уменьшении значения. |
| $I_{618}/I_{546}$ | Соотношение флуоресцентных интенсивностей при 618 нм и 546 нм, используемое для определения температуры. |
| $p$ | p-значение, статистическая мера, используемая для определения значимости экспериментальных результатов. |
| $V/V_0$ | Нормализованный объем опухоли, представляющий объем опухоли относительно ее начального объема. |
| $\sigma$ | Стандартное отклонение, мера количества вариации или дисперсии в наборе значений. |
Определение проблемы и ограничения
Формулировка основной проблемы и дилемма
Фундаментальная проблема, рассматриваемая в данной статье, проистекает из критической потребности в эффективной и минимально инвазивной тераностике рака – комбинированном диагностическом и терапевтическом подходе. Современные методы сталкиваются со значительными ограничениями, которые препятствуют их клиническому применению.
Входное/текущее состояние может быть охарактеризовано несколькими недостатками:
1. Ограниченное проникновение света и системная токсичность: Традиционные фототераностические агенты, часто на основе наноматериалов, страдают от изначально ограниченной глубины проникновения света (обычно менее 10 мм) в ткани из-за рассеяния и поглощения. Кроме того, их неспецифическое накопление в нормальных тканях и органах приводит к системной токсичности.
2. Недооцененный мультиплексирующий потенциал оптических волокон: Хотя оптические волокна предлагают преимущества, такие как доступ к глубоко расположенным опухолям и локализованное удержание агентов, их потенциал для интеграции нескольких функций на одной платформе в значительной степени не использовался.
3. Перекрестные помехи между функциями и сложность устройства: Предыдущие волоконно-оптические зонды либо ограничивались реализацией одной функции на волокно, либо, при попытке интеграции нескольких функций, страдали от перекрестных помех между функциями. Эти перекрестные помехи в основном возникали из-за спектрального перекрытия в полосах поглощения или эмиссии различных функциональных реагентов. Чтобы обойти это, исследователи часто прибегали к конфигурациям с несколькими волокнами, что неизбежно увеличивало жесткость и размеры устройства, делая их менее совместимыми с минимально инвазивными интервенционными методами и повышая риски повреждения тканей и пост-терапевтического воспаления.
4. Отсутствие обратной связи в реальном времени о терапии: Существующие методы часто не имеют возможностей мониторинга в реальном времени для терапевтической дозы и эффективности, что препятствует контролю в замкнутом контуре и персонализированной прецизионной медицине.
Желаемое конечное состояние (выходное/целевое состояние) — это единый, компактный, многофункциональный волоконно-оптический тераностический зонд, способный:
1. Фототермическая терапия опухолей (ФТТ) в замкнутом контуре: Это включает интеграцию диагностических и терапевтических функций на одной платформе для обратной связи в реальном времени.
2. Многопараметрический мониторинг: Зонд должен обеспечивать одновременный мониторинг ключевых параметров опухолевого микроокружения (ОМО), в частности pH и температуры.
3. Минимально инвазивное вмешательство: Устройство должно быть компактным (например, диаметром 440 мкм, как достигнуто авторами) для доступа к опухолевым поражениям посредством интервенционных процедур, избегая увеличенных разрезов и повторных инвазивных процедур.
4. Предоперационная идентификация опухоли: Точное определение границ опухоли путем выявления градиента pH опухоли.
5. Контроль тепловой дозы во время лечения: Точный контроль тепловой дозы во время ФТТ путем одновременного мониторинга температуры.
6. Оценка эффективности после лечения: Быстрая оценка эффективности лечения путем мониторинга обратного развития кислотного ОМО.
7. Преодоление ограничений проникновения света и токсичности: Решение проблем ограниченной глубины проникновения света и системной токсичности, связанных с наноматериальными стратегиями.
Точное недостающее звено или математический пробел, который данная статья пытается преодолеть, — это разработка надежной одноволоконной платформы, которая может одновременно выполнять несколько тераностических функций (определение pH, определение температуры и фототермическая терапия) без перекрестных помех между функциями, обеспечивая при этом обратную связь в реальном времени. Основная математическая/конструкторская задача заключается в выборе и совместной иммобилизации нескольких функциональных агентов (индикатор pH, индикатор температуры, фототермический агент) таким образом, чтобы их спектры возбуждения и эмиссии были достаточно разделены, чтобы обеспечить мультиплексирование с разделением по длине волны (WDM) на одном волокне. Это позволяет активировать различные функции по требованию с помощью определенных длин волн, эффективно устраняя проблему спектрального перекрытия, которая преследовала предыдущие попытки мультиплексирования на одном волокне. Решение статьи заключается в тщательном выборе HPTS-IP, LnMOF и ICG, полосы поглощения которых (405/450 нм для HPTS-IP, 295 нм для LnMOF, 790 нм для ICG) не перекрываются, что обеспечивает WDM.
Болезненный компромисс или дилемма, которая загнала предыдущих исследователей в тупик, — это присущий конфликт между функциональным мультиплексированием и простотой/производительностью устройства. Для достижения нескольких функций приходилось:
* Увеличивать сложность устройства: Использовать несколько волокон, что приводило к громоздким, жестким устройствам, непригодным для минимально инвазивных процедур и повышающим риск для пациента.
* Компрометировать функциональную целостность: Пытаться интегрировать несколько агентов на одном волокне, только чтобы столкнуться с серьезными перекрестными помехами между функциями из-за спектрального перекрытия, что делало многофункциональность ненадежной или неточной. Это означало, что улучшение одного аспекта (например, добавление большего количества функций) напрямую нарушало другой (например, целостность сигнала или размер устройства).
Ограничения и режимы отказа
Проблема разработки многофункционального волоконно-оптического тераностического зонда чрезвычайно сложна из-за нескольких суровых, реалистичных стен, с которыми столкнулись авторы:
-
Физические ограничения:
- Ограниченная глубина проникновения света: Естественное рассеяние и поглощение света в биологических тканях сильно ограничивают его проникновение, обычно до менее 10 мм. Это затрудняет лечение глубоко расположенных опухолей для фототермических методов.
- Системная токсичность: Неспецифическое накопление тераностических наноматериалов в нормальных тканях и органах приводит к нежелательной системной токсичности, что является серьезным препятствием для клинического применения.
- Жесткость и размеры устройства: Для минимально инвазивных процедур зонд должен быть гибким и компактным. Многоволоконные конструкции увеличивают жесткость и размеры, делая их несовместимыми с интервенционными методами и повышая риски повреждения тканей.
- Ограничения конструкции конического волокна: Геометрия конического оптического волокна имеет решающее значение. Чрезмерно короткие конусы рискуют утечкой света и ухудшают соотношение сигнал/шум (SNR), в то время как слишком длинные конусы непригодны для локализованного зондирования и терапии. Диаметр кончика влияет как на силу эванесцентного поля (и, следовательно, на эффективность возбуждения/сбора флуоресценции), так и на доступную площадь поверхности для иммобилизации индикатора, требуя тщательной оптимизации (например, 100 мкм было признано оптимальным).
- Целостность гидрогелевой пленки: Матрица на основе золь-геля, используемая для инкапсуляции функциональных агентов, должна быть стабильной и биосовместимой. Чистые пленки тетраэтилортосиликата (TEOS) склонны к сильному растрескиванию, что приводит к низкой однородности пленки и высоким скоростям выщелачивания, что ухудшает стабильность и биосовместимость датчика. Добавление со-прекурсоров, таких как GLYMO, и поверхностно-активных веществ, таких как Triton X-100, необходимо для смягчения этого.
-
Ограничения, основанные на данных, и ограничения производительности:
- Перекрестные помехи между функциями: Основная проблема мультиплексирования на одном волокне — предотвращение спектрального перекрытия между полосами поглощения и эмиссии различных функциональных реагентов (индикатор pH, индикатор температуры, фототермический агент). Это перекрытие привело бы к неточным показаниям и невозможности различать сигналы от различных функций.
- Требования к задержке в реальном времени: Для терапии в замкнутом контуре и мониторинга в реальном времени датчики должны иметь достаточно быстрое время отклика. В статье сообщается о времени отклика pH-зондирования 3,2 с (увеличение pH) и 12,8 с (уменьшение pH), а также о времени отклика температурного зондирования 2,0 с (увеличение температуры) и 0,6 с (уменьшение температуры), которые считаются приемлемыми для in vivo мониторинга.
- Стабильность и надежность датчика: Функциональные агенты должны оставаться стабильными и не выщелачиваться значительно с поверхности волокна со временем в физиологической среде. Тесты на выщелачивание показали минимальное снижение интенсивности флуоресценции (1,6% для HPTS-IP, 3,5% для LnMOF за 72 часа), что указывает на хорошую стабильность.
- Вмешательство физиологических факторов: Производительность зондирования должна быть устойчивой к различным мешающим веществам, присутствующим в сложных физиологических средах, а также к фотообесцвечиванию, вариациям концентрации индикатора и изменениям морфологии волокна. Использование ратиометрических флуоресцентных зондов и тщательный выбор агентов помогают смягчить эти проблемы.
- Собственная флуоресценция тканей: Эндогенная флуоресценция тканей может мешать сигналам зонда, ухудшая точность и специфичность зондирования. Неглубокая глубина проникновения эванесцентного поля, где концентрация индикатора высока, помогает поддерживать высокое SNR.
- Точный контроль тепловой дозы: Во время фототермической терапии доставка эффективной тепловой дозы без чрезмерного нагрева прилегающих нормальных тканей имеет решающее значение. Перегрев может привести к повреждению тканей, коллапсу сосудов и нарушению кровотока. Это требует точного мониторинга температуры в реальном времени.
Почему этот подход
Неизбежность выбора
Решение авторов в пользу стратегии многофункциональной интеграции на одном волокне с использованием технологии мультиплексирования с разделением по длине волны (WDM) было не просто улучшением, а неизбежным выбором, обусловленным присущими ограничениями существующих подходов. Статья четко определяет момент, когда традиционные "передовые" (SOTA) методы оказались недостаточными: "Несмотря на недавние достижения, мультиплексирующий потенциал волоконно-оптических зондов остается недооцененным. Текущие исследования ограничиваются реализацией одной функции на волокно или страдают от перекрестных помех между функциями, которые в основном возникают из-за спектрального перекрытия в полосах поглощения или эмиссии используемых функциональных реагентов." Эта проблема спектрального перекрытия означала, что достижение многопараметрического мониторинга или интегрированной тераностики часто требовало конфигураций с несколькими волокнами. Однако такие установки "неизбежно увеличивают жесткость и размеры устройства, снижая совместимость с минимально инвазивными методами и повышая риски повреждения тканей и пост-терапевтического воспаления". Учитывая эти критические недостатки — отсутствие обратной связи в реальном времени, инвазивность и перекрестные помехи между функциями — требовался сдвиг парадигмы. Подход на основе WDM для одного волокна стал единственным жизнеспособным решением для преодоления этих фундаментальных проблем путем обеспечения множества функций на одной компактной платформе без спектральных помех.
Сравнительное превосходство
Помимо простых метрик производительности, этот метод предлагает глубокое качественное превосходство, в первую очередь благодаря своей структурной конструкции. Основное преимущество заключается в его способности интегрировать несколько функций (определение pH, мониторинг температуры и фототермическая терапия) на одном оптическом волокне с использованием мультиплексирования с разделением по длине волны. Эта структурная инновация по своей сути минимизирует перекрестные помехи между функциями, что является серьезной проблемой в предыдущих системах с несколькими агентами, где спектральное перекрытие ухудшало целостность сигнала. Тщательно выбирая агенты (HPTS-IP, LnMOF, ICG) с "неперекрывающимися полосами поглощения", зонд обеспечивает точное и надежное измерение каждого параметра.
Кроме того, выбранные ратиометрические флуоресцентные зонды для определения pH и температуры обеспечивают решающее качественное преимущество. Эта стратегия ратиометрического детектирования "снижает влияние фотообесцвечивания, вариаций концентрации индикатора и изменений морфологии волокна на результаты зондирования, облегчая получение точных и надежных сигналов". Это значительное улучшение по сравнению с интенсивным зондированием, которое очень подвержено шуму и флуктуациям окружающей среды. Компактная конструкция на одном волокне также значительно уменьшает физические размеры и жесткость по сравнению с многоволоконными пучками, что делает ее подавляюще превосходящей для минимально инвазивных вмешательств. Она также локализует тераностические агенты, эффективно снижая системную токсичность, связанную со свободными наноматериалами.
Соответствие ограничениям
Выбранный метод идеально соответствует строгим ограничениям передовых тераностических применений.
- Минимально инвазивный: Использование одного гибкого оптического волокна (диаметром 440 мкм, диаметром кончика 100 мкм) позволяет "получить доступ к опухолевым поражениям посредством интервенционных процедур", значительно снижая инвазивность по сравнению с многоволоконными или более крупными конструкциями зондов. Это напрямую решает задачу минимизации повреждения тканей и пост-терапевтического воспаления.
- Обратная связь в реальном времени и терапия в замкнутом контуре: Интеграция индикаторов pH и температуры с фототермическим агентом на одной платформе обеспечивает "фототермическую терапию опухолей в замкнутом контуре с обратной связью в реальном времени". Это означает, что зонд может выполнять предоперационную идентификацию опухоли (через градиент pH), контроль дозы во время лечения (через мониторинг температуры во время ФТТ) и оценку эффективности после лечения (через обратное развитие кислотного ОМО), удовлетворяя критическую потребность в динамической, адаптивной терапии.
- Многопараметрический мониторинг: Схема мультиплексирования с разделением по длине волны позволяет одновременно отслеживать pH и температуру, наряду с фототермической терапией, на одном волокне. Это напрямую удовлетворяет требованию комплексной многопараметрической оценки в сложных биологических средах.
- Снижение системной токсичности и доступ к глубоким тканям: Иммобилизуя фототераностические агенты на поверхности оптического волокна, подход "эффективно снижает внецелевую токсичность за счет локализованного удержания". Кроме того, оптические волокна обеспечивают "сквозную передачу света с минимальными потерями", позволяя зондировать и лечить "глубоко расположенные опухоли", тем самым преодолевая ограниченную глубину проникновения света традиционных фототераностических агентов.
Отклонение альтернатив
Статья неявно и явно отклоняет несколько альтернативных подходов на основе их фундаментальных ограничений для конкретной проблемы замкнутой, многофункциональной тераностики опухолей.
- Реализации "одна функция на волокно": Они были признаны недостаточными, поскольку требовали бы нескольких волокон для многопараметрического мониторинга и терапии, что приводило бы к "увеличенным разрезам, повторным инвазивным процедурам" и повышенной жесткости устройства. Целью была интегрированная тераностика, а не фрагментированные функциональные возможности.
- Многоволоконные конфигурации: Хотя они и обеспечивали мультиплексирование, они были отклонены из-за их присущих физических ограничений, таких как "увеличенная жесткость и размеры устройства", которые ухудшают совместимость с минимально инвазивными интервенционными методами и повышают риски повреждения тканей.
- Подходы, страдающие от перекрестных помех между функциями: Методы, где функциональные реагенты имеют "спектральное перекрытие в полосах поглощения и эмиссии", были явно определены как проблематичные. Тщательный выбор авторами агентов с неперекрывающимися полосами и стратегия WDM напрямую решают эту точку отказа, обеспечивая целостность сигнала.
- Стратегии, зависящие от наноматериалов (без интеграции волокна): В заключении подчеркивается, что по сравнению с "наноматериальными стратегиями", этот волоконно-оптический подход "эффективно решает проблемы ограниченной глубины проникновения света и системной токсичности". Это подразумевает, что полагаться исключительно на свободно плавающие или неинтегрированные с волокном наноматериалы не удастся обеспечить необходимого доступа к глубоким тканям и локализованной, нетоксичной доставки, необходимой для эффективной фототермической терапии опухолей.
Математический и логический механизм
Основное уравнение
В основе возможностей зондирования этого тераностического зонда лежит модель сигмоиды Больцмана, которая служит фундаментальной логикой преобразования для перевода ратиометрических сигналов флуоресценции в значимые физиологические параметры, такие как pH и температура. Хотя компонент фототермической терапии включает прямое преобразование света в тепло, его точный контроль и мониторинг полностью зависят от точных показаний, предоставляемых этими механизмами зондирования.
Общая форма уравнения Больцмана, как используется в данной статье для определения как pH, так и температуры, может быть выражена следующим образом:
$$ y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}} $$
Где:
- Для определения pH (выведено из рис. 2f):
$$
R_{pH} = 0.97 - \frac{0.78}{1 + e^{(pH - 7.07)/0.87}}
$$
Здесь $y$ — это соотношение интенсивностей флуоресценции $R_{pH} = I_{520}(450nm) / I_{520}(405nm)$, а $x$ — значение pH.
- Для определения температуры (выведено из рис. 3g):
$$ R_{Temp} = 1.55 - \frac{0.81}{1 + e^{(Temp - 65.74)/10.71}} $$
Здесь $y$ — это соотношение интенсивностей флуоресценции $R_{Temp} = I_{618} / I_{546}$, а $x$ — значение температуры в градусах Цельсия.
Эти уравнения являются основным математическим механизмом, который позволяет зонду количественно интерпретировать оптические сигналы, которые он получает, предоставляя решающую обратную связь для тераностики в замкнутом контуре.
Потерминальная аутопсия
Давайте разберем общее уравнение Больцмана $y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}}$, чтобы понять роль каждого компонента:
-
$y$ (Соотношение интенсивностей флуоресценции, $R_{pH}$ или $R_{Temp}$)
- Математическое определение: Это зависимая переменная, представляющая безразмерное соотношение интенсивностей флуоресценции. Для определения pH это соотношение интенсивности эмиссии при 520 нм при возбуждении на 450 нм к интенсивности при возбуждении на 405 нм ($I_{520}(450nm) / I_{520}(405nm)$). Для определения температуры это соотношение интенсивностей эмиссии при 618 нм к 546 нм ($I_{618} / I_{546}$) при возбуждении на 295 нм.
- Физическая/логическая роль: Этот член является прямым выходом оптической измерительной системы. Используя соотношение, авторы искусно смягчают распространенные источники ошибок, такие как фотообесцвечивание, вариации концентрации индикатора и изменения морфологии волокна. Эта нормализация делает сигнал надежным и достоверным, действуя как основной наблюдаемый параметр, который предсказуемо изменяется в зависимости от целевого параметра.
- Почему соотношение/вычитание/деление: Соотношение является стандартным методом в ратиометрическом зондировании для самореференции и отмены общего шумового сигнала. Общая сигмоидальная форма, включающая вычитание и деление, естественно возникает из химических или физических процессов, где индикатор переходит между двумя состояниями (например, протонированным/депротонированным или различными состояниями переноса энергии) в ответ на непрерывную переменную, демонстрируя насыщение на обоих крайних значениях.
-
$x$ (Физиологический параметр, $pH$ или $Temp$)
- Математическое определение: Это независимая переменная, представляющая измеряемое условие окружающей среды (pH или температура в °C).
- Физическая/логическая роль: Это фактическая физическая величина, которую тераностический зонд предназначен для обнаружения и мониторинга. Это "истинное" значение, которое система стремится определить.
- Почему независимая переменная: Это причина, а $y$ — следствие. Процесс калибровки устанавливает функциональную связь между этим входом и измеренным выходным соотношением.
-
$C_1$ (Верхняя асимптота)
- Математическое определение: Постоянный коэффициент, представляющий верхнее плато сигмоидальной кривой при стремлении $x$ к плюс бесконечности (для данной формы убывающей сигмоиды).
- Физическая/логическая роль: Для pH $C_1 = 0.97$ представляет максимальное соотношение флуоресценции, достигаемое, когда индикатор HPTS-IP преимущественно находится в одном из своих состояний протонирования (например, полностью депротонирован при высоком pH). Для температуры $C_1 = 1.55$ представляет максимальное соотношение для LnMOF при высоких температурах. Он определяет один край динамического диапазона датчика, указывая точку насыщения, где дальнейшее увеличение $x$ больше не изменяет состояние индикатора значительно.
- Почему константа: Это асимптотическое значение, отражающее максимальный возможный отклик индикатора в экстремальных условиях, когда равновесие почти полностью сместилось в одну сторону.
-
$C_2$ (Масштабирующий коэффициент диапазона)
- Математическое определение: Постоянный коэффициент, который масштабирует величину сигмоидального перехода. Он представляет общее изменение $y$ от его нижней асимптоты до его верхней асимптоты.
- Физическая/логическая роль: Для pH $C_2 = 0.78$ определяет общий диапазон изменения соотношения флуоресценции при изменении pH в чувствительном диапазоне. Для температуры $C_2 = 0.81$ делает то же самое для температуры. Этот член по существу определяет "высоту" сигмоидального шага, указывая общий динамический диапазон отклика датчика.
- Почему константа: Это присущее свойство индикатора и его взаимодействия с окружающей средой, отражающее максимальное возможное изменение ратиометрического сигнала.
-
$C_3$ (Середина или центр перехода)
- Математическое определение: Постоянный коэффициент, представляющий значение $x$, при котором отклик находится на полпути между его асимптотическими пределами (или где наклон максимален).
- Физическая/логическая роль: Для pH $C_3 = 7.07$ указывает значение pH, при котором индикатор HPTS-IP наиболее чувствителен к изменениям, часто соответствующее его pKa. Для температуры $C_3 = 65.74$ °C отмечает температуру, при которой механизм переноса энергии LnMOF демонстрирует самое крутое изменение. Этот параметр имеет решающее значение для определения рабочего диапазона и оптимальной чувствительности датчика.
- Почему константа: Это присущее свойство химического или физического процесса, контролируемого индикатором.
-
$C_4$ (Параметр наклона)
- Математическое определение: Постоянный коэффициент, обратно пропорциональный максимальному наклону сигмоидальной кривой. Меньшее абсолютное значение $C_4$ указывает на более крутую кривую.
- Физическая/логическая роль: Для pH $C_4 = 0.87$ количественно определяет крутизну кривой отклика pH. Для температуры $C_4 = 10.71$ делает то же самое для температуры. Этот параметр напрямую связан с чувствительностью датчика: меньшее значение $C_4$ означает более быстрое изменение соотношения флуоресценции для данного изменения $x$ вблизи середины $C_3$.
- Почему константа: Он отражает присущую отзывчивость и кооперативность перехода индикатора.
-
$e$ (Число Эйлера)
- Математическое определение: Математическая константа, основание натурального логарифма, приблизительно равное 2.71828.
- Физическая/логическая роль: Оно является фундаментальным для экспоненциальных функций, которые используются здесь для моделирования сигмоидального перехода. Такие переходы часто возникают из статистической механики или уравнений химического равновесия (например, уравнения Гендерсона-Хассельбаха для pH или распределений Больцмана для энергетических состояний), где вероятность состояния экспоненциально изменяется с движущей силой.
- Почему экспоненциальная: Экспоненциальный член естественно описывает нелинейное, насыщающееся поведение, наблюдаемое во многих физических и химических системах при приближении к равновесию.
-
Показатель степени $(x - C_3)/C_4$
- Математическое определение: Аргумент экспоненциальной функции.
- Физическая/логическая роль: Этот член нормализует разницу между текущим входом $x$ и серединой $C_3$, деленную на параметр наклона $C_4$. Он эффективно масштабирует вход для соответствия экспоненциальному затуханию или росту, определяя, насколько система далека от точки полуперехода.
-
Деление на $(1 + e^{(x - C_3)/C_4})$
- Математическое определение: Эта специфическая форма является ядром сигмоидальной формы, часто называемой логистической функцией или распределением Ферми-Дирака.
- Физическая/логическая роль: Этот член гарантирует, что выход $y$ плавно переходит между двумя асимптотами при изменении $x$. Он моделирует постепенный сдвиг состояния индикатора от одного крайнего значения к другому.
-
Вычитание $C_1 - \frac{C_2}{...}$
- Математическое определение: Эта операция объединяет верхнюю асимптоту с масштабированным сигмоидальным членом.
- Физическая/логическая роль: Для конкретной формы, используемой в статье, это вычитание создает убывающую сигмоиду, если $C_2$ положительно, что означает, что соотношение $y$ начинается с высокого значения и уменьшается до $C_1 - C_2$ при увеличении $x$. Однако графики (рис. 2f и 3g) показывают увеличивающиеся соотношения с увеличением pH/температуры. Это подразумевает, что подгоночное уравнение авторов $y = C_1 - \frac{C_2}{1 + e^{(x - C_3)/C_4}}$ на самом деле является увеличивающейся сигмоидой, где $C_1$ является верхней асимптотой, а $C_1 - C_2$ — нижней асимптотой. При $x \to -\infty$, $e^{(x - C_3)/C_4} \to 0$, так что $y \to C_1 - C_2$. При $x \to +\infty$, $e^{(x - C_3)/C_4} \to \infty$, так что $y \to C_1$. Это соответствует рисункам. Вычитание является неотъемлемой частью определения ориентации и диапазона кривой.
Пошаговый поток
Представьте тераностический зонд как сложный, миниатюрный сборочный конвейер для обработки данных, где каждый шаг преобразует необработанные оптические сигналы в действенные физиологические выводы.
-
Вход света и выбор длины волны: Процесс начинается с поступления света от настраиваемого источника в Y-образное оптическое волокно. В зависимости от желаемого измерения выбирается определенная длина волны, подобно выбору инструмента из ящика. Для определения pH система быстро переключается между возбуждающим светом 405 нм и 450 нм. Для определения температуры используется длина волны возбуждения 295 нм. Это мультиплексирование с разделением по длине волны (WDM) является начальным "переключателем", который определяет функцию зонда.
-
Взаимодействие эванесцентного поля: Выбранный свет проходит вниз по волокну к его коническому кончику, где он выходит в окружающую гидрогелевую матрицу в виде "эванесцентного поля". Это поле действует как микроскопическая сеть, непосредственно взаимодействуя с совместно иммобилизованными молекулами индикатора (HPTS-IP для pH, LnMOF для температуры). Индикаторы поглощают этот свет, становясь возбужденными.
-
Эмиссия флуоресценции: После возбуждения возбужденные молекулы индикатора испускают флуоресценцию. Характеристики этого испускаемого света чувствительны к локальной среде. Для pH HPTS-IP испускает флуоресценцию при 520 нм, но его интенсивность при этой длине волны варьируется в зависимости от того, был ли он возбужден на 405 нм или 450 нм, отражая локальное состояние протонирования. Для температуры LnMOF испускает флуоресценцию на двух различных длинах волн, 546 нм и 618 нм, причем их относительные интенсивности изменяются в зависимости от локальной температуры из-за динамики переноса энергии.
-
Сбор сигнала: Испускаемая флуоресценция затем эффективно собирается обратно в то же оптическое волокно, подобно пылесосу, всасывающему свет, и направляется от ткани.
-
Спектральный анализ: Собранный свет направляется в анализатор спектра флуоресценции (FSA). Это устройство действует как "сортировщик света", измеряя точную интенсивность флуоресценции на соответствующих длинах волн эмиссии. Для pH оно измеряет $I_{520}(450nm)$ и $I_{520}(405nm)$. Для температуры оно измеряет $I_{618}$ и $I_{546}$.
-
Ратиометрический расчет: Затем вычислительный блок рассчитывает безразмерное соотношение из этих необработанных измерений интенсивности. Для pH он вычисляет $R_{pH} = I_{520}(450nm) / I_{520}(405nm)$. Для температуры он вычисляет $R_{Temp} = I_{618} / I_{546}$. Это соотношение является стандартизированной "точкой данных", которая будет подаваться в математический механизм.
-
Преобразование по модели Больцмана: Это рассчитанное соотношение ($R_{pH}$ или $R_{Temp}$) затем вводится в предварительно откалиброванное уравнение Больцмана. Уравнение, действующее как "декодер", выполняет нелинейное преобразование, фактически инвертируя калибровочную кривую для получения фактического физиологического параметра. Например, если $R_{pH}$ вводится в уравнение Больцмана для pH, оно выводит соответствующее значение pH. Аналогично, $R_{Temp}$ дает температуру.
-
Обратная связь в реальном времени и действие: Полученные значения pH и температуры отображаются в реальном времени. Эти точные показания служат критической обратной связью. Во время фототермической терапии (ФТТ) показания температуры позволяют "контролировать тепловую дозу", позволяя оператору регулировать мощность насосного лазера 808 нм для поддержания целевой температуры (например, 65 °C на кончике волокна, обеспечивая 45 °C на краю опухоли). После лечения мониторинг pH оценивает эффективность, отслеживая обратное развитие кислотного микроокружения опухоли. Эта система с замкнутым контуром гарантирует, что терапия не только доставляется, но и постоянно оптимизируется на основе физиологического состояния пациента в реальном времени.
Динамика оптимизации
"Динамика оптимизации" этого тераностического зонда в основном заключается в его первоначальной калибровке и его присущей конструкции для надежного контроля с обратной связью в реальном времени, а не в непрерывном итеративном обучении в смысле машинного обучения.
-
Калибровка как первоначальное "обучение":
- Сбор данных: Перед клиническим применением зонд проходит строгий процесс калибровки. Это включает воздействие датчика на диапазон известных значений pH (например, от 4,0 до 9,0) и температур (например, от 30 °C до 100 °C) в контролируемых лабораторных условиях. При каждой известной точке измеряется соответствующий сигнал ратиометрической флуоресценции.
- Подгонка модели: Эти собранные точки данных (известный параметр $x$ против измеренного соотношения $y$) затем используются для "обучения" или "подгонки" модели сигмоиды Больцмана. Этот процесс подгонки является формой нелинейной регрессии, где коэффициенты ($C_1, C_2, C_3, C_4$) уравнения Больцмана итеративно корректируются для минимизации разницы (например, суммы квадратов ошибок) между предсказанным соотношением модели и экспериментально наблюдаемым соотношением для каждого известного входа. Это похоже на навигацию по "ландшафту потерь" для поиска оптимального набора параметров, которые наилучшим образом описывают кривую отклика датчика. В статье сообщается о высоких значениях $R^2$ (0,997 для pH, 0,997 для температуры), что указывает на отличную подгонку и, следовательно, на четко определенный ландшафт потерь с явным минимумом.
- Фиксация параметров: Как только эти коэффициенты определены, они фиксируются. Датчик не "обучается" и не обновляет эти параметры во время своей рабочей фазы. Эта однократная калибровка устанавливает "базу знаний" датчика.
-
Ратиометрическая конструкция для надежности (неявная оптимизация):
- Выбор ратиометрического зондирования является критической "оптимизацией" конструкции. Принимая соотношение двух интенсивностей флуоресценции (либо от разных длин волн возбуждения для pH, либо от разных длин волн эмиссии для температуры), система автоматически отменяет многие общие источники шума. Это включает флуктуации интенсивности возбуждающего света, фотообесцвечивание индикатора, вариации концентрации индикатора и даже незначительные изменения оптических свойств волокна или эффективности связи.
- Этот механизм гарантирует, что соотношение сигнал/шум (SNR) остается высоким, а выход датчика стабильным и надежным, эффективно "оптимизируя" качество измерения в реальном времени без явных алгоритмических обновлений. Тесты на стабильность (рис. 2g,h,i,j и рис. 3j,k,l,n) подтверждают эту надежность, показывая минимальное стандартное отклонение и выщелачивание.
-
Обратная связь в замкнутом контуре для оптимизации терапии:
- Во время фактической фототермической терапии система работает как механизм управления с обратной связью. Датчик непрерывно предоставляет показания температуры и pH в реальном времени.
- Эти показания не используются для обновления внутренней математической модели датчика, а для регулировки внешнего терапевтического входа. Например, если контролируемая температура отклоняется от целевой тепловой дозы, мощность насосного лазера (терапевтический вход) соответствующим образом регулируется. Это классическая петля обратной связи: Сенсор (температура/pH) $\rightarrow$ Оценка (по отношению к цели) $\rightarrow$ Действие (регулировка мощности лазера).
- Эта итеративная корректировка терапевтического входа на основе данных датчика в реальном времени является способом оптимизации самой терапии для достижения желаемых результатов (например, поддержания температуры опухоли на уровне 65 °C на кончике волокна для обеспечения 45 °C на краю опухоли), минимизируя при этом побочные эффекты. Система сходится к целевому терапевтическому состоянию посредством непрерывного мониторинга и корректировки, делая лечение точным и адаптивным.
По сути, математический механизм "учится" своей характеристической реакции один раз во время калибровки, а затем надежно применяет эту выученную функцию. Общая "оптимизация" системы во время терапии достигается за счет надежной петли обратной связи в реальном времени, которая использует точные и стабильные измерения датчика для управления терапевтическим вмешательством.
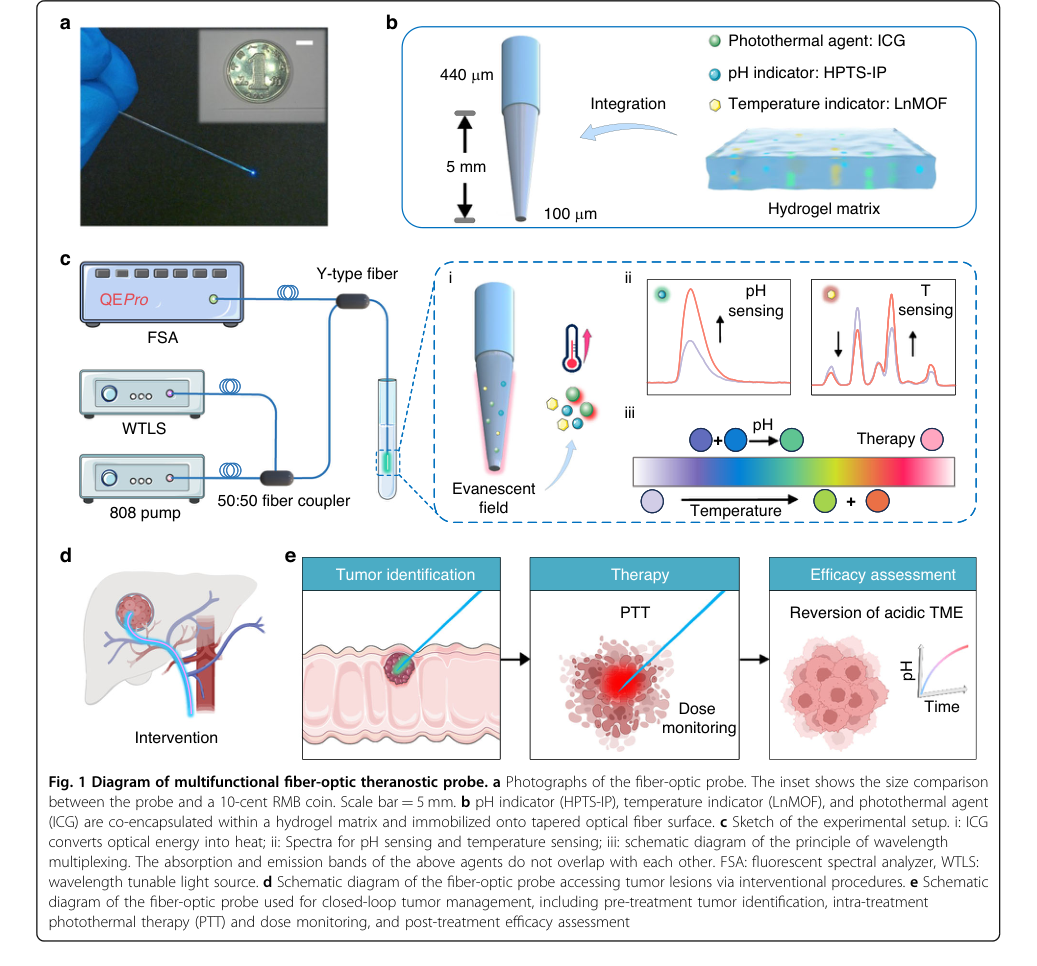 Figure 1. Diagram of multifunctional fiber-optic theranostic probe. a Photographs of the fiber-optic probe. The inset shows the size comparison between the probe and a 10-cent RMB coin. Scale bar = 5 mm. b pH indicator (HPTS-IP), temperature indicator (LnMOF), and photothermal agent (ICG) are co-encapsulated within a hydrogel matrix and immobilized onto tapered optical fiber surface. c Sketch of the experimental setup. i: ICG converts optical energy into heat; ii: Spectra for pH sensing and temperature sensing; iii: schematic diagram of the principle of wavelength multiplexing. The absorption and emission bands of the above agents do not overlap with each other. FSA: fluorescent spectral analyzer, WTLS: wavelength tunable light source. d Schematic diagram of the fiber-optic probe accessing tumor lesions via interventional procedures. e Schematic diagram of the fiber-optic probe used for closed-loop tumor management, including pre-treatment tumor identification, intra-treatment photothermal therapy (PTT) and dose monitoring, and post-treatment efficacy assessment
Figure 1. Diagram of multifunctional fiber-optic theranostic probe. a Photographs of the fiber-optic probe. The inset shows the size comparison between the probe and a 10-cent RMB coin. Scale bar = 5 mm. b pH indicator (HPTS-IP), temperature indicator (LnMOF), and photothermal agent (ICG) are co-encapsulated within a hydrogel matrix and immobilized onto tapered optical fiber surface. c Sketch of the experimental setup. i: ICG converts optical energy into heat; ii: Spectra for pH sensing and temperature sensing; iii: schematic diagram of the principle of wavelength multiplexing. The absorption and emission bands of the above agents do not overlap with each other. FSA: fluorescent spectral analyzer, WTLS: wavelength tunable light source. d Schematic diagram of the fiber-optic probe accessing tumor lesions via interventional procedures. e Schematic diagram of the fiber-optic probe used for closed-loop tumor management, including pre-treatment tumor identification, intra-treatment photothermal therapy (PTT) and dose monitoring, and post-treatment efficacy assessment
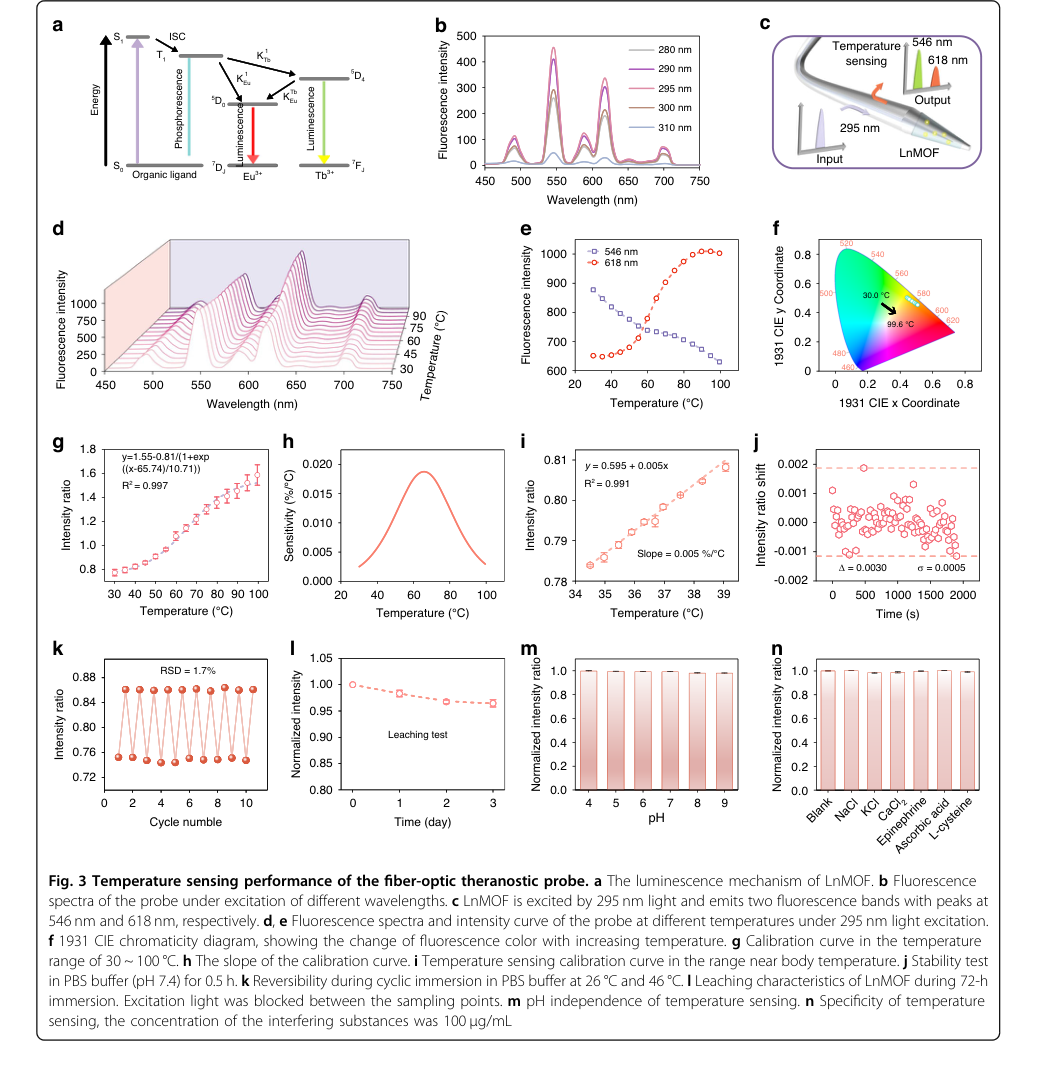 Figure 3. Temperature sensing performance of the fiber-optic theranostic probe. a The luminescence mechanism of LnMOF. b Fluorescence spectra of the probe under excitation of different wavelengths. c LnMOF is excited by 295 nm light and emits two fluorescence bands with peaks at 546 nm and 618 nm, respectively. d, e Fluorescence spectra and intensity curve of the probe at different temperatures under 295 nm light excitation. f 1931 CIE chromaticity diagram, showing the change of fluorescence color with increasing temperature. g Calibration curve in the temperature range of 30 ~ 100 °C. h The slope of the calibration curve. i Temperature sensing calibration curve in the range near body temperature. j Stability test in PBS buffer (pH 7.4) for 0.5 h. k Reversibility during cyclic immersion in PBS buffer at 26 °C and 46 °C. l Leaching characteristics of LnMOF during 72-h immersion. Excitation light was blocked between the sampling points. m pH independence of temperature sensing. n Specificity of temperature sensing, the concentration of the interfering substances was 100 μg/mL
Figure 3. Temperature sensing performance of the fiber-optic theranostic probe. a The luminescence mechanism of LnMOF. b Fluorescence spectra of the probe under excitation of different wavelengths. c LnMOF is excited by 295 nm light and emits two fluorescence bands with peaks at 546 nm and 618 nm, respectively. d, e Fluorescence spectra and intensity curve of the probe at different temperatures under 295 nm light excitation. f 1931 CIE chromaticity diagram, showing the change of fluorescence color with increasing temperature. g Calibration curve in the temperature range of 30 ~ 100 °C. h The slope of the calibration curve. i Temperature sensing calibration curve in the range near body temperature. j Stability test in PBS buffer (pH 7.4) for 0.5 h. k Reversibility during cyclic immersion in PBS buffer at 26 °C and 46 °C. l Leaching characteristics of LnMOF during 72-h immersion. Excitation light was blocked between the sampling points. m pH independence of temperature sensing. n Specificity of temperature sensing, the concentration of the interfering substances was 100 μg/mL
Результаты, ограничения и заключение
Экспериментальный дизайн и базовые уровни
Исследователи тщательно разработали свои эксперименты для строгой проверки многофункциональных возможностей и терапевтической эффективности своего нового волоконно-оптического тераностического зонда. Основу их экспериментальной архитектуры составляла демонстрация способности зонда выполнять три различные функции — определение pH, определение температуры и фототермическая терапия (ФТТ) — с использованием одного оптического волокна, используя мультиплексирование с разделением по длине волны для предотвращения перекрестных помех.
Для определения pH зонд, функционализированный HPTS-IP, тестировался в фосфатно-солевом буфере (PBS) в широком диапазоне pH (от 4,0 до 9,0) при комнатной температуре. Его стабильность оценивалась путем непрерывной спектральной записи в течение 150 секунд в PBS с pH 7,4. Обратимость была подтверждена чередованием погружения в буферы с pH 4,0 и 9,0 в течение пяти циклов. Характеристики выщелачивания оценивались в течение 72 часов в PBS с pH 7,4. Для подтверждения надежности в сложных биологических средах специфичность зонда тестировалась против распространенных мешающих веществ, таких как NaCl, KCl, CaCl₂, эпинефрин, аскорбиновая кислота и L-цистеин. Критически важно, что перекрестные помехи температуры оценивались путем варьирования температур от 26 до 41 °C при измерении pH.
Определение температуры с использованием LnMOF оценивалось в широком диапазоне (30-100 °C) и особенно в физиологически релевантном диапазоне (34,5-39 °C). Стабильность тестировалась в течение 0,5 часа в PBS с pH 7,4, а обратимость демонстрировалась в течение 10 циклов путем чередования погружения в PBS при 26 °C и 46 °C. Выщелачивание контролировалось в течение 72 часов, а независимость от pH подтверждалась тестированием в буферах от pH 4,0 до 9,0. Также оценивалась специфичность к мешающим веществам.
Для фототермического преобразования зонд, функционализированный ICG, подвергался in vitro тестам с использованием насосного лазера 808 нм, измеряя максимальные температуры при различных мощностях насоса (до 267 мВт). Фототермическая стабильность оценивалась в течение пяти циклов нагрева/охлаждения, а выщелачивание ICG контролировалось в течение 72 часов. "Жертвой" здесь было типичное требование к высокой мощности насоса в обычных наноматериальных системах ФТТ, которые часто превышают 1 Вт.
Окончательная валидация была проведена в ходе in vivo экспериментов с использованием моделей ксенографтов колоректального рака подкожной локализации у голых мышей BALB/c. Опухолям давали вырасти примерно до 100 мм³ перед вмешательством.
- Идентификация опухоли была тщательно протестирована путем введения зонда в опухолевую ткань, прилегающую нормальную ткань, поверхность опухоли и нормальную ткань, сравнивая измеренные значения pH.
- Мониторинг ФТТ и дозы включал введение зонда в центр опухоли и активное поддержание температуры волокна на уровне 65 °C в течение 15 минут, при этом тепловое изображение подтверждало, что край опухоли достигал эффективной терапевтической температуры 45 °C.
- Оценка эффективности была многосторонней: мониторинг pH в реальном времени в опухолевом микроокружении (ОМО) после лечения (через 30 минут и 24 часа), а также долгосрочный мониторинг объема опухоли и массы тела каждые 3 дня в течение 20 дней. "Жертвами" в этом контексте были мыши контрольной группы, не получавшие лечения, опухоли которых демонстрировали прогрессирующий рост, что приводило к эвтаназии при объеме более 2000 мм³.
- Биосовместимость оценивалась in vitro путем культивирования клеток HCT116 с вытяжкой зонда (24 часа) и проведения анализов CCK-8 и окрашивания на живые/мертвые клетки. In vivo биосовместимость органов (сердце, печень, селезенка, легкие, почки) оценивалась путем окрашивания H&E через 24 часа после лечения в группах имплантации (волокно без лазера) и лечения по сравнению с контрольными группами. Гистологический и иммуногистохимический анализ (каспаза-3, HIF-1α, Ki67) опухолевых тканей проводился через 24 часа после лечения, при этом группы, подвергшиеся фиктивной обработке (имплантация волокна без возбуждения лазером), служили базовым уровнем для сравнения.
Что доказывают доказательства
Представленные в статье доказательства однозначно подтверждают успешную разработку и функциональность многофункционального волоконно-оптического тераностического зонда, способного к фототермической терапии опухолей в замкнутом контуре с обратной связью в реальном времени.
Основное математическое утверждение о мультиплексировании с разделением по длине волны (WDM) для неперекрывающихся полос возбуждения было безжалостно доказано различными спектрами поглощения HPTS-IP (405 нм, 450 нм), LnMOF (295 нм) и ICG (790 нм), как показано на рис. 2b и рис. S7. Это спектральное разделение является неоспоримым доказательством того, что основной механизм переключения функций по требованию работает, эффективно устраняя перекрестные помехи между функциями, что является серьезным ограничением предыдущих систем с несколькими агентами.
Для определения pH зонд продемонстрировал исключительную производительность:
- Он достиг высокого разрешения 0,013 единиц pH в линейном диапазоне от 6,0 до 8,0, что имеет решающее значение для различения физиологических значений pH в нормальных и опухолевых тканях. Это было выведено из подгонки модели Больцмана (рис. 2f) и теста на стабильность, показывающего стандартное отклонение ($\sigma$) 0,0009 (рис. 2g).
- Отличная обратимость была подтверждена относительным стандартным отклонением (RSD) 0,8% в течение пяти циклов (рис. 2h), что указывает на стабильную производительность.
- Минимальное выщелачивание HPTS-IP (снижение интенсивности флуоресценции на 1,6% за 72 часа, рис. 2i) и отличная селективность против различных мешающих веществ (рис. 2j) дополнительно подтвердили его надежность в сложных биологических средах.
- Критически важно, что пренебрежимые перекрестные помехи температуры наблюдались в диапазоне pH от 4,0 до 7,0, а для pH > 7,0, встроенный мониторинг температуры зонда обеспечивает встроенную компенсацию, обеспечивая точное определение pH (рис. 2k).
Определение температуры также продемонстрировало надежную производительность:
- Ратиометрический подход, использующий термически усиленный перенос энергии от Tb³⁺ к Eu³⁺ (рис. 3a, c), позволил точно контролировать.
- Разрешение 0,3 °C было достигнуто, удовлетворяя требованиям in vivo мониторинга, с линейной зависимостью, наблюдаемой в физиологически релевантном диапазоне (34,5-39 °C) (рис. 3i).
- Высокая обратимость (RSD 1,7% в течение 10 циклов, рис. 3k) и минимальное выщелачивание LnMOF (снижение на 3,5% за 72 часа, рис. 3l) были продемонстрированы.
- Доказательства также подтвердили его независимость от pH (рис. 3m) и отличную специфичность (рис. 3n), обеспечивая точные показания температуры независимо от флуктуаций pH или других биологических интерферентов.
Фототермическая конверсионная способность зонда была однозначно установлена:
- При мощности возбуждения всего 267 мВт зонд нагревался in vitro до 102,9 °C (рис. 4b, c), подтверждая эффективное фототермическое преобразование. Это значительная победа над обычными наноматериальными системами, которые обычно требуют мощности насоса более 1 Вт, что делает этот подход более экономичным и снижает потенциальные побочные эффекты.
- Отличная фототермическая стабильность была показана стабильным повышением температуры в течение пяти циклов нагрева/охлаждения (рис. 4d) и минимальным выщелачиванием ICG (снижение на 5,9% за 72 часа, рис. 4g, h), что обеспечивало долгосрочную производительность.
- In vivo эксперименты подтвердили прогрессирующее повышение температуры в опухолевых областях с увеличением мощности насоса (рис. 4e, f).
In vivo валидация предоставила наиболее убедительные доказательства реальной полезности зонда:
- Идентификация границ опухоли была однозначно доказана статистически значимым различием в измеренных значениях pH между здоровыми и опухолевыми тканями (p < 0,0001) и между поверхностью опухоли и нормальной тканью (p < 0,01) (рис. 5a, b). Это является неоспоримым доказательством его диагностической способности.
- Точный контроль тепловой дозы во время ФТТ был продемонстрирован активным поддержанием температуры волокна на уровне 65 °C, что обеспечивало достижение краем опухоли эффективной терапевтической температуры 45 °C (рис. 5c).
- Быстрая оценка эффективности была подтверждена значительным повышением pH в ОМО после лечения (увеличение на 0,12-0,22 единицы в течение 30 минут и p < 0,01 через 24 часа) (рис. 5d, e, f), что служит надежным биомаркером терапевтического ответа.
- Окончательное доказательство противоопухолевой эффективности пришло из мониторинга объема опухоли: у 3 из 4 обработанных мышей наблюдалась полная регрессия опухоли, а у оставшейся мыши наблюдалось значительное подавление роста, в то время как контрольная группа "жертв" демонстрировала прогрессирующий рост опухоли (рис. 5g, h, i, j).
- Отличная биосовместимость и биобезопасность были подтверждены стабильной массой тела у всех мышей (рис. 5k), отсутствием значительных апоптотических/некротических областей или инфильтрации воспалительных клеток в органах, окрашенных H&E (рис. S10), и высокой жизнеспособностью клеток в тестах на вытяжку in vitro (рис. S9, рис. 6c).
- Наконец, мультимодальные противоопухолевые эффекты были подтверждены гистологическим анализом (рис. 6a), выявившим множественные очаги некроза и геморрагические области в обработанных опухолях. Иммуногистохимия показала повышенную экспрессию каспазы-3 (биомаркер апоптоза), пониженную экспрессию Ki67 (биомаркер пролиферации) и пониженную экспрессию HIF-1α, что указывает на снижение гипоксии опухоли, что было далее подтверждено МРТ (рис. 6b, рис. S8). Эти всесторонние доказательства неоспоримо подтверждают, что основной механизм зонда действительно работал на практике, приводя к эффективной абляции опухоли и ремоделированию ОМО.
Ограничения и будущие направления
Хотя представленный волоконно-оптический тераностический зонд демонстрирует замечательные возможности, важно признать определенные ограничения и рассмотреть направления для дальнейшего развития.
Одно из присущих ограничений, хотя и смягченное волоконно-оптической конструкцией, — это глубина проникновения света. Эванесцентное поле, хотя и обеспечивает локализованное зондирование, имеет небольшую глубину проникновения (рис. S5), что означает, что зонд в основном ощущает и обрабатывает непосредственную близость своей поверхности. Хотя это подходит для точных, локализованных вмешательств, более широкое объемное картирование ОМО может потребовать нескольких зондов или более продвинутых оптических стратегий. Время отклика для определения pH (до 12,8 с для уменьшения) и определения температуры (до 2,0 с для увеличения) хорошо подходит для многих приложений, но может быть ограничением для захвата чрезвычайно быстрых, миллисекундных физиологических динамик.
Другим практическим соображением является выщелачивание. Хотя в статье сообщается о минимальном выщелачивании HPTS-IP (1,6%), LnMOF (3,5%) и ICG (5,9%) за 72 часа, это не ноль. Для долгосрочных имплантируемых устройств даже минимальное хроническое выщелачивание может накапливаться или вызывать иммунные реакции в течение недель или месяцев, потенциально влияя как на производительность зонда, так и на безопасность пациента. Упоминание о блокировании возбуждающего света между точками выборки для минимизации фотообесцвечивания (подписи к рис. 2i, 3l) предполагает, что, хотя ратиометрическое детектирование помогает, фотообесцвечивание остается фактором, который может повлиять на очень длительный непрерывный мониторинг. Кроме того, хотя перекрестные помехи температуры для определения pH были компенсированы для pH > 7,0, они не были полностью пренебрежимыми во всем диапазоне pH, что указывает на тонкое взаимодействие, которое может потребовать более сложных алгоритмов компенсации в будущем. Выбор одного слоя покрытия, хотя и оптимизирован для SNR и времени отклика, подразумевает компромисс; более толстые пленки могут улучшить сигнал, но за счет более медленного отклика.
Заглядывая вперед, сама статья предлагает несколько захватывающих направлений. Стратегия интеграции может быть перенесена на гибкие полимерные и гидрогелевые оптические волокна для повышения механической совместимости и биосовместимости, открывая путь для долгосрочных имплантируемых устройств. Использование спектральных ресурсов и применение алгоритмов многопиковой подгонки могут еще больше расширить функциональные возможности, решая потенциальное перекрытие полос эмиссии по мере интеграции большего количества функций. Авторы также предлагают интегрировать систему с МРТ-термометрией для более точного мониторинга температуры края опухоли, что подразумевает, что текущее тепловое изображение может иметь ограничения по пространственному разрешению или глубине без этого дополнения.
Помимо явных предложений статьи, возникает несколько тем для обсуждения для дальнейшей разработки и эволюции:
-
Расширенная интеграция мультипараметров и обратная связь на основе ИИ: Сколько еще параметров ОМО (например, насыщение кислородом, уровни глюкозы, активность специфических ферментов, концентрации лекарств) можно одновременно интегрировать в одно волокно с использованием WDM или других методов мультиплексирования без ущерба для целостности сигнала или увеличения сложности устройства? Можно ли подавать данные в реальном времени от такого зонда в модель искусственного интеллекта (ИИ) или машинного обучения (МО) для создания действительно адаптивных, персонализированных протоколов лечения, которые динамически регулируют мощность лазера, продолжительность или даже доставку лекарств на основе развивающегося ОМО? Это могло бы выйти за рамки простых петель обратной связи к предиктивной, оптимизированной терапии.
-
Долгосрочная биостабильность и иммуномодуляция: Хотя краткосрочная биосовместимость доказана, каковы долгосрочные последствия хронической имплантации? Как биообрастание, инкапсуляция тканями хозяина или хронические воспалительные реакции влияют на точность зондирования и терапевтическую эффективность устройства в течение месяцев или лет? Может ли золь-гелевая матрица быть дополнительно разработана с иммуномодулирующими свойствами для активного содействия интеграции и минимизации неблагоприятных реакций, возможно, путем высвобождения противовоспалительных агентов или факторов роста?
-
Масштабируемость, миниатюризация и интеграция в клинический рабочий процесс: Текущий зонд имеет диаметр 440 мкм с кончиком 100 мкм. Можно ли его дальнейшую миниатюризацию для еще менее инвазивных процедур, или можно разработать массивы таких зондов для более крупных или мультифокальных опухолей? Каковы производственные проблемы и затраты, связанные с масштабированием производства для широкого клинического применения? Как такое сложное устройство интегрируется в существующие клинические рабочие процессы, учитывая потребность в специализированном обучении, оборудовании и интерпретации данных?
-
Неинвазивное наведение и комплементарные терапии: Можно ли адаптировать принципы этой тераностической системы с замкнутым контуром для наведения или усиления неинвазивных терапий? Например, может ли менее инвазивная версия зонда предоставлять обратную связь ОМО в реальном времени для оптимизации внешней лучевой терапии, фокусированного ультразвука или системной химиотерапии, а не только для абляции опухоли? Это расширило бы его применимость за пределы прямой абляции опухоли.
-
Этические соображения и опыт пациента: По мере того как эти устройства становятся все более сложными и имплантируемыми, каковы этические соображения относительно конфиденциальности данных, автономии пациента и потенциала чрезмерного лечения или непреднамеренных побочных эффектов от непрерывной, адаптивной терапии? Как можно оптимизировать опыт пациента, минимизируя дискомфорт и психологическую нагрузку, связанную с имплантируемыми устройствами и частым мониторингом?
Эти обсуждения подчеркивают огромный потенциал этой технологии, но также и сложные, междисциплинарные проблемы, которые необходимо решить для ее полной реализации и широкого воздействия в онкологии.
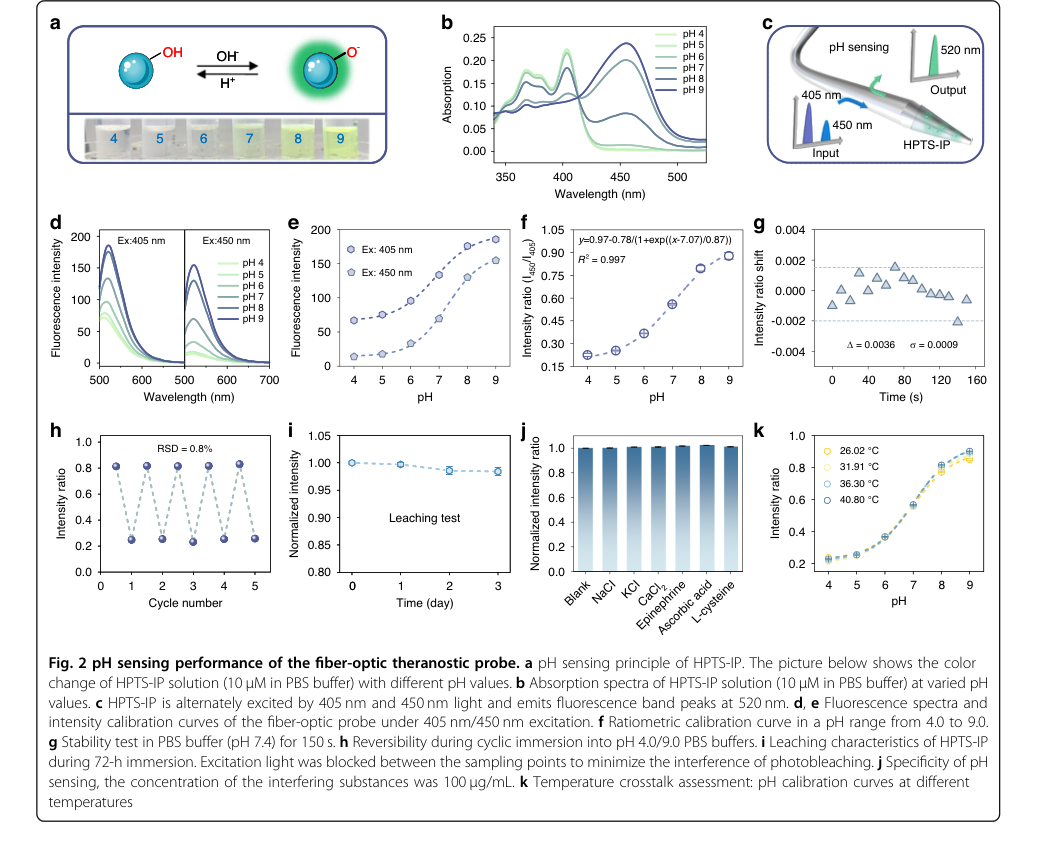 Figure 2. pH sensing performance of the fiber-optic theranostic probe. a pH sensing principle of HPTS-IP. The picture below shows the color change of HPTS-IP solution (10 μM in PBS buffer) with different pH values. b Absorption spectra of HPTS-IP solution (10 μM in PBS buffer) at varied pH values. c HPTS-IP is alternately excited by 405 nm and 450 nm light and emits fluorescence band peaks at 520 nm. d, e Fluorescence spectra and intensity calibration curves of the fiber-optic probe under 405 nm/450 nm excitation. f Ratiometric calibration curve in a pH range from 4.0 to 9.0. g Stability test in PBS buffer (pH 7.4) for 150 s. h Reversibility during cyclic immersion into pH 4.0/9.0 PBS buffers. i Leaching characteristics of HPTS-IP during 72-h immersion. Excitation light was blocked between the sampling points to minimize the interference of photobleaching. j Specificity of pH sensing, the concentration of the interfering substances was 100 μg/mL. k Temperature crosstalk assessment: pH calibration curves at different temperatures
Figure 2. pH sensing performance of the fiber-optic theranostic probe. a pH sensing principle of HPTS-IP. The picture below shows the color change of HPTS-IP solution (10 μM in PBS buffer) with different pH values. b Absorption spectra of HPTS-IP solution (10 μM in PBS buffer) at varied pH values. c HPTS-IP is alternately excited by 405 nm and 450 nm light and emits fluorescence band peaks at 520 nm. d, e Fluorescence spectra and intensity calibration curves of the fiber-optic probe under 405 nm/450 nm excitation. f Ratiometric calibration curve in a pH range from 4.0 to 9.0. g Stability test in PBS buffer (pH 7.4) for 150 s. h Reversibility during cyclic immersion into pH 4.0/9.0 PBS buffers. i Leaching characteristics of HPTS-IP during 72-h immersion. Excitation light was blocked between the sampling points to minimize the interference of photobleaching. j Specificity of pH sensing, the concentration of the interfering substances was 100 μg/mL. k Temperature crosstalk assessment: pH calibration curves at different temperatures
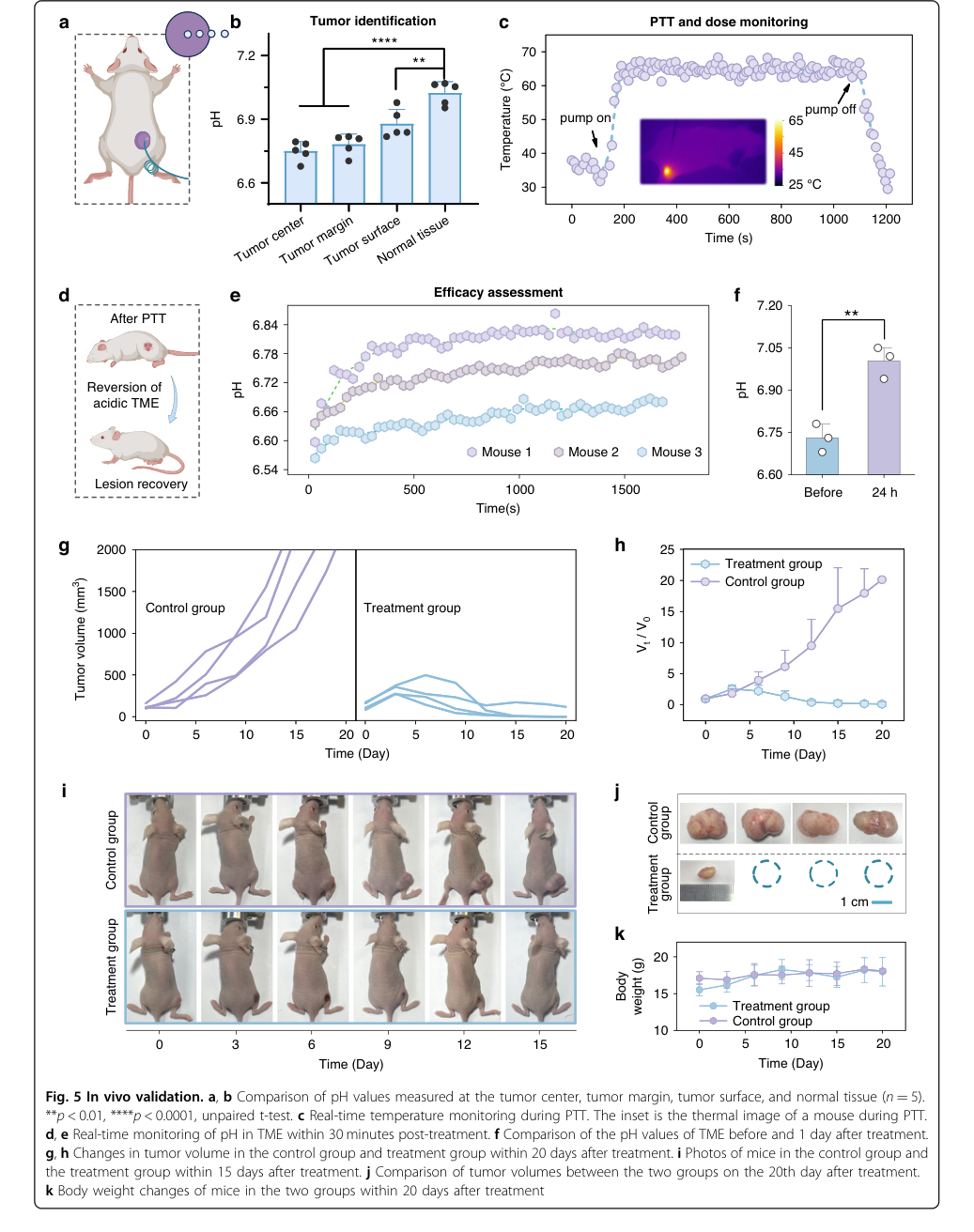 Figure 5. In vivo validation. a, b Comparison of pH values measured at the tumor center, tumor margin, tumor surface, and normal tissue (n = 5). **p < 0.01, ****p < 0.0001, unpaired t-test. c Real-time temperature monitoring during PTT. The inset is the thermal image of a mouse during PTT. d, e Real-time monitoring of pH in TME within 30 minutes post-treatment. f Comparison of the pH values of TME before and 1 day after treatment. g, h Changes in tumor volume in the control group and treatment group within 20 days after treatment. i Photos of mice in the control group and the treatment group within 15 days after treatment. j Comparison of tumor volumes between the two groups on the 20th day after treatment. k Body weight changes of mice in the two groups within 20 days after treatment
Figure 5. In vivo validation. a, b Comparison of pH values measured at the tumor center, tumor margin, tumor surface, and normal tissue (n = 5). **p < 0.01, ****p < 0.0001, unpaired t-test. c Real-time temperature monitoring during PTT. The inset is the thermal image of a mouse during PTT. d, e Real-time monitoring of pH in TME within 30 minutes post-treatment. f Comparison of the pH values of TME before and 1 day after treatment. g, h Changes in tumor volume in the control group and treatment group within 20 days after treatment. i Photos of mice in the control group and the treatment group within 15 days after treatment. j Comparison of tumor volumes between the two groups on the 20th day after treatment. k Body weight changes of mice in the two groups within 20 days after treatment
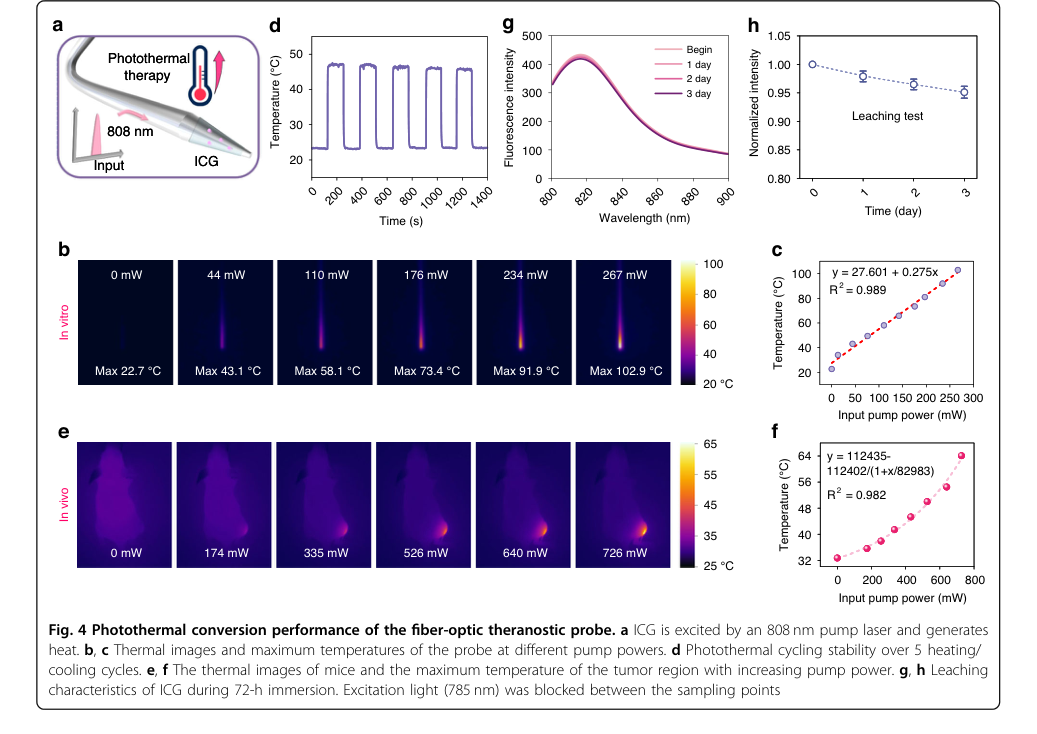 Figure 4. Photothermal conversion performance of the fiber-optic theranostic probe. a ICG is excited by an 808 nm pump laser and generates heat. b, c Thermal images and maximum temperatures of the probe at different pump powers. d Photothermal cycling stability over 5 heating/ cooling cycles. e, f The thermal images of mice and the maximum temperature of the tumor region with increasing pump power. g, h Leaching characteristics of ICG during 72-h immersion. Excitation light (785 nm) was blocked between the sampling points
Figure 4. Photothermal conversion performance of the fiber-optic theranostic probe. a ICG is excited by an 808 nm pump laser and generates heat. b, c Thermal images and maximum temperatures of the probe at different pump powers. d Photothermal cycling stability over 5 heating/ cooling cycles. e, f The thermal images of mice and the maximum temperature of the tumor region with increasing pump power. g, h Leaching characteristics of ICG during 72-h immersion. Excitation light (785 nm) was blocked between the sampling points
