マルチチューブ電圧vBMD測定:二分岐周波数バランスと非対称チャネルアテンションによる
Phantom-less volumetric bone mineral density (vBMD) measurement using computed tomography (CT) presents a cost-effective alternative to conventional phantom-based approaches, yet faces accuracy challenges across...
背景と学術的系譜
本稿で取り組む問題の正確な起源を理解するためには、医師が骨粗鬆症をどのように診断するかを考察する必要がある。骨強度を評価するためのゴールドスタンダードは、体積骨密度(vBMD)の測定である。歴史的には、これは定量CT(QCT)を用いて行われていたが、CTスキャン中に「ファントム」として知られる物理的な校正オブジェクトを患者の下に配置する必要があった。本稿では、これらの物理ファントムが高価であると指摘しているが、正直なところ、テキストだけでは正確な臨床価格は不明である。しかし、医用画像処理において、特殊な校正ハードウェアはセッションあたり150ドル以上、あるいはそれ以上になることも容易であり、頻繁な再校正の手間は言うまでもない。
これを回避するため、医療分野では「ファントムレス」(PL)手法が開発された。これらの手法は、外部オブジェクトの代わりに、患者自身の内部組織(脂肪や筋肉など)を参照点として骨密度を計算する。最近では、このプロセスを自動化するために深層ニューラルネットワーク(DNN)が導入されている。
しかし、現代の臨床実践の変化により、大きな「ペインポイント」が出現した。患者を過剰な放射線被曝から保護するため、病院ではCTスキャナの管電圧を標準の120 kVpから80 kVpまたは100 kVpへと低下させる傾向にある。従来のDNNモデルの根本的な限界は、120 kVpスキャンに厳密に最適化されていたことである。低電圧画像を入力すると、全体の明るさとコントラスト(CT減衰)が劇的に変化する。これらのグローバルな強度変化(低周波情報)に大きく依存していた従来のモデルは、性能が著しく低下し、最大で $20 \text{ mg/cm}^3$ の推定誤差を生じる。放射線量に関わらず安定している骨の微細で海綿状のテクスチャ(高周波情報)を完全に捉えられない。さらに、これらの周波数を分離するための従来の計算方法は、3D医用画像には実用的には重すぎる。
科学を直感的に理解してもらうために、以下にいくつかの高度に専門的なドメイン用語を日常的な概念に翻訳する。
- ファントムレス(PL)vBMD測定: 写真に写ったリンゴの重さを推測しようとしていると想像してほしい。「ファントム」法では、比較のためにリンゴの隣に標準的な1ポンドの金属製重りを置く必要がある。「ファントムレス」法は、写真にすでに写っているもの、つまりリンゴが置かれている皿の大きさと比較してリンゴの重さを推測するようなもので、外部ツールを持ち込むのではなく、写真内のものを使用する。
- 管電圧(kVp): 写真を撮るために使用される懐中電灯の明るさだと考えてほしい。高電圧(120 kVp)は、すべてをはっきりと見せるが多くのエネルギー(放射線)を消費する、まぶしいほどの明るい光である。低電圧(80 kVp)は、被写体にとってより安全な暗い光であるが、結果として得られる画像が異なり、古いコンピュータプログラムを混乱させる。
- 骨小梁構造: 骨の内部構造は固い岩ではなく、むしろ剛性のあるスポンジやハニカム構造のように見える。この用語は、骨の内部にあるその複雑で多孔質なネットワークを指す。
- 周波数分解: 交響曲を聴いていると想像してほしい。このプロセスは、オーディオイコライザーを使用して、深い重低音(低周波:骨の全体的な形状と位置)と、バイオリンのシャープでクリアな音(高周波:骨の内部の微細で海綿状のテクスチャ)を分離するようなものである。
これを解決するために、著者らは周波数を分離・バランスさせる軽量なデュアルブランチニューラルネットワークを設計した。数学的には、重い計算なしに高周波の詳細を抽出し、非対称チャネルアテンションメカニズムを使用して各周波数帯の重要度を重み付けする。
以下に、彼らが周波数変調と特徴融合を数学的に解釈し、解決する方法を示す。
まず、フーリエ変換と空間アテンションメカニズムを用いて周波数特徴を変調する。
$$ Y = \sum_{b \in B} \sigma(f(X_b; W_b)) \odot X_b $$
$$ X_b = \mathcal{F}^{-1}(M_b \odot \mathcal{F}(X)) $$
その後、低周波と高周波の特徴を融合してアテンション重みを生成し、ネットワークが最も重要な情報に焦点を当てるようにする。
$$ \widetilde{X} = upsample(X_L) + X_H $$
$$ A_H = \sigma(MLP(GMP(\widetilde{X}))) $$
$$ A_L = \sigma(MLP(GAP(\widetilde{X}))) $$
最後に、これらのアテンション重みを適用して、特徴をそれぞれのドメインに分離する。
$$ X = A_H \odot X_H + A_L \odot X_L $$
以下は、彼らのアーキテクチャを理解するために必要な主要な数学的記法を整理した表である。
| 記法 | 説明 |
|---|---|
| $X$ | 入力特徴マップ、$X \in \mathbb{R}^{C,D,H,W}$ として3D空間で定義される |
| $Y$ | 周波数変調後の出力特徴マップ |
| $\mathcal{F}, \mathcal{F}^{-1}$ | フーリエ変換とその逆変換 |
| $M_b$ | 特定の周波数帯を分離するために使用されるバイナリ周波数マスク |
| $W$ | 畳み込みパラメータ(重み) |
| $X_L, X_H$ | 分離された低周波および高周波の特徴成分 |
| $Y_L, Y_H$ | 処理された低周波および高周波の特徴 |
| $A_L, A_H$ | 低周波および高周波のチャネルアテンションマップ |
| $\widetilde{X}$ | 再分割前の融合特徴マップ |
| $AP(x)$ | $2 \times 2 \times 2$ カーネルを用いた平均プーリング操作 |
| $upsample(x)$ | 最近傍補間アップサンプリング操作 |
| $\sigma$ | シグモイド活性化関数 |
| $\odot$ | アダマール積(要素ごとの乗算) |
問題定義と制約
スポンジの重さを量ろうとしているが、体重計に乗せるのではなく、写真を見ただけで重さを推測しなければならないと想像してみよう。さらに、部屋の照明が常に変化するとしたらどうだろうか。明るい時もあれば、暗い時もある。これは、物理的な校正ツール(「ファントム」)を使用せずにCTスキャンから骨密度を測定しようとする医師が直面する課題と全く同じである。
出発点と目標点
入力(現状): 患者の椎体(vertebral bodies)の3Dコンピュータ断層撮影(CT)画像から開始する。これらのスキャンは、管電圧(tube voltage)(通常80、100、または120 kVp)として知られる様々な放射線レベルで撮影される。
出力(目標状態): 目標は、$mg/cm^3$で表される、非常に精度の高い体積骨密度(volumetric Bone Mineral Density, vBMD)測定値を出力することである。
数学的なギャップ:
従来、医師は骨密度を、組織がX線をどれだけ遮断するかを示す数学的表現であるハンスフィールドユニット(Hounsfield Unit, HU)を見て測定していた。ここでの欠けているリンクは、HU値がX線管電圧に厳密に依存していることである。病院が過剰な放射線から患者を救うために電圧を下げると、全く同じ骨のHU値は大幅に低下する。著者らは、非常に変動しやすく、電圧に依存する3D空間強度行列 $X \in \mathbb{R}^{C,D,H,W}$ を、スキャナーの設定に完全に依存しない、安定した絶対密度値にマッピングする数学的な橋を構築する必要があった。
苦痛なジレンマ
コンピュータビジョンの世界では、一つの側面を改善すると、常に別の側面が悪化する。この特定の問題において、以前の研究者たちは「周波数抽出と計算コスト」の過酷なトレードオフに囚われていた。
これを理解するためには、画像を2つの「周波数」に分割する必要がある。
1. 低周波特徴(Low-frequency features): 脊椎の全体的な輪郭のような、広範で巨視的な形状。これらは標準的なニューラルネットワークが学習しやすく、モデルが骨を素早く特定するのに役立つ。しかし、これらは管電圧の変化に非常に敏感である。
2. 高周波特徴(High-frequency features): 骨のスポンジ状の微細構造のような、微細で細かい構造(海綿骨構造)。これらの特徴は、異なる電圧間で信じられないほど安定しており、骨粗鬆症の真の指標である。
ここにジレンマがある。標準的なディープニューラルネットワーク(DNN)は、自然に低周波情報を優先する。ネットワークに高周波3Dテクスチャに注意を払うように強制したい場合、従来は深い複雑なネットワークや、3Dウェーブレット変換のような重い数学的操作を使用する必要があった。しかし、これを3D空間で行うと、メモリと処理要件が指数関数的に爆発する。病院がCT電圧を変更したときに失敗する軽量なモデルか、標準的な臨床ハードウェアでは実行するには大きすぎて遅すぎる堅牢なモデルかのどちらかになる。
過酷な壁と制約
著者らは、この問題を解決することを非常に困難にする、いくつかの過酷で現実的な壁に直面した。
- 臨床放射線壁(The Clinical Radiation Wall): 患者の放射線被曝量を削減するため、スキャンを120 kVpから80 kVpに引き下げるという世界的な大きな動きがある。これらの低い電圧では、全体的な強度測定は根本的に信頼できなくなる。モデルは、精度を失うことなく、これらのより暗く、より低エネルギーのスキャンに適応しなければならない。
- 疾患の物理的な疎性(The Physical Sparsity of the Disease): 骨粗鬆症は文字通り骨の消失である。疾患が進行するにつれて、海綿骨は極めて疎になる。ネットワークは、積極的に消失している微細なテクスチャ特徴を探すことを強いられる。
- 3D計算ボトルネック(The 3D Computational Bottleneck): 医療画像は平坦な2D画像ではなく、巨大な3Dボリュームである。奥行き、高さ、幅全体にわたって従来の周波数分解(繰り返しフーリエ変換のような)を適用するには、膨大なメモリが必要となる。著者らは、重い数学に頼らずに周波数を分離する方法を見つける必要があり、代わりに平均プーリング(average pooling)を使用して低周波を抽出し、それを元の画像から差し引いて高周波を見つけるという巧妙なトリックを採用した。
- 特徴混合トラップ(The Feature Mixing Trap): 低周波と高周波を並列に処理しようとすると(デュアルブランチネットワーク)、標準的な畳み込み層は意図せず情報を再び混合してしまう傾向がある。著者らは、高周波ブランチが微細な詳細のみに注目し、低周波ブランチが広範な形状のみに注目するように、厳密な数学的ゲートキーパー、すなわち非対称チャネルアテンションメカニズム(asymmetric channel attention mechanism)を設計する必要があった。これは、特徴マップ $X$ を低周波 ($X_L$) と高周波 ($X_H$) の成分に分離することによって数学的に定義される。
$$X = upsample(X_L) + X_H$$
要するに、著者らは、骨の微細で消失しつつある構造を3Dで捉え、X線装置の「照明」の変化を無視し、すべてを厳格な計算予算内で実行できるシステムを構築する必要があった。
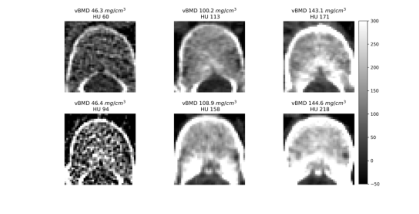 Figure 1. Intuitive comparison of features in vBMD measurement. The first row shows vertebral bodies with varying bone densities at 120 kVp. The second row shows corresponding vertebral bodies at non-120 kVp, where vBMD texture remains similar, but HU values within the VOI differ significantly. Low vBMD vertebral bodies exhibit both reduced HU values and a sparser trabecular structure in the measurement area
Figure 1. Intuitive comparison of features in vBMD measurement. The first row shows vertebral bodies with varying bone densities at 120 kVp. The second row shows corresponding vertebral bodies at non-120 kVp, where vBMD texture remains similar, but HU values within the VOI differ significantly. Low vBMD vertebral bodies exhibit both reduced HU values and a sparser trabecular structure in the measurement area
このアプローチの理由
著者が、標準的な3次元畳み込みニューラルネットワーク(CNN)、Vision Transformer、またはDiffusionモデルのような従来の最先端(SOTA)手法が、この問題に対して根本的に不十分であると認識した正確な瞬間は、管電圧の変化下でのCTスキャンの物理的挙動を分析したときであった。放射線被曝を低減するため、現代のクリニックではCT管電圧を標準の$120$ kVpから$100$ kVpまたは$80$ kVpに低下させることが多い。しかし、この電圧の低下は、グローバルなハンスフィールドユニット(HU)値(放射線密度を示す標準的な尺度)を劇的に変化させる。標準的なCNNは、画像の全体的な形状とグローバルな強度に対応する低周波情報を自然に優先する。これらの低周波グローバル強度は電圧変化に非常に敏感であるため、$120$ kVpのデータで学習された標準モデルは、$80$ kVpのデータでテストされると大幅な性能低下を経験し、$20$ $mg/cm^3$までの誤差を生じる。
著者は決定的な洞察を得た。グローバルな強度は電圧とともに変動するが、高周波特徴、特に骨の微細でスポンジ状の骨梁微細構造は、構造的に安定したままであるということだ。したがって、巨視的な形状を優先して高周波テクスチャの詳細をぼかす標準的なネットワークは、失敗する運命にあった。これらの周波数ドメインを別々に処理する必要があった。
単純な性能指標を超えて、この手法は3次元医用画像処理の膨大な計算負荷を処理する方法において、質的にも優れている。従来の周波数ドメイン手法は、通常、ウェーブレット変換やマルチスケール畳み込みカーネルのような計算集約的な技術に依存して周波数を分離する。これを大規模な3次元ボリュームCTデータに適用すると、メモリ複雑度が急増し、臨床現場ではモデルが実質的に使用不能になる。著者は、各層で重い数学的変換を放棄することによって、大幅な構造的利点を達成した。代わりに、彼らは非常にシンプルな分離手法を導入した。平均プーリングを使用して特徴マップをダウンサンプリングすることで低周波成分($X_L$)を抽出し、元の特徴マップとアップサンプリングされた低周波マップとの差を計算することで高周波成分($X_H$)を導き出す。数学的には、これは次のように表される。
$$X_H = X - \text{upsample}(X_L)$$
これは、重い信号処理の必要性をエレガントに回避する。さらに、ネットワーク全体でフーリエ変換を繰り返し適用することによる大規模なオーバーヘッドを回避するため、局所的な特徴抽出が最も重要である浅い層に周波数変調を限定した。
この選択されたアーキテクチャは、問題の厳しい制約とソリューションのユニークな特性との完璧な「結婚」を表している。制約は、モデルが外部キャリブレーションファントムに依存することなく、さまざまなCT管電圧にわたって一般化する必要があり、同時に重い3次元データを効率的に処理する必要があることを示している。デュアルブランチアーキテクチャはこれに完全に適合している。ネットワークを分割することにより、モデルは巨視的な椎骨の解剖学的構造(低周波)を理解するためのより深いパスと、繊細な骨梁構造(高周波)を捉えるためのより浅いパスを使用する。それらを融合するために、非対称チャネルアテンションメカニズムを利用する。グローバル最大プーリング(GMP)を適用してシャープで安定した高周波詳細を強調し、グローバル平均プーリング(GAP)を滑らかな低周波データに使用する。
$$A_H = \sigma(MLP(GMP(\tilde{X})))$$
$$A_L = \sigma(MLP(GAP(\tilde{X})))$$
これにより、安定した骨梁特徴が最終的なボリューム骨密度(vBMD)測定を積極的にガイドし、モデルが電圧誘発性の強度シフトに対して非常に堅牢になる。
最後に、これにより、敵対的生成ネットワーク(GAN)やDiffusionモデルのような他の一般的なアプローチがここで壊滅的に失敗した理由が説明される。生成モデルは、欠落しているデータ分布を合成または幻覚するように設計されている。骨粗鬆症の診断に必要な正確な物理測定が求められる定量的医用画像処理において、構造データを幻覚することは臨床的に危険である。さらに、これらのモデルは悪名高いほど重い。著者は、標準的な2次元DNNを3次元に拡張することさえ「過剰な計算リソース」を必要とすると明記している。3次元ボリュームCTスキャンに対して大規模なTransformerまたは多段階のDiffusionプロセスを展開することは、計算的に麻痺し、安定した構造テクスチャを抽出することを目的とした回帰タスクには全く不要である。軽量で周波数バランスの取れたデュアルブランチネットワークは、絶対的な精度に対する臨床的需要と効率性に対するエンジニアリング需要の両方を満たす唯一の実行可能な経路であった。
数学的・論理的メカニズム
この論文の核心を理解するためには、まずそれが解決する物理的な問題を理解する必要がある。医師がCTスキャンを用いて骨密度(vBMD)を測定する際、通常は特定のX線管電圧、典型的には120 kVpに依存する。しかし、現代のクリニックでは、患者への放射線被曝を低減するために、より低い電圧(80 kVpや100 kVpなど)へと移行している。問題は何か?電圧を下げると、CT画像の全体的な明るさとコントラスト(ハンスフィールドユニット)が劇的に変化する点である。
もしディープラーニングモデルが120 kVpでの全体的な明るさ(低周波データ)を記憶してしまえば、80 kVpでは悲惨な結果となるだろう。しかし、骨の微細な海綿骨構造(高周波データ)は、電圧に関わらず物理的に安定している。著者らは、画像を低周波と高周波に分割し、それらの重要度を動的に重み付けし、再び融合する、巧妙なデュアルブランチニューラルネットワークを設計した。
このクロス電圧汎化を可能にする、まさに核心となる数学的エンジンがこれである。
$$ \widetilde{X}_{base} = upsample(X_L) + X_H $$
$$ A_H = \sigma(MLP(GMP(\widetilde{X}_{base}))) $$
$$ A_L = \sigma(MLP(GAP(\widetilde{X}_{base}))) $$
$$ \widetilde{X}_{coupled} = A_H \odot X_H + A_L \odot X_L $$
$$ Y_L = AP(\widetilde{X}_{coupled}) $$
$$ Y_H = \widetilde{X}_{coupled} - upsample(Y_L) $$
(注:著者らは$\widetilde{X}$を初期融合状態と注意機構で結合された状態の両方を表すために使用している。時系列的な変換をより明確にするために、'base'と'coupled'の添え字を追加した。)
このエンジンがどのように機能するかを理解するために、一つずつ分解してみよう。
- $X_L$ および $X_H$: これらは低周波および高周波ブランチの入力特徴マップである。$X_L$は骨の巨視的でぼやけた形状(電圧変化に非常に敏感)を表す。$X_H$はシャープで微細な海綿骨のメッシュ(電圧間で安定)を表す。
- $upsample()$: 最近傍補間によるアップサンプリング関数。低周波特徴はメモリを節約するためにプーリングされダウンサンプリングされることが多いが、高周波特徴と相互作用するためには、それらと同じ空間次元に引き伸ばす必要がある。
- $+$ (加算): なぜ連結ではなく加算なのか?連結はメモリフットプリントを倍増させる。加算は物理的な重ね合わせとして機能する――ぼやけたカラーマップの上にシャープなテクスチャマップを同じ数学的空間に直接追加するようなものである。
- $GMP()$ および $GAP()$: Global Max Pooling および Global Average Pooling。ここで骨の物理学が関わってくる。$GMP$は、絶対的に最もシャープで最も高強度のスパイクを検出するレーダーとして機能する(硬い海綿骨構造を分離するのに最適)。$GAP$は、領域の全体的な環境エネルギーまたは平均密度を計算する。
- $MLP()$: Multi-Layer Perceptron(小さなニューラルネットワーク)。これは、プーリングされた統計情報を見て、骨密度を予測するために実際にどの特徴チャネルが有用かを決定する「脳」として機能する。
- $\sigma$ (シグモイド関数): これはMLPの出力を0から1の範囲に圧縮する。これは一連の調光器として機能する。
- $A_H$ および $A_L$: 高周波および低周波に対する結果的なアテンションウェイトである。
- $\odot$ (アダマール積): 要素ごとの乗算。なぜ加算ではなく乗算なのか?これはゲーティングメカニズムだからである。特定の低周波チャネルが電圧変化によって過度に破損していると判断された場合、対応する$A_L$の値は0.1となり、そのチャネルを効果的にミュートする。高周波チャネルが重要な構造データを含んでいる場合、$A_H$の値は0.9となり、それを増幅する。
- $AP()$: $2 \times 2 \times 2$カーネルを用いたAverage Pooling。これはローパスフィルタとして機能し、新たに結合されたマスター特徴マップを平滑化して、洗練された低周波出力$Y_L$を抽出する。
- $-$ (減算): $Y_H$を得るために減算を用いるのはなぜか?これは残差論理の美しい応用である。高周波は数学的に「低周波でないすべて」として定義される。平滑化されたベース($upsample(Y_L)$)をマスター結合マップ($\widetilde{X}_{coupled}$)から差し引くことで、ネットワークは計算負荷の高い複雑なフーリエ変換をこの段階で必要とすることなく、シャープな高周波ディテールを完全に分離する。
ステップバイステップの流れ
3次元の生CTデータブロックが機械的な組み立てラインに入る様子を想像してほしい。
まず、データは2つの別々のコンベアベルトに分割される。一つはぼやけた全体的な骨の形状($X_L$)を運び、もう一つはシャープな海綿骨のテクスチャ($X_H$)を運ぶ。ぼやけた形状は、シャープなテクスチャと同じサイズになるように物理的に引き伸ばされ($upsample$)、2つは重ね合わされて複合ブロック($\widetilde{X}_{base}$)が作成される。
次に、この複合ブロックは2つの特殊センサーの下を通過する。最初のセンサー($GMP$)は最もシャープで極端な構造スパイクをスキャンする。2番目のセンサー($GAP$)は全体的な環境密度を測定する。これらの測定値は中央コンピューター($MLP$)に供給され、各特徴チャネルの信頼度が正確に計算される。
コンピューターは2組のダイヤル($A_H$と$A_L$)を出力する。これらのダイヤルは元のコンベアベルトに適用され、関連性の低い、またはノイズの多いチャネルを減光し、非常に高い関連性のあるチャネルをブーストする。最適化されたベルトは、マスターの結合ブロック($\widetilde{X}_{coupled}$)にマージされる。
最後に、このマスターブロックは平滑化マシン($AP$)を通してプレスされ、新たに洗練された安定したぼやけた形状($Y_L$)が作成される。洗練されたシャープなテクスチャ($Y_H$)を得るために、マシンはマスターブロックからぼやけた形状を単純にスライスして($-$)取り除く。完全にバランスの取れた更新された2つのコンポーネントは、アーキテクチャの次のステージへと進む。
最適化ダイナミクス
このメカニズムは実際にどのように学習し、収束するのか?ネットワークは、120 kVpで取得されたゴールドスタンダードのファントムベースの測定値に対して、回帰損失(平均絶対誤差など)を用いてエンドツーエンドでトレーニングされる。
このアーキテクチャは加算と減算に大きく依存しているため、損失ランドスケープは驚くほど滑らかである。微積分では、加算または減算操作の局所的な微分は正確に1(または-1)である。これは、ネットワークがエラーを犯したときに、勾配信号が$Y_H$および$Y_L$の等式を劣化または消失させることなく逆方向に流れることを意味する。
トレーニングが進むにつれて、$MLP$は継続的なフィードバックを受け取る。もしモデルが、80 kVpスキャンによって人工的に暗くなった低周波チャネルに過度に依存したために骨密度を過大評価した場合、勾配は$MLP$に「次回この特定の変動を検出した際には、$A_L$の調光器を下げてください」と伝える。時間とともに、ネットワークは動的に注意をシフトすることを学習する。低電圧スキャンの混乱するグローバル強度シフトを検出すると、安定した高周波海綿骨特徴に自動的にさらに依存するようになる。
正直なところ、著者らが具体的にどのオプティマイザ(例:Adam、SGD)または学習率スケジューラを使用したのか、提供されたテキストにハイパーパラメータの詳細が明示されていないため、完全には確信が持てない。しかし、構造設計自体――特に残差分離と非対称アテンション――は、自然な正則化器として機能する。それは、モデルが単一のX線管電圧の絶対的なハンスフィールドユニットに過剰適合するのを防ぎ、代わりに骨の根本的な物理的現実を学習するように強制する。
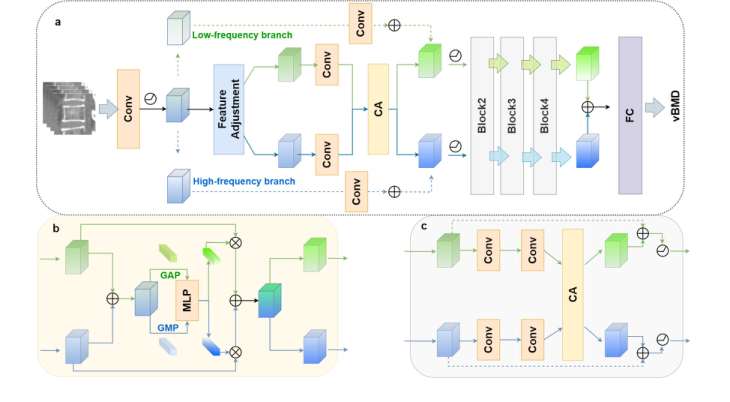 Figure 2. The proposed network. The proposed network adopts a dual-branch ar- chitecture consisting of four distinct modules (a). The first module is responsible for spatial reallocation of feature maps in the frequency domain. The following modules incorporate convolutional layers designed to perform coupling and re-decoupling oper- ations, guided by a channel attention mechanism (b and c). This design facilitates the effective fusion of frequency features, thereby enhancing the model’s ability to dynam- ically process both low- and high-frequency information.CA, channel attention; FC, fully connected
Figure 2. The proposed network. The proposed network adopts a dual-branch ar- chitecture consisting of four distinct modules (a). The first module is responsible for spatial reallocation of feature maps in the frequency domain. The following modules incorporate convolutional layers designed to perform coupling and re-decoupling oper- ations, guided by a channel attention mechanism (b and c). This design facilitates the effective fusion of frequency features, thereby enhancing the model’s ability to dynam- ically process both low- and high-frequency information.CA, channel attention; FC, fully connected
結果、限界および結論
建物の構造的完全性を判断しようとしているが、写真を見るしか許されていないと想像してほしい。さらに、一部の写真は明るい昼間に撮影され、他は安価なカメラで夕暮れ時に撮影されている。照明によって建物の全体的な色と明るさは劇的に変化するが、コンクリートの微細なひび割れ、すなわち高周波のディテールは一貫している。
これは、コンピューテッド・トモグラフィー(CT)スキャンを用いて骨粗鬆症を診断するために、体積骨密度(vBMD)を測定する際に医師が直面する問題と全く同じである。
歴史的に、病院ではスキャン中に患者の下に置かれる「ファントム」と呼ばれる物理的な校正オブジェクト(非常に高価で、処置のオーバーヘッドに150米ドル以上の費用を追加することもある)を使用して、ベースライン密度基準を提供していた。コストを削減するため、患者自身の脂肪と筋肉を参照点として使用する「ファントムレス」(PL)手法が開発された。しかし、大きな制約が生じた。現代のクリニックでは、患者を保護するためにCTスキャンの放射線量を低減しており(管電圧を120 kVpから80または100 kVpに低下させている)、この根本的な変化がハンスフィールドユニット(CTスキャンにおけるピクセル強度値)を変化させる。従来のAIモデルは、「全体像」の全体的な明るさ(低周波データ)に大きく依存しているため、この電圧低下によって完全に混乱し、測定誤差が大きくなる。
本論文の著者らは、ある素晴らしいことに気づいた。低放射線量で骨の全体的な明るさは変化するが、骨の微細なスポンジ状の構造(小柱構造)は変化しないということである。彼らは、変化する照明を無視して、コンクリートのひび割れに焦点を当てることができるAIを必要としていた。
数学的コア:現実の分離と変調
これを解決するために、著者らは厳しい計算上の制約を克服しなければならなかった。高周波3Dテクスチャの抽出には、通常、マルチスケールウェーブレット変換のような非常に重い数学が必要であり、これは標準的な病院用コンピュータをクラッシュさせるだろう。
代わりに、彼らは画像を個別のパスに分割する軽量なデュアルブランチネットワークを設計した。まず、単純な平均プーリング操作を使用して低周波の「ぼやけた」データ($X_L$)を抽出する。次に、このぼやけた画像を元の画像から減算して、高周波の「シャープな」ディテール($X_H$)を分離する。
ネットワークがシステムを遅延させることなく、これらのシャープなディテールに早期に注意を払うようにするために、彼らはフーリエ変換($\mathcal{F}$)を使用した周波数領域変調を適用する。数学的には、空間的アテンションメカニズムを使用して高周波特徴を選択的に強調する。
$$Y = \sum_{b \in B} \sigma(f(X_b; W_b)) \odot X_b$$
ここで、周波数帯域は次のように分離される。
$$X_b = \mathcal{F}^{-1}(M_b \odot \mathcal{F}(X))$$
ここで、$M_b$は周波数をフィルタリングするバイナリマスクであり、$\odot$はアダマール(要素ごとの)積を表す。
特徴が変調されたら、それらは2つの異なる畳み込みブランチに送られる。
$$Y_L = f(X_L; W_L) + X_L$$
$$Y_H = f(X_H; W_H) + X_H$$
しかし、真の天才は、これらのブランチをどのように再び融合させるかにある。彼らは単に最後にそれらを混ぜ合わせるだけではない。非対称チャネルアテンションメカニズムを使用する。高周波データには、マックスプーリングがシャープで孤立したスパイク(骨小柱の端など)の検出に優れているため、グローバルマックスプーリング(GMP)を使用する。低周波データには、一般的な滑らかな解剖学的レイアウトを捉えるためにグローバルアベレージプーリング(GAP)を使用する。
彼らは、各特徴の重要性を決定するためにアテンションウェイト($A_H$および$A_L$)を計算する。
$$\widetilde{X} = upsample(X_L) + X_H$$
$$A_H = \sigma(MLP(GMP(\widetilde{X})))$$
$$A_L = \sigma(MLP(GAP(\widetilde{X})))$$
最後に、データを再分割し、これらの学習済みウェイトを適用して、ネットワークが巨視的な解剖学的構造と微視的なテクスチャの完璧なバランスを維持するようにする。
$$X = A_H \odot X_H + A_L \odot X_L$$
実験的アーキテクチャ:過酷な証明
著者らは、単にクリーンなデータセットにモデルを投入して、5%の精度向上を主張したわけではない。彼らは、臨床環境の混沌とした現実に数学的主張を過酷にテストするように設計された実験を構築した。
彼らは、完全に独立した2つの医療センターからデータを収集した。一方のセンターのデータは、モデルのトレーニングと内部テスト(1,614枚の画像)に使用され、もう一方のセンターのデータ(2,245枚の画像)は、「外部テストセット」として金庫に保管された。これにより、AIが単一の病院のCTスキャナーの特定の癖を記憶していないことが保証される。
犠牲者たち:
著者らは、彼らの創造物を3つのベースラインと比較した。
1. 従来のファントムレス(PL)線形回帰手法(マルチ電圧データを処理しようとする数学的変換式で適応)。
2. ResNet-10(標準的で非常に尊敬されている深層学習モデル)。
3. OctResNet-10(空間冗長性を処理するように特別に設計されたモデル)。
明白な証拠:
彼らのコアメカニズムが機能した決定的な証拠は、単に120 kVpおよび100 kVpデータセットで犠牲者を打ち負かしたこと(内部で5.990 $mg/cm^3$、外部で7.175 $mg/cm^3$という非常に優れた平均絶対誤差を達成)だけではなかった。本当の決定的な証拠は、アブレーションスタディであった。
彼らは体系的にモデルを「脳を切断」した。周波数バランスをオフにした。次にチャネルアテンションをオフにした。すべてのケースで、誤差率は急増した。高/低周波分離と非対称GMP/GAPアテンションメカニズムの両方が連携して機能した場合にのみ、モデルはピークパフォーマンスを達成した。これは、高周波テクスチャを分離して一意に重み付けすることが、管電圧変動を乗り切るために必要であるという仮説が、数学的および経験的に正しいことを証明した。
正直なところ、外部データセットの80 kVpレベルでの深刻な画像劣化を引き起こす正確な物理的物理学については完全には確信が持てない。著者らは、彼らのモデルが「センター間の大幅な画質の違い」のためにそこでベースラインを下回ったと述べており、これは極端に低い放射線量では、高周波の小柱データがAIがそれを見る前に、量子ノイズによって単純に破壊される可能性があることを示唆している。
将来の進化のための議論トピック
本論文の深遠な影響に基づき、将来の探求と批判的思考のためのいくつかの道筋を以下に示す。
-
情報破壊の閾値:
80 kVpでは、モデルは外部データで苦戦した。これは、物理学とAIが交差する興味深い疑問を提起する。高周波小柱構造が「隠されているが回復可能」から「光子飢餓と量子ノイズによって物理的に破壊される」へと移行する正確な放射線量はどの程度か?AI駆動の骨密度分析に必要な放射線の絶対下限を数学的に定義できるか? -
クロスモダリティ周波数分離:
高周波テクスチャを低周波グローバル照明から分離することがCT電圧問題を解決する場合、この正確な数学的フレームワークをMRIや超音波に移植できるか?例えば、このデュアルブランチアーキテクチャは、異なる磁場強度(1.5T vs 3T)によって引き起こされる低周波変動を無視して、MRI上の靭帯の高周波微細断裂を分離できるか? -
物理ファントムの終焉?
経済的影響は甚大である。ソフトウェアが内部組織参照と周波数変調を使用して任意のスキャナーの電圧に確実に動的に調整できる場合、物理的なCTファントムを製造、出荷、校正する必要は二度とないだろうか?生死に関わる診断シナリオにおいて、物理的なグラウンドトゥルースオブジェクトを確率的ニューラルネットワークで置き換えることの規制上および法的なハードルは何であるか?
他の体との同型
この論文を理解するためには、まず医師が骨粗鬆症をどのように診断するかを見る必要がある。医師はCTスキャンを用いて骨密度 (vBMD) を測定する。従来、これにはスキャン中に患者の下に置かれる物理的な校正オブジェクトである「ファントム」が必要であり、高価で煩雑であった。ファントムレス (PL) 手法は、患者自身の内部組織(脂肪や筋肉など)を参照点として使用する。
この動機は、現代の病院における重要な制約、すなわち様々な放射線線量に由来する。患者を過剰な放射線から救うため、クリニックでは標準的な120 kVpの代わりに、80 kVpや100 kVpのような低い管電圧の使用が増えている。問題は、電圧を下げることでCT画像の全体的なピクセル強度 (ハンスフィールドユニット、HU) が劇的に変化することである。既存の深層学習モデルは、これらの低周波の全体的な強度に大きく依存しているため、電圧が低下するとその精度は崩壊する。しかし、著者らは重要な生物学的な抜け穴に気づいた。全体の明るさは変化するものの、海綿骨のテクスチャの高周波成分は、異なる電圧間でも驚くほど安定しているのである。
これを解決するため、著者らは揮発性の巨視的データと安定した微視的データを数学的に分離する必要があった。標準的なニューラルネットワークに画像全体を入力する代わりに、周波数を分離するためのデュアルブランチアーキテクチャを構築した。
まず、冗長な計算オーバーヘッドを回避するために、フーリエ変換と空間的アテンションを組み合わせた周波数特徴の変調を行う。入力特徴マップ $X$ に対して、変調された出力 $Y$ は次のように定義される。
$$ Y = \sum_{b \in B} \sigma(f(X_b; W_b)) \odot X_b $$
ここで、周波数帯域は $X_b = \mathcal{F}^{-1}(M_b \odot \mathcal{F}(X))$ を介して抽出され、$\mathcal{F}$ はフーリエ変換を表し、$M_b$ は二値周波数マスクとして機能する。
信号が低周波 ($X_L$) と高周波 ($X_H$) の成分に分割されたら、それらは並列ブランチで処理される。この論文の真の独創性は、これらのブランチがどのように再び融合されるかにある。著者らは、高周波データ(シャープな骨のエッジ)と低周波データ(一般的な骨の形状)には、異なる数学的レンズが必要であることを認識した。彼らは非対称チャネルアテンションメカニズムを設計した。高周波特徴のシャープなピークを捉えるためにGlobal Max Pooling (GMP) を、低周波特徴を平滑化して捉えるためにGlobal Average Pooling (GAP) を適用する。
$$ A_H = \sigma(MLP(GMP(\tilde{X}))) $$
$$ A_L = \sigma(MLP(GAP(\tilde{X}))) $$
これらのアテンション重みは、分離された信号を動的に再結合するために使用される。
$$ \tilde{X} = A_H \odot X_H + A_L \odot X_L $$
この方程式により、低周波の全体的な強度が電圧変化によって信頼できなくなった場合に、ネットワークは安定した高周波テクスチャを適応的に信頼することができる。
その核心において、この研究の構造的骨格は、複雑な信号を揮発性の巨視的ベースラインと安定した微視的変動に分離し、それらを並列処理し、非対称重み付け関数を用いて動的に再結合することで、様々な環境条件下での不変な指標を抽出するメカニズムである。
この骨格に基づいて、科学工学の全く異なる分野でこの正確な論理の「鏡像」を見つけることができる。
1) 定量的金融: アルゴリズム取引において、資産価格はマクロ経済トレンド(低周波、金利引き上げのような外部「電圧」に非常に敏感)と、マイクロ構造のオーダーブックダイナミクス(高周波、安定した本質的な取引行動を表す)で構成される。市場全体のノイズと本質的なマイクロボラティリティを分離することで、資産の真のファンダメンタルバリューを抽出することは、CTの全体的な強度と海綿骨のテクスチャを分離することと直接的に鏡像関係にある。
2) 地震学: 地震の規模を検出する際、地震計は低周波の表面波(局所的な土壌タイプによって大きく歪み、CT管電圧の変化のように作用する)と、高周波の体波(断層線の破壊の真の、安定したシグネチャを伝える)を記録する。地震学者は、地震の不変の真実を見つけるために、これらの周波数のバランスを取ることに常に苦労している。
定量的金融の研究者が明日、この論文の正確な非対称アテンション方程式を「盗んだ」らどうなるだろうか?もし彼らが $$ \tilde{X} = A_H \odot X_H + A_L \odot X_L $$ を高頻度取引アルゴリズムに適用した場合、Global Max Pooling を使用してオーダーブック異常の絶対的なピーク(「海綿骨」取引)を積極的に捉え、Global Average Pooling を使用して揮発性のマクロ経済センチメントを平滑化することができるだろう。ブレークスルーは、市場全体が突然高ボラティリティまたは低ボラティリティのレジームに移行したかどうかにかかわらず、予測精度と収益性を維持する、根本的に堅牢な取引ボットとなるだろう。これは、アルゴリズムを市場の「管電圧」変動に対して実質的に免疫にする。
最終的に、このアーキテクチャは、衰退する骨の密度を測定する場合でも、変動する金融資産の隠された価値を測定する場合でも、不変の真実の数学的追求は、分離された周波数と適応的アテンションの全く同じシンフォニーに依存することを示しており、普遍的な構造ライブラリに素晴らしい新しい設計図を追加する。
