다중 튜브 전압 vBMD 측정을 위한 이중 분기 주파수 균형 및 비대칭 채널 어텐션
Phantom-less volumetric bone mineral density (vBMD) measurement using computed tomography (CT) presents a cost-effective alternative to conventional phantom-based approaches, yet faces accuracy challenges across...
배경 및 학문적 계보
이 논문에서 다루는 문제의 정확한 기원을 이해하기 위해서는 의사들이 골다공증을 진단하는 방식을 살펴볼 필요가 있다. 골밀도(vBMD) 측정은 뼈의 강도를 평가하는 Gold Standard이다. 과거에는 정량적 컴퓨터 단층 촬영(QCT)을 사용하여 이를 수행했으며, CT 스캔 중에 환자 아래에 "팬텀(phantom)"이라 불리는 물리적 보정 객체를 배치해야 했다. 논문에서는 이러한 물리적 팬텀이 고가라고 언급하지만, 정확한 임상 가격은 텍스트만으로는 확실하지 않다. 그러나 의료 영상 분야에서 특수 보정 하드웨어는 세션당 150달러 이상, 혹은 그 이상을 쉽게 초과할 수 있으며, 빈번한 재보정의 번거로움은 말할 것도 없다.
이를 우회하기 위해 의료계에서는 "팬텀-리스(phantom-less, PL)" 방법을 개발했다. 이러한 방법은 외부 객체 대신 환자 자신의 내부 조직(지방 및 근육 등)을 참조점으로 사용하여 골밀도를 계산한다. 최근에는 심층 신경망(DNN)이 이 과정을 자동화하는 데 활용되고 있다.
그러나 현대 임상 실습의 변화로 인해 심각한 "문제점(pain point)"이 발생했다. 환자를 과도한 방사선으로부터 보호하기 위해 병원에서는 표준 120 kVp에서 80 또는 100 kVp로 CT 스캐너의 튜브 전압을 점차 낮추고 있다. 기존 DNN 모델의 근본적인 한계는 120 kVp 스캔에 대해 엄격하게 최적화되었다는 점이다. 저전압 이미지를 입력받으면 전체적인 밝기와 대비(CT 감쇠)가 급격하게 변한다. 이러한 전역적인 강도 변화(저주파 정보)에 크게 의존하는 기존 모델은 심각한 성능 저하를 겪으며, 최대 $20 \text{ mg/cm}^3$의 추정 오류를 발생시킨다. 이들은 방사선량과 무관하게 안정적으로 유지되는 뼈의 미세하고 스펀지 같은 질감(고주파 정보)을 완전히 놓친다. 더욱이, 이러한 주파수를 분리하는 전통적인 방법은 3D 의료 영상에 적용하기에는 계산량이 너무 많다.
과학적 원리를 직관적으로 이해할 수 있도록, 몇 가지 고도로 전문화된 분야 용어를 일상적인 개념으로 번역하면 다음과 같다.
- 팬텀-리스(PL) vBMD 측정: 사진 속 사과의 무게를 추측하는 것을 상상해보자. "팬텀" 방식은 비교를 위해 사과 옆에 표준 1파운드 무게추를 놓는 것을 요구한다. "팬텀-리스" 방식은 외부 도구를 가져오는 대신, 사진에 이미 있는 것(사과가 놓인 접시의 크기 등)을 비교하여 사과의 무게를 추측하는 것과 같다.
- 튜브 전압(kVp): 사진을 찍는 데 사용되는 손전등의 밝기라고 생각하면 된다. 높은 전압(120 kVp)은 모든 것을 명확하게 보여주지만 많은 에너지(방사선)를 사용하는 눈부시게 밝은 빛이다. 낮은 전압(80 kVp)은 피사체에 더 안전한 어두운 빛이지만 결과 이미지가 다르게 보이며, 오래된 컴퓨터 프로그램을 혼란스럽게 만든다.
- 골내 구조(Trabecular architecture): 뼈의 내부 구조는 단단한 암석이 아니라, 단단한 스펀지나 벌집과 더 유사하게 보인다. 이 용어는 뼈 내부의 복잡하고 다공성인 네트워크를 지칭한다.
- 주파수 분해(Frequency decomposition): 교향곡을 듣는 것을 상상해보자. 이 과정은 오디오 이퀄라이저를 사용하여 깊고 웅장한 베이스(저주파: 뼈의 전체적인 모양과 위치)와 바이올린의 날카롭고 선명한 소리(고주파: 뼈 내부의 미세하고 스펀지 같은 질감)를 분리하는 것과 같다.
이를 해결하기 위해 저자들은 이러한 주파수를 분리하고 균형을 맞추는 경량의 듀얼 브랜치 신경망을 설계했다. 수학적으로, 이들은 무거운 계산 없이 고주파 디테일을 추출하고 비대칭 채널 어텐션 메커니즘을 사용하여 각 주파수 대역의 중요도를 가중한다.
주파수 변조 및 특징 융합을 수학적으로 해석하고 해결하는 방법은 다음과 같다.
먼저, 푸리에 변환과 공간 어텐션 메커니즘을 사용하여 주파수 특징을 변조한다.
$$ Y = \sum_{b \in B} \sigma(f(X_b; W_b)) \odot X_b $$
$$ X_b = \mathcal{F}^{-1}(M_b \odot \mathcal{F}(X)) $$
이후, 저주파 및 고주파 특징을 융합하여 어텐션 가중치를 생성함으로써 네트워크가 가장 중요한 정보에 집중하도록 한다.
$$ \widetilde{X} = upsample(X_L) + X_H $$
$$ A_H = \sigma(MLP(GMP(\widetilde{X}))) $$
$$ A_L = \sigma(MLP(GAP(\widetilde{X}))) $$
마지막으로, 이러한 어텐션 가중치를 적용하여 특징을 해당 도메인으로 다시 분리한다.
$$ X = A_H \odot X_H + A_L \odot X_L $$
아키텍처를 이해하는 데 필요한 주요 수학적 표기법을 정리한 표는 다음과 같다.
| 표기법 | 설명 |
|---|---|
| $X$ | 입력 특징 맵, 3D 공간에서 $X \in \mathbb{R}^{C,D,H,W}$로 정의됨 |
| $Y$ | 주파수 변조 후의 출력 특징 맵 |
| $\mathcal{F}, \mathcal{F}^{-1}$ | 푸리에 변환 및 그 역변환 |
| $M_b$ | 특정 주파수 대역을 분리하는 데 사용되는 이진 주파수 마스크 |
| $W$ | 컨볼루션 파라미터 (가중치) |
| $X_L, X_H$ | 분리된 저주파 및 고주파 특징 구성 요소 |
| $Y_L, Y_H$ | 처리된 저주파 및 고주파 특징 |
| $A_L, A_H$ | 저주파 및 고주파에 대한 채널 어텐션 맵 |
| $\widetilde{X}$ | 재분할 전 융합된 특징 맵 |
| $AP(x)$ | $2 \times 2 \times 2$ 커널을 사용한 평균 풀링 연산 |
| $upsample(x)$ | 최근접 이웃 업샘플링 연산 |
| $\sigma$ | 시그모이드 활성화 함수 |
| $\odot$ | Hadamard 곱 (요소별 곱셈) |
문제 정의 및 제약 조건
스펀지의 무게를 재려고 하는데, 저울에 올리는 대신 사진만 보고 무게를 추측해야 한다고 상상해 보세요. 게다가 방의 조명이 계속 변합니다. 때로는 밝고, 때로는 어둡습니다. 이것이 바로 의사들이 물리적인 보정 도구("팬텀")를 사용하지 않고 CT 스캔에서 골밀도를 측정하려고 할 때 직면하는 문제입니다.
시작점과 목표점
입력 (현재 상태): 환자의 척추체 3D 컴퓨터 단층 촬영(CT) 이미지로 시작합니다. 이 스캔은 튜브 전압(일반적으로 80, 100 또는 120 kVp)으로 알려진 다양한 방사선 수준에서 촬영됩니다.
출력 (목표 상태): 목표는 $mg/cm^3$으로 표현되는 매우 정확한 체적 골밀도(vBMD) 측정을 출력하는 것입니다.
수학적 간극:
전통적으로 의사들은 조직이 X선을 얼마나 차단하는지를 나타내는 수학적 표현인 Hounsfield Unit(HU)을 보고 골밀도를 측정합니다. 여기서 누락된 연결 고리는 HU 값이 X선 튜브 전압에 엄격하게 의존한다는 것입니다. 병원에서 환자의 과도한 방사선 노출을 줄이기 위해 전압을 낮추면 동일한 뼈의 HU 값이 크게 떨어집니다. 저자들은 매우 가변적이고 전압에 의존적인 3D 공간 강도 행렬 $X \in \mathbb{R}^{C,D,H,W}$을 스캐너 설정과 완전히 독립적인 안정적인 절대 밀도 값으로 매핑하는 수학적 다리를 구축해야 했습니다.
고통스러운 딜레마
컴퓨터 비전 분야에서는 한 가지 측면을 개선하면 거의 항상 다른 측면이 깨집니다. 이 특정 문제에 대해 이전 연구자들은 주파수 추출과 계산 비용 사이의 잔인한 절충안에 갇혀 있었습니다.
이를 이해하기 위해 이미지를 두 가지 "주파수"로 분할해야 합니다.
1. 저주파 특징: 척추의 전체 윤곽과 같은 광범위하고 거시적인 모양입니다. 이는 표준 신경망이 학습하기 쉽고 모델이 뼈를 빠르게 찾는 데 도움이 됩니다. 그러나 튜브 전압 변화에 매우 민감합니다.
2. 고주파 특징: 뼈의 작고 미세하며 스펀지 같은 미세 구조(골소주 구조)입니다. 이러한 특징은 다양한 전압에서 매우 안정적이며 골다공증의 진정한 지표입니다.
딜레마는 다음과 같습니다. 표준 심층 신경망(DNN)은 자연스럽게 저주파 정보를 우선시합니다. 네트워크가 고주파 3D 질감에 주의를 기울이도록 강제하려면 전통적으로 깊고 복잡한 네트워크 또는 3D 웨이블릿 변환과 같은 무거운 수학적 연산을 사용해야 합니다. 그러나 3D 공간에서 이렇게 하면 메모리와 처리 요구 사항이 기하급수적으로 폭발합니다. 병원에서 CT 전압을 변경해도 실패하는 경량 모델을 얻거나 표준 임상 하드웨어에서 실행하기에는 너무 크고 느린 강력한 모델을 얻게 됩니다.
가혹한 벽과 제약
저자들은 이 문제를 해결하기 매우 어렵게 만드는 몇 가지 가혹하고 현실적인 벽에 부딪혔습니다.
- 임상 방사선 벽: 환자의 방사선 노출을 줄이기 위한 전 세계적인 대규모 추진으로 인해 스캔이 120 kVp에서 80 kVp로 낮아지고 있습니다. 이러한 낮은 전압에서는 전역 강도 측정값이 근본적으로 신뢰할 수 없게 됩니다. 모델은 정확도를 잃지 않고 이러한 더 어둡고 낮은 에너지 스캔에 적응해야 합니다.
- 질병의 물리적 희소성: 골다공증은 말 그대로 뼈의 소실입니다. 질병이 진행됨에 따라 골소주 뼈는 극도로 희소해집니다. 네트워크는 적극적으로 사라지고 있는 미세한 질감 특징을 찾도록 강요받습니다.
- 3D 계산 병목 현상: 의료 영상은 평평한 2D 사진이 아니라 거대한 3D 볼륨입니다. 깊이, 높이 및 너비에 걸쳐 전통적인 주파수 분해(반복적인 푸리에 변환과 같은)를 적용하려면 막대한 메모리가 필요합니다. 저자들은 무거운 수학 없이 주파수를 분리하는 방법을 찾아야 했으며, 대신 평균 풀링을 사용하여 저주파를 추출하고 이를 원본 이미지에서 빼서 고주파를 찾는 영리한 트릭을 사용했습니다.
- 특징 혼합 함정: 저주파와 고주파를 병렬로 처리하려고 하면(이중 분기 네트워크), 표준 컨볼루션 레이어는 실수로 정보를 다시 혼합하는 경향이 있습니다. 저자들은 고주파 분기가 미세한 세부 사항만 보고 저주파 분기가 넓은 모양만 보도록 보장하기 위해 엄격한 수학적 게이트키퍼, 즉 비대칭 채널 주의 메커니즘을 설계해야 했습니다. 이는 특징 맵 $X$를 저주파($X_L$) 및 고주파($X_H$) 구성 요소로 분리하여 수학적으로 정의됩니다.
$$X = upsample(X_L) + X_H$$
요약하자면, 저자들은 3D에서 뼈의 미세하고 사라져가는 구조를 보고, X선 기계의 변화하는 "조명"을 무시하며, 이 모든 것을 엄격한 계산 예산으로 수행할 수 있는 시스템을 구축해야 했습니다.
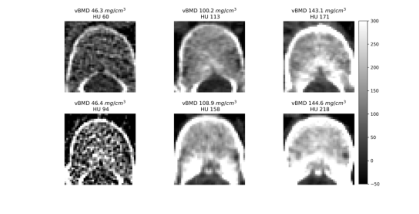 Figure 1. Intuitive comparison of features in vBMD measurement. The first row shows vertebral bodies with varying bone densities at 120 kVp. The second row shows corresponding vertebral bodies at non-120 kVp, where vBMD texture remains similar, but HU values within the VOI differ significantly. Low vBMD vertebral bodies exhibit both reduced HU values and a sparser trabecular structure in the measurement area
Figure 1. Intuitive comparison of features in vBMD measurement. The first row shows vertebral bodies with varying bone densities at 120 kVp. The second row shows corresponding vertebral bodies at non-120 kVp, where vBMD texture remains similar, but HU values within the VOI differ significantly. Low vBMD vertebral bodies exhibit both reduced HU values and a sparser trabecular structure in the measurement area
이 접근 방식은 왜
저자들이 전통적인 최첨단(SOTA) 방법론, 예를 들어 표준 3D Convolutional Neural Networks (CNNs), Vision Transformers, 또는 Diffusion 모델이 본 문제에 근본적으로 불충분하다는 것을 깨달은 결정적인 순간은 CT 스캔의 물리적 거동을 다양한 튜브 전압 하에서 분석했을 때였다. 방사선 노출을 줄이기 위해 현대의 병원들은 종종 표준 $120$ kVp에서 $100$ kVp 또는 $80$ kVp로 CT 튜브 전압을 낮춘다. 그러나 이러한 전압 강하는 전역 Hounsfield Unit (HU) 값(방사선 밀도의 표준 측정값)을 극적으로 변화시킨다. 표준 CNN은 이미지의 전체적인 형태와 전역 강도에 해당하는 저주파 정보에 자연스럽게 우선순위를 둔다. 이러한 저주파 전역 강도는 전압 변화에 매우 민감하기 때문에, $120$ kVp 데이터로 학습된 표준 모델은 $80$ kVp 데이터로 테스트될 때 성능이 대폭 저하되어 $20$ $mg/cm^3$까지의 오차를 발생시킨다.
저자들은 중요한 통찰을 얻었다: 전역 강도는 전압에 따라 변하지만, 고주파 특징, 특히 뼈의 미세하고 스펀지 같은 골소주 미세 구조는 구조적으로 안정적으로 유지된다는 것이다. 따라서 거시적인 형태를 선호하여 고주파 텍스처 디테일을 흐리게 하는 모든 표준 네트워크는 실패할 운명이었다. 그들은 반드시 이러한 주파수 영역을 별도로 처리해야만 했다.
단순한 성능 지표를 넘어, 이 방법론은 3D 의료 영상의 막대한 계산 부담을 처리하는 방식 때문에 질적으로도 우수하다. 전통적인 주파수 영역 방법론은 일반적으로 웨이블릿 변환이나 다중 스케일 컨볼루션 커널과 같은 계산 집약적인 기법에 의존하여 주파수를 분리한다. 이를 대규모 3D 볼륨 CT 데이터에 적용하면 메모리 복잡성이 폭발적으로 증가하여 임상 환경에서 모델을 실질적으로 사용할 수 없게 된다. 저자들은 모든 계층에서 무거운 수학적 변환을 포기함으로써 막대한 구조적 이점을 달성했다. 대신, 그들은 매우 간단한 분리 방법을 도입했다: 평균 풀링을 사용하여 특징 맵을 다운스케일링하여 저주파 성분($X_L$)을 추출하고, 원본 특징 맵과 업샘플링된 저주파 맵 간의 잔차를 계산하여 고주파 성분($X_H$)을 도출한다. 수학적으로 이는 다음과 같이 표현된다:
$$X_H = X - \text{upsample}(X_L)$$
이는 무거운 신호 처리의 필요성을 우아하게 우회한다. 또한, 네트워크 전체에 푸리에 변환을 반복적으로 적용하여 막대한 오버헤드를 생성하는 대신, 국소 특징 추출이 가장 중요한 얕은 계층으로 주파수 변조를 제한한다.
이러한 선택된 아키텍처는 문제의 엄격한 제약 조건과 해결책의 고유한 특성 간의 완벽한 "결합"을 나타낸다. 제약 조건은 모델이 외부 보정 팬텀에 의존하지 않고 다양한 CT 튜브 전압에 걸쳐 일반화되어야 하며, 동시에 무거운 3D 데이터를 효율적으로 처리해야 한다는 것을 요구한다. 이중 분기 아키텍처는 이러한 요구 사항에 완벽하게 부합한다. 네트워크를 분할함으로써, 모델은 거시적인 척추 해부학(저주파)을 이해하기 위한 더 깊은 경로와 섬세한 골소주 구조(고주파)를 포착하기 위한 더 얕은 경로를 사용한다. 이를 융합하기 위해 비대칭 채널 주의 메커니즘을 활용한다. 날카롭고 안정적인 고주파 디테일을 강조하기 위해 Global Max Pooling (GMP)을 적용하고, 부드러운 저주파 데이터를 위해 Global Average Pooling (GAP)을 적용한다:
$$A_H = \sigma(MLP(GMP(\tilde{X})))$$
$$A_L = \sigma(MLP(GAP(\tilde{X})))$$
이는 안정적인 골소주 특징이 최종 골밀도(vBMD) 측정치를 적극적으로 안내하도록 보장하여, 모델이 전압 유발 강도 변화에 대해 매우 강력하도록 만든다.
마지막으로, 이는 Generative Adversarial Networks (GANs) 또는 Diffusion 모델과 같은 다른 인기 있는 접근 방식이 왜 여기서 치명적으로 실패했을지를 설명한다. 생성 모델은 누락된 데이터 분포를 합성하거나 환각하는 데 설계되었다. 골다공증을 진단하기 위해 정확한 물리적 측정이 필요한 정량적 의료 영상에서 구조적 데이터를 환각하는 것은 임상적으로 위험하다. 더욱이, 이러한 모델들은 악명 높게 무겁다. 저자들은 표준 2D DNN을 3D로 확장하는 것조차 "과도한 계산 자원"을 요구한다고 명시적으로 언급한다. 3D 볼륨 CT 스캔에 대해 거대한 Transformer 또는 다단계 Diffusion 프로세스를 배포하는 것은 계산적으로 마비될 것이며, 안정적인 구조적 텍스처 추출을 목표로 하는 회귀 작업에는 전혀 불필요하다. 경량의 주파수 균형 이중 분기 네트워크는 절대적인 정밀도에 대한 임상적 요구와 효율성에 대한 엔지니어링 요구를 모두 충족하는 유일한 실행 가능한 경로였다.
수학 및 논리 메커니즘
이 논문의 핵심을 이해하기 위해서는 먼저 이 논문이 해결하는 물리적 문제를 이해해야 한다. 의사들은 CT 스캔을 사용하여 골밀도(vBMD)를 측정할 때, 일반적으로 120 kVp와 같은 특정 방사선관 전압에 의존한다. 그러나 현대의 병원들은 환자의 방사선 노출을 줄이기 위해 더 낮은 전압(80 또는 100 kVp 등)으로 전환하고 있다. 문제는 무엇인가? 전압을 낮추면 CT 이미지의 전반적인 밝기와 대비(Hounsfield Units)가 크게 변한다는 것이다.
만약 딥러닝 모델이 120 kVp에서의 전반적인 밝기(저주파 데이터)를 기억한다면, 80 kVp에서는 심각하게 실패할 것이다. 그러나 뼈의 미세하고 스펀지 같은 골소주 구조(고주파 데이터)는 전압에 관계없이 물리적으로 안정적으로 유지된다. 저자들은 이미지를 저주파와 고주파로 분리하고, 동적으로 중요도를 가중하며, 다시 융합하는 독창적인 이중 분기 신경망을 설계했다.
이러한 전압 간 일반화를 가능하게 하는 절대적인 핵심 수학 엔진은 다음과 같다.
$$ \widetilde{X}_{base} = upsample(X_L) + X_H $$
$$ A_H = \sigma(MLP(GMP(\widetilde{X}_{base}))) $$
$$ A_L = \sigma(MLP(GAP(\widetilde{X}_{base}))) $$
$$ \widetilde{X}_{coupled} = A_H \odot X_H + A_L \odot X_L $$
$$ Y_L = AP(\widetilde{X}_{coupled}) $$
$$ Y_H = \widetilde{X}_{coupled} - upsample(Y_L) $$
(참고: 저자들은 초기 융합 상태와 어텐션 결합 상태 모두에 $\widetilde{X}$를 사용했다. 시간적 변환을 더 명확하게 하기 위해 'base'와 'coupled'라는 접미사를 추가했다.)
이 엔진이 어떻게 작동하는지 알아보기 위해 조각별로 분해해 보자.
- $X_L$ 및 $X_H$: 저주파 및 고주파 분기의 입력 특징 맵이다. $X_L$은 뼈의 거시적이고 흐릿한 형태(전압 변화에 매우 민감함)를 나타낸다. $X_H$는 날카롭고 미세한 골소주 격자(전압에 걸쳐 안정적임)를 나타낸다.
- $upsample()$: 최근접 이웃 업샘플링 함수이다. 저주파 특징은 메모리를 절약하기 위해 종종 풀링되고 다운샘플링되기 때문에, 고주파 특징과 상호 작용하기 전에 동일한 공간 차원으로 다시 확장되어야 한다.
- $+$ (덧셈): 왜 연결(concatenate) 대신 덧셈을 사용하는가? 연결은 메모리 사용량을 두 배로 늘린다. 덧셈은 물리적 중첩으로 작용한다. 마치 동일한 수학적 공간에서 흐릿한 색상 지도 위에 날카로운 질감 지도를 직접 추가하는 것과 같다.
- $GMP()$ 및 $GAP()$: Global Max Pooling 및 Global Average Pooling이다. 여기서 뼈의 물리적 특성이 작용한다. $GMP$는 절대적으로 가장 날카롭고 가장 높은 강도의 스파이크를 위한 레이더 역할을 한다(단단한 골소주 뼈 구조를 분리하는 데 완벽함). $GAP$는 영역의 전반적인 주변 에너지 또는 평균 밀도를 계산한다.
- $MLP()$: 다층 퍼셉트론(작은 신경망)이다. 이는 풀링된 통계를 살펴보고 골밀도 예측에 실제로 유용한 특정 특징 채널이 무엇인지 결정하는 "두뇌" 역할을 한다.
- $\sigma$ (시그모이드 함수): MLP의 출력을 0과 1 사이의 범위로 압축한다. 이는 조광기 스위치 세트 역할을 한다.
- $A_H$ 및 $A_L$: 고주파 및 저주파에 대한 결과 어텐션 가중치이다.
- $\odot$ (Hadamard Product): 요소별 곱셈이다. 왜 덧셈 대신 곱셈을 사용하는가? 이는 게이팅 메커니즘이기 때문이다. 특정 저주파 채널이 전압 변화로 인해 너무 손상되었다고 판단되면, 해당 $A_L$ 값은 0.1이 되어 해당 채널을 효과적으로 음소거할 수 있다. 고주파 채널이 중요한 구조 데이터를 포함하고 있다면, 해당 $A_H$ 값은 0.9가 되어 증폭될 수 있다.
- $AP()$: $2 \times 2 \times 2$ 커널을 사용한 평균 풀링이다. 이는 저주파 통과 필터 역할을 하여, 새로 결합된 마스터 특징 맵을 평활화하여 정제된 저주파 출력 $Y_L$을 추출한다.
- $-$ (뺄셈): $Y_H$를 얻기 위해 왜 뺄셈을 사용하는가? 이는 잔차 논리의 아름다운 활용이다. 고주파는 수학적으로 "저주파가 아닌 모든 것"으로 정의된다. 평활화된 기본값($upsample(Y_L)$)을 마스터 결합 맵($\widetilde{X}_{coupled}$)에서 빼면, 네트워크는 이 단계에서 복잡하고 계산량이 많은 푸리에 변환 없이도 선명한 고주파 세부 정보를 완벽하게 분리한다.
단계별 흐름
3D 원시 CT 데이터 블록이 기계 조립 라인에 들어가는 것을 상상해 보자.
먼저, 데이터는 두 개의 별도 컨베이어 벨트로 분리된다. 하나는 흐릿하고 전반적인 뼈 모양($X_L$)을 운반하고, 다른 하나는 날카롭고 스펀지 같은 뼈 질감($X_H$)을 운반한다. 흐릿한 모양은 날카로운 질감과 정확히 같은 크기가 되도록 물리적으로 확장($upsample$)되고, 두 개는 복합 블록($\widetilde{X}_{base}$)을 만들기 위해 쌓인다.
다음으로, 이 복합 블록은 두 개의 특수 센서 아래를 통과한다. 첫 번째 센서($GMP$)는 가장 날카롭고 가장 극단적인 구조 스파이크를 스캔한다. 두 번째 센서($GAP$)는 전반적인 주변 밀도를 측정한다. 이 측정값은 중앙 컴퓨터($MLP$)로 공급되어 각 특징 채널의 신뢰도를 정확하게 계산한다.
컴퓨터는 두 세트의 다이얼($A_H$ 및 $A_L$)을 출력한다. 이 다이얼은 원래 컨베이어 벨트에 다시 적용되어, 관련성이 없거나 노이즈가 많은 채널은 어둡게 하고 매우 관련성이 높은 채널은 증폭시킨다. 최적화된 벨트는 마스터 결합 블록($\widetilde{X}_{coupled}$)으로 병합된다.
마지막으로, 이 마스터 블록은 평활화 기계($AP$)를 통해 압착되어 새로 정제되고 안정적인 흐릿한 모양($Y_L$)을 만든다. 정제된 날카로운 질감($Y_H$)을 얻기 위해, 기계는 단순히 마스터 블록을 가져와 흐릿한 모양을 잘라낸다($-$). 그러면 완벽하게 균형 잡힌 업데이트된 두 구성 요소가 아키텍처의 다음 단계로 진행된다.
최적화 역학
이 메커니즘은 실제로 어떻게 학습하고 수렴하는가? 네트워크는 120 kVp에서 촬영된 금 표준 팬텀 기반 측정값에 대해 회귀 손실(예: 평균 절대 오차)을 사용하여 종단 간(end-to-end)으로 훈련된다.
이 아키텍처는 덧셈과 뺄셈에 크게 의존하기 때문에 손실 지형이 놀랍도록 부드럽다. 미적분학에서 덧셈 또는 뺄셈 연산의 국소 미분은 정확히 1(또는 -1)이다. 이는 네트워크가 오류를 범했을 때, $Y_H$ 및 $Y_L$ 방정식을 통해 기울기 신호가 저하되거나 소실되지 않고 역방향으로 흐른다는 것을 의미한다.
훈련이 진행됨에 따라 $MLP$는 지속적인 피드백을 받는다. 만약 모델이 80 kVp 스캔에 의해 인위적으로 어두워진 저주파 채널에 너무 많이 의존하여 골밀도를 과대평가한다면, 기울기는 $MLP$에게 다음과 같이 알려준다: "다음에 이 특정 분산을 보면, $A_L$ 조광기를 낮춰라." 시간이 지남에 따라 네트워크는 동적으로 주의를 전환하는 방법을 학습한다. 저전압 스캔의 혼란스러운 전역 강도 변화를 감지하면, 안정적인 고주파 골소주 특징에 자동으로 더 많이 의존하게 된다.
솔직히 말해서, 저자들이 정확히 어떤 특정 최적화기(예: Adam, SGD)나 학습률 스케줄을 사용했는지는 제공된 텍스트에 해당 하이퍼파라미터 세부 정보가 명시적으로 나열되어 있지 않기 때문에 완전히 확신할 수 없다. 그러나 잔차 분리 및 비대칭 어텐션과 같은 구조 설계 자체는 자연스러운 정규화기 역할을 한다. 이는 모델이 단일 튜브 전압의 절대적인 Hounsfield Units에 과적합되는 것을 방지하고, 대신 뼈의 근본적인 물리적 현실을 학습하도록 강제한다.
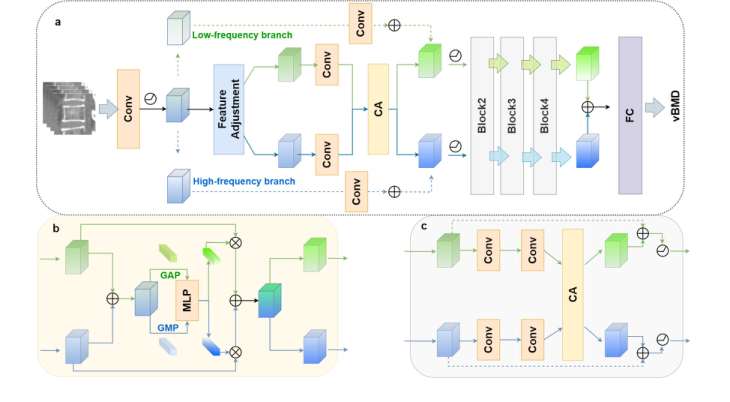 Figure 2. The proposed network. The proposed network adopts a dual-branch ar- chitecture consisting of four distinct modules (a). The first module is responsible for spatial reallocation of feature maps in the frequency domain. The following modules incorporate convolutional layers designed to perform coupling and re-decoupling oper- ations, guided by a channel attention mechanism (b and c). This design facilitates the effective fusion of frequency features, thereby enhancing the model’s ability to dynam- ically process both low- and high-frequency information.CA, channel attention; FC, fully connected
Figure 2. The proposed network. The proposed network adopts a dual-branch ar- chitecture consisting of four distinct modules (a). The first module is responsible for spatial reallocation of feature maps in the frequency domain. The following modules incorporate convolutional layers designed to perform coupling and re-decoupling oper- ations, guided by a channel attention mechanism (b and c). This design facilitates the effective fusion of frequency features, thereby enhancing the model’s ability to dynam- ically process both low- and high-frequency information.CA, channel attention; FC, fully connected
결과, 한계점 및 결론
건물의 구조적 무결성을 판단하려 하는데, 오직 사진만 볼 수 있다고 가정해 보자. 상황을 더 어렵게 만들기 위해, 어떤 사진은 밝은 대낮에 찍혔고, 다른 사진은 저렴한 카메라로 황혼에 찍혔다고 하자. 조명에 따라 건물의 전반적인 색상과 밝기는 극적으로 변하지만, 콘크리트의 미세한 균열, 즉 고주파 디테일은 일관되게 유지된다.
이것이 바로 전산화 단층 촬영(CT) 스캔을 사용하여 골다공증을 진단하기 위해 골밀도(vBMD)를 측정할 때 의사들이 직면하는 문제와 정확히 같다.
역사적으로 병원에서는 스캔 중 환자 아래에 "팬텀(phantom)"이라고 불리는 물리적 보정 물체를 배치하여 기준 밀도 참조를 제공했다. (이는 상당히 비싸며, 때로는 시술 비용에 미화 150달러 이상을 추가하기도 한다.) 비용 절감을 위해, 환자 자신의 지방과 근육을 참조점으로 사용하는 "팬텀 없는(phantom-less, PL)" 방법이 개발되었다. 그러나 중대한 제약이 발생했다. 현대 병원들은 환자를 보호하기 위해 CT 스캔의 방사선량을 낮추고 있다(관 전압을 120 kVp에서 80 또는 100 kVp로 낮추고 있다). 이러한 근본적인 변화는 Hounsfield Units(CT 스캔의 픽셀 강도 값)를 변화시킨다. 전체적인 밝기("큰 그림", 저주파 데이터)에 크게 의존하는 기존 AI 모델은 이러한 전압 강하로 인해 완전히 혼란스러워져 측정 오류가 발생한다.
이 논문의 저자들은 다음과 같은 훌륭한 점을 깨달았다. 낮은 방사선량으로 인해 뼈의 전반적인 밝기는 변하지만, 뼈의 미세한 스펀지 같은 질감(골소주 구조)은 변하지 않는다는 것이다. 그들은 변화하는 조명을 무시하고 콘크리트의 균열에 집중할 수 있는 AI가 필요했다.
수학적 핵심: 현실의 분리 및 조절
이를 해결하기 위해 저자들은 심각한 계산 제약을 극복해야 했다. 고주파 3D 질감을 추출하는 것은 일반적으로 다중 스케일 웨이블릿 변환과 같이 엄청나게 무거운 수학을 요구하며, 이는 표준 병원 컴퓨터를 충돌시킬 수 있다.
대신, 그들은 이미지를 별도의 경로로 분할하는 경량의 이중 분기 네트워크를 설계했다. 먼저, 간단한 평균 풀링 연산을 사용하여 저주파 "흐릿한" 데이터($X_L$)를 추출한다. 그런 다음, 이 흐릿한 이미지를 원본에서 빼서 고주파 "선명한" 디테일($X_H$)을 분리한다.
네트워크가 시스템을 느리게 하지 않고 이러한 선명한 디테일에 조기에 주의를 기울이도록 하기 위해, 푸리에 변환($\mathcal{F}$)을 사용한 주파수 영역 조절을 적용한다. 수학적으로, 공간 주의 메커니즘을 사용하여 고주파 특징을 선택적으로 강화한다.
$$Y = \sum_{b \in B} \sigma(f(X_b; W_b)) \odot X_b$$
여기서 주파수 대역은 다음과 같이 분리된다.
$$X_b = \mathcal{F}^{-1}(M_b \odot \mathcal{F}(X))$$
여기서 $M_b$는 주파수를 필터링하는 이진 마스크이고, $\odot$는 Hadamard(요소별) 곱을 나타낸다.
특징이 조절되면, 두 개의 별도 컨볼루션 분기로 전달된다.
$$Y_L = f(X_L; W_L) + X_L$$
$$Y_H = f(X_H; W_H) + X_H$$
하지만 진정한 천재성은 이 분기들을 다시 융합하는 방식에 있다. 단순히 마지막에 섞는 것이 아니다. 비대칭 채널 주의 메커니즘을 사용한다. 고주파 데이터의 경우, 맥스 풀링은 날카롭고 고립된 스파이크(골소주의 가장자리와 같은)를 감지하는 데 뛰어나므로 Global Max Pooling(GMP)을 사용한다. 저주파 데이터의 경우, 일반적이고 부드러운 해부학적 레이아웃을 포착하기 위해 Global Average Pooling(GAP)을 사용한다.
주의 가중치($A_H$ 및 $A_L$)를 계산하여 각 특징의 중요도를 결정한다.
$$\widetilde{X} = upsample(X_L) + X_H$$
$$A_H = \sigma(MLP(GMP(\widetilde{X})))$$
$$A_L = \sigma(MLP(GAP(\widetilde{X})))$$
마지막으로 데이터를 다시 분할하여 이러한 학습된 가중치를 적용하여 네트워크가 거시적 해부학과 미세 질감의 완벽한 균형을 유지하도록 한다.
$$X = A_H \odot X_H + A_L \odot X_L$$
실험 아키텍처: 무자비한 증명
저자들은 단순히 깨끗한 데이터셋에 모델을 적용하고 5%의 정확도 향상을 주장하지 않았다. 그들은 수학적 주장을 임상 환경의 혼란스러운 현실에 대해 무자비하게 테스트하도록 설계된 실험을 설계했다.
그들은 완전히 독립적인 두 개의 의료 센터에서 데이터를 수집했다. 한 센터의 데이터는 모델을 훈련하고 내부적으로 테스트하는 데 사용되었으며(1,614개 이미지), 다른 센터의 데이터(2,245개 이미지)는 "외부 테스트 세트"로 잠긴 금고에 보관되었다. 이는 AI가 특정 병원의 CT 스캐너의 특정 특성을 단순히 암기하지 않았음을 보장한다.
희생자들:
저자들은 자신들의 창작물을 세 가지 기준선과 비교했다.
1. 전통적인 팬텀 없는(PL) 선형 회귀 방법 (다중 전압 데이터를 처리하기 위한 수학적 변환 공식으로 조정됨).
2. ResNet-10 (표준적이고 매우 존경받는 딥러닝 모델).
3. OctResNet-10 (공간 중복성을 처리하도록 특별히 설계된 모델).
부인할 수 없는 증거:
그들의 핵심 메커니즘이 120 kVp 및 100 kVp 데이터셋에서 기준선을 능가하는 것(내부적으로 매우 우수한 평균 절대 오차 5.990 $mg/cm^3$, 외부적으로 7.175 $mg/cm^3$ 달성)뿐만 아니라, 진정한 결정적 증거는 그들의 Ablation Study였다.
그들은 체계적으로 모델을 "뇌 절제"했다. 주파수 균형을 껐다. 그런 다음 채널 주의를 껐다. 모든 경우에 오류율이 급증했다. 고/저주파 분리 및 비대칭 GMP/GAP 주의 메커니즘이 모두 협력할 때만 모델이 최고 성능을 달성했다. 이는 가설이 옳았음을 수학적 및 경험적으로 증명했다. 즉, 관 전압 변화에서 살아남으려면 고주파 질감을 분리하고 고유하게 가중치를 부여해야 한다는 것이다.
솔직히 말해서, 외부 데이터셋에서 80 kVp 수준에서 심각한 이미지 저하를 유발하는 정확한 물리적 물리학에 대해서는 완전히 확신할 수 없다. 저자들은 "센터 간 상당한 이미지 품질 차이" 때문에 모델이 해당 수준에서 기준선보다 성능이 떨어졌다고 언급하는데, 이는 극도로 낮은 방사선량에서는 고주파 골소주 데이터가 AI가 볼 수 있기 전에 양자 노이즈에 의해 단순히 파괴될 수 있음을 시사한다.
미래 발전을 위한 토론 주제
이 논문의 심오한 함의를 바탕으로, 미래 탐구 및 비판적 사고를 위한 몇 가지 경로를 제시한다.
-
정보 파괴의 임계값:
80 kVp에서 모델은 외부 데이터에서 어려움을 겪었다. 이는 흥미로운 물리학과 AI의 질문을 제기한다. 정확히 어떤 방사선량에서 고주파 골소주 구조가 "숨겨져 있지만 복구 가능"에서 "광자 부족 및 양자 노이즈에 의해 물리적으로 파괴됨"으로 전환되는가? AI 기반 골밀도 분석에 필요한 방사선의 절대 하한선을 수학적으로 정의할 수 있는가? -
교차 모달 주파수 분리:
고주파 질감을 저주파 전역 조명에서 분리하는 것이 CT 전압 문제를 해결한다면, 이 정확한 수학적 프레임워크를 MRI 또는 초음파에 이식할 수 있을까? 예를 들어, 이 이중 분기 아키텍처가 다른 자기장 강도(1.5T 대 3T)로 인한 저주파 변동을 무시하고 MRI에서 인대의 고주파 미세 파열을 분리할 수 있을까? -
물리적 팬텀의 종말?
경제적 함의는 엄청나다. 소프트웨어가 내부 조직 참조 및 주파수 변환을 사용하여 모든 스캐너의 전압에 안정적으로 동적으로 조정할 수 있다면, 물리적 CT 팬텀을 다시 제조, 배송 및 보정해야 할 필요가 있을까? 생사를 가르는 진단 시나리오에서 물리적 기준 객체를 확률적 신경망으로 대체하는 데 따른 규제 및 법적 장애물은 무엇인가?
다른 분야와의 동형 사상
이 논문을 이해하기 위해서는 먼저 의사들이 골다공증을 진단하는 방식을 살펴볼 필요가 있다. 의사들은 CT 스캔을 사용하여 골밀도(vBMD)를 측정한다. 전통적으로 이는 스캔 중 환자 아래에 놓이는 물리적 보정 객체인 "팬텀"을 필요로 하는데, 이는 비용이 많이 들고 번거롭다. 팬텀리스(PL) 방법은 환자 자신의 내부 조직(지방 및 근육 등)을 참조점으로 사용한다.
이러한 동기는 현대 병원의 중요한 제약 조건인 다양한 방사선량에서 비롯된다. 환자를 과도한 방사선으로부터 보호하기 위해 병원에서는 표준 120 kVp 대신 80 kVp 또는 100 kVp와 같은 낮은 관전압을 점점 더 많이 사용한다. 문제는 관전압을 낮추면 CT 영상의 전역 픽셀 강도(Hounsfield Units, HU)가 크게 변한다는 것이다. 기존의 딥러닝 모델은 이러한 저주파 전역 강도에 크게 의존하기 때문에 관전압이 떨어지면 정확도가 급격히 저하된다. 그러나 저자들은 중요한 생물학적 허점을 발견했다. 전반적인 밝기는 변하지만, 해면골의 고주파 질감은 다양한 관전압에 걸쳐 놀랍도록 안정적으로 유지된다.
이를 해결하기 위해 저자들은 휘발성 거시 데이터와 안정적인 미시 데이터를 수학적으로 분리해야 했다. 전체 이미지를 표준 신경망에 입력하는 대신, 주파수를 분리하기 위해 이중 분기 아키텍처를 구축했다.
먼저, 불필요한 계산 오버헤드를 피하기 위해 공간 주의(spatial attention)와 결합된 푸리에 변환을 사용하여 주파수 특징을 변조한다. 입력 특징 맵 $X$에 대해 변조된 출력 $Y$는 다음과 같이 정의된다:
$$ Y = \sum_{b \in B} \sigma(f(X_b; W_b)) \odot X_b $$
여기서 주파수 대역은 $X_b = \mathcal{F}^{-1}(M_b \odot \mathcal{F}(X))$를 통해 추출되며, $\mathcal{F}$는 푸리에 변환을 나타내고 $M_b$는 이진 주파수 마스크 역할을 한다.
신호가 저주파($X_L$) 및 고주파($X_H$) 구성 요소로 분할되면 병렬 분기에서 처리된다. 이 논문의 진정한 독창성은 이러한 분기가 다시 어떻게 융합되는지에 있다. 저자들은 고주파 데이터(날카로운 뼈 가장자리)와 저주파 데이터(일반적인 뼈 모양)가 서로 다른 수학적 렌즈를 필요로 한다는 것을 인식했다. 그들은 비대칭 채널 주의 메커니즘을 설계했다. 고주파 특징의 날카로운 피크를 포착하기 위해 Global Max Pooling(GMP)을 적용하고, 저주파 특징을 부드럽게 하고 포착하기 위해 Global Average Pooling(GAP)을 적용한다:
$$ A_H = \sigma(MLP(GMP(\tilde{X}))) $$
$$ A_L = \sigma(MLP(GAP(\tilde{X}))) $$
이러한 주의 가중치는 분리된 신호를 동적으로 재결합하는 데 사용된다:
$$ \tilde{X} = A_H \odot X_H + A_L \odot X_L $$
이 방정식은 관전압 변화로 인해 저주파 전역 강도가 신뢰할 수 없게 될 때 네트워크가 안정적인 고주파 질감에 적응적으로 의존할 수 있도록 한다.
본질적으로, 이 연구의 구조적 골격은 복잡한 신호를 휘발성 거시 기준선과 안정적인 미시 변동으로 분리하고, 이를 병렬로 처리하며, 비대칭 가중 함수를 사용하여 동적으로 재결합하여 다양한 환경 조건에 걸쳐 불변의 척도를 추출하는 메커니즘이다.
이러한 골격을 기반으로 우리는 완전히 다른 과학 및 공학 분야에서 이 논리의 정확한 "거울 이미지"를 찾을 수 있다:
1) 계량 금융: 알고리즘 거래에서 자산 가격은 거시 경제 추세(저주파, 금리 인상과 같은 외부 "전압"에 매우 민감함)와 미시 구조 주문 책 동학(고주파, 안정적이고 본질적인 거래 행동을 나타냄)으로 구성된다. 시장 전체의 노이즈를 내재적 미세 변동성에서 분리하여 자산의 진정한 기본 가치를 추출하는 것은 CT 전역 강도를 해면골 질감에서 분리하는 것과 직접적으로 유사하다.
2) 지진학: 지진의 규모를 감지할 때 지진계는 저주파 표면파(국지적 토양 유형에 의해 크게 왜곡되어 다양한 CT 관전압과 유사하게 작용함)와 고주파 체파(단층선의 파열에 대한 진정한 안정적인 신호를 전달함)를 기록한다. 지진학자들은 지진의 불변의 진실을 찾기 위해 이러한 주파수 간의 균형을 맞추기 위해 끊임없이 노력한다.
계량 금융 연구자가 내일 이 논문의 정확한 비대칭 주의 방정식을 "훔친다면" 어떻게 될까? 만약 그들이 고주파 거래 알고리즘에 $$ \tilde{X} = A_H \odot X_H + A_L \odot X_L $$을 적용한다면, 그들은 Global Max Pooling을 사용하여 주문 책 이상(즉, "해면골" 거래)의 절대 피크를 공격적으로 포착하는 동시에 Global Average Pooling을 사용하여 휘발성 거시 경제 심리를 완화할 수 있다. 이러한 돌파구는 광범위한 시장이 갑자기 고변동성 또는 저변동성 체제로 전환되더라도 예측 정확도와 수익성을 유지하는, 즉 알고리즘을 시장 "관전압" 변동에 면역으로 만드는 혁신적으로 강력한 거래 봇이 될 것이다.
궁극적으로, 이 아키텍처는 우리가 쇠퇴하는 뼈의 밀도를 측정하든, 변동하는 금융 자산의 숨겨진 가치를 측정하든, 불변의 진실을 추구하는 수학적 과정이 분리된 주파수와 적응적 주의의 정확히 동일한 교향곡에 의존한다는 것을 증명하며, 보편적 구조 라이브러리에 훌륭한 새로운 청사진을 추가한다.
