ニンシャ、中国におけるブルセラ症の差別化された最適制御戦略:2パッチ動的モデルからの洞察
As a high-incidence region of brucellosis in China, the incidence pattern of brucellosis in Ningxia shows a significant spatial-temporal heterogeneity, thus, it is of significance to allocate the differentiated...
背景と学術的系譜
起源と学術的系譜
本稿で取り上げる問題は、特に中国寧夏のような高発生地域における人獣共通感染症であるブルセラ症の持続的かつ空間的に不均一な性質に由来する。歴史的に、ブルセラ症は地中海、中東、アジアの一部を含む地域で大きな蔓延が見られ、世界的な懸念事項であったことが初期の文献で指摘されている[1]。中国では、1990年代半ばから同疾患が顕著に再興し、2014年にピークを迎えた。その地理的拡大は、伝統的な牧畜地域から農業地域、さらには南部の沿岸地域にまで及んだ[3]。この拡大は、同疾患の二重の脅威を浮き彫りにした。すなわち、動物の不妊や生産性の低下による畜産業への甚大な経済的損失[4, 5]と、世界中で毎年数十万件のヒト症例が報告される深刻な公衆衛生リスク[2]である。
この特定の問題の発生は、ブルセラ症の伝播が顕著な時空間的異質性とクラスター化を示すという観察に起因する[6, 7]。特に高リスク地域から低リスク地域への地域間家畜移動[8]や、気圧・気温などの環境条件[9]は、その拡散に深く影響を与える。これまでの疫学研究は、主に予測のための統計モデルに依存していた。しかし、これらのモデルでは、異なる場所や時間における疫病と人間の活動および自然環境との複雑な動的な相互作用を捉えることに限界があった。この根本的な限界は、高リスク地域を正確に特定し、予防および制御のための差別化された資源配分を促進できる、より洗練されたアプローチの喫緊の必要性を生み出した。したがって、動的モデリングは、この空間的異質性の影響を定量化し、最適で調整された予防戦略を策定するための不可欠なツールとなった[10-12]。本稿は、羊におけるB. melitensisによって引き起こされるブルセラ症の深刻な流行地域である寧夏に焦点を当て、限られた保健資源を考慮した、正確で差別化された制御戦略のための定量的基盤を提供することを目的とする。
直感的領域用語
- ブルセラ症 (Brucellosis): 感染した動物(羊など)からヒトに容易に感染し、両者に長期的な疾患を引き起こす、非常にしつこい「動物インフルエンザ」を想像してほしい。農家にとっては二重の打撃である。動物が病気になり流産や乳・肉の減少を引き起こし、人間自身も感染する可能性がある。
- 時空間的異質性 (Spatial-temporal heterogeneity): 病気が均一な霧のように広がるのではなく、むしろまだらで変化する嵐のように広がる様子を想像してほしい。ある町では他の町よりもはるかに悪く、その強度は季節や数年で変化する。これは、病気が常に同じ強さでどこにでもあるわけではないことを意味する。
- パッチモデル (Patch model): ある地域の地図をいくつかの異なるゾーンまたは「近隣」に分割したものを想像してほしい。パッチモデルは、各ゾーン内での病気の広がりと、それらが互いにどのように移動するかを追跡するようなものであり、各ゾーンが異なる条件やリスクレベルを持つ可能性があることを認識している。
- 基本再生産数 ($R_0$) (Basic reproduction number): これは病気の「伝染スコア」のようなものである。1匹の感染した動物が平均して1匹以上の他の動物に感染させる場合、スコアは1を超え、病気は広がる可能性が高い。1匹未満に感染させる場合、スコアは1を下回り、病気はいずれ消滅する。
- 最適制御戦略 (Optimal control strategy): 限られた兵士と物資で戦争に勝とうとする将軍を想像してほしい。最適制御戦略とは、将軍にいつ、どこで、どれだけ資源(ワクチン、移動制限など)を投入すれば最も効果的に勝利(病気の最小化)を達成できるかを正確に指示する、最善の戦術計画である。
記法表
| 記法 | 説明 |
|---|---|
問題定義と制約
中核問題の定式化とジレンマ
本稿で取り上げる中核問題は、ブルセラ症の発生率が高く、同疾患の時空間的異質性が著しい地域である中国寧夏における、効果的かつ差別化された最適制御戦略の開発である。
入力または現在の状態は、ブルセラ症の伝播が明確な時空間パターンを示し、高リスク地域と低リスク地域を生み出している(図1に示す)複雑な疫学的状況である。予防および制御のための保健資源は限られており、均一な介入戦略は非効率的で、しばしば実行不可能である。さらに、地域間の家畜移動は病気の拡散の既知の要因であり、制御努力を複雑にしている。主に統計モデルに依存するこれまでの研究は、複雑な時空間的動態と、人間の活動および自然環境との相互作用を捉えるのに苦労してきた。ワクチン接種は利用可能で(例:有効率約65%のM5ワクチン)、ある程度効果的であるが、資源不足のため、すべての地域で均一な接種率を達成することは困難である。
望ましい終点または目標状態は、ワクチン資源の合理的な配分と効果的な輸送監督の実施により、高リスクおよび低リスクパッチの両方における累積感染羊個体数を削減することである。これには、異なる地域の特定の危険度レベルに合わせた正確な制御戦略を情報提供するための定量的フレームワークが必要である。
本稿が埋めようとしている正確な欠落リンクまたは数学的ギャップは、空間的異質性(2パッチシステム)とワクチン接種効果の両方を統合する、堅牢で空間的に明示的な動的モデルと、最適制御フレームワークの欠如である。具体的には、本稿は、差別化された介入を考慮し、一般的な戦略を超えて資源効率的で標的化されたアプローチへと移行する、最適制御解を数学的に導出し評価することを目的とする。
これまでの研究者を悩ませてきた痛みを伴うトレードオフまたはジレンマであり、本稿がナビゲートしようとしているのは、固有の時空間的異質性に対処しながら、深刻な資源制約下で包括的な疾患制御を達成するという課題である。しばしば、ある地域またはある方法(例:広範なワクチン接種)での制御を改善することは、指数関数的に多くの資源を必要とし、それは単に利用できない。ジレンマは、移動パターンによってさらに悪化する。移動は低リスクパッチでのブルセラ症のリスクを高める可能性があるが、高リスク地域では「希釈効果」(11ページの注釈2)を持つ可能性もあり、単純で差別化されていない制御措置は、特定のパッチで状況を意図せず悪化させたり、貴重な資源を誤って配分したりする可能性がある。著者らは、介入が効果的かつ資源に配慮したものであることを保証し、バランスを見つけることを目指している。
制約と失敗モード
寧夏におけるブルセラ症制御の問題は、いくつかの厳しい現実的な制約によって極めて困難になっている。
-
物理的/生物学的制約:
- 人獣共通感染症と伝播ダイナミクス: ブルセラ症は主に感染動物(羊)からヒトに伝播する人獣共通感染症であり、動物の健康と公衆衛生の両方に関わるため、制御努力は複雑になる。小反芻獣における最も病原性の高い種であるB. melitensisは寧夏で蔓延している(3ページ)。
- 時空間的異質性: ブルセラ症の発生率は、空間的および時間的に著しい変動を示し、均一なアプローチではなく差別化されたアプローチが必要となる(1ページ、要旨)。
- 家畜移動: 地域間家畜移動は病気の拡散の主要な推進要因である(2ページ)。国境管理と輸送監督は重要であるが、完全に施行することは困難である。
- ワクチン接種の有効性: ワクチンは存在するが、その有効性は100%ではない(M5ワクチンの場合約65%、3ページ)。したがって、ワクチン接種だけでは病気を完全に根絶することはできない。
-
計算的/数学的制約:
- 複雑な疫病ダイナミクス: ブルセラ症の伝播ダイナミクスは、異なるパッチ間の感受性、感染性、およびワクチン接種された個体群との複雑な相互作用を伴い、より単純な統計モデルでは効果的に捉えることが困難である(2ページ)。
- 最適制御問題の複雑性: 最適制御解を導出するには、状態変数と関連する共状態変数の微分方程式系を解く必要があり、しばしば非線形関数とポントリャーギンの最大原理の適用(第4節、11ページ)が含まれる。制御変数 $u_i(t)$ は $[0, 1]$ の範囲に制限され、介入努力の実行可能な範囲を表す。
-
データ駆動型制約:
- 羊の感染に関するデータ不足: 重要な制約は、「羊の群れにおけるブルセラ症感染に関する直接的なデータの欠如」である(16ページ)。このため、著者らは線形回帰モデル(式5.1)を用いてヒトブルセラ症陽性率から羊の感染率を間接的に推定せざるを得ない。この間接的な推定は、$R^2$値が高いにもかかわらず、潜在的な「データバイアス」を導入する(21ページ)。
- モデルの単純化: 現在のモデルは、各パッチ内での羊の均一な混合を仮定しており、病気の広がりに対する個体群構造(例:年齢、繁殖タイプ)の影響を無視している(21ページ)。
- 決定論的モデルの限界: モデルの決定論的な性質は、感染した羊の確率的移動など、伝播に影響を与える可能性のあるランダムなイベントを完全に捉えることができない(21ページ)。
-
資源制約:
- 限られた保健資源: 最も重要な制約は、ブルセラ症の予防および制御に利用可能な「限られた保健資源」である(1ページ、要旨;3ページ)。これは、広範で均一な介入を実施する能力に直接影響する。
- 限られた免疫資源: 特に、免疫のための資源が限られているため、地域全体で均一なワクチン接種率を達成することは困難である(3ページ)。
- 不均一な資源配分: 保健資源は「比較的均一に配分されていない」(20ページ)ため、公平で効果的な制御努力をさらに複雑にしている。
なぜこのアプローチか
選択の必然性
2パッチ感受性-感染性-ワクチン接種済み(SIV)羊動的モデルと最適制御理論の採用は、寧夏におけるブルセラ症伝播の固有の複雑さを考慮すると、単なる選択ではなく必然的な必要性であった。著者らは、多くの疫学研究で以前のゴールドスタンダードを形成してきた統計モデルのような、従来の「SOTA」手法の限界を明確に認識していた。導入部で述べられているように、「既存の研究は主に疫病予測のための統計モデルの使用に焦点を当てているが、これらのモデルは疫病伝播の複雑なダイナミクスを処理する上で限界があり、人間の活動や自然環境との時空間的相互作用を効果的に捉えることが困難である。」この認識は、純粋な統計的手法からの脱却が不可欠となったまさにその瞬間であった。
統計モデルは予測に有用であるが、しばしば病気の広がり、個体群移動、および介入効果の時間的・空間的相互作用のメカニズム的な表現を苦手とする。寧夏におけるブルセラ症は顕著な時空間的異質性を示し、その有病率は地理的地域によって大きく異なり、時間とともに変化する。これらの複雑なダイナミクスを特徴づけ、そして最も重要なこととして、最適かつ差別化された制御戦略を策定するためには、動的モデリングフレームワークが唯一実行可能な道であった。SIVのようなコンパートメントモデルは、個体群の状態(感受性、感染性、ワクチン接種済み)とその間の遷移を明示的に表現することを可能にし、統計的相関だけでは提供できないメカニズム的な理解を提供する。
比較優位性
この2パッチSIV動的モデルは、複雑で相互作用する疫学的プロセスを捉え、最適化する構造的能力を通じて、以前のアプローチに対して質的な優位性を提供する。単純な統計モデルとは異なり、結果を予測するだけでなく、病気がなぜ、どのように広がり、どの介入が最も効果的であるかを理解するためのフレームワークを提供する。
- 時空間的異質性: 図1に示すように、「高リスク」と「低リスク」のパッチへの分割は、根本的な構造的利点である。これにより、モデルは異なる地理的地域における異なる疾患ダイナミクスと介入ニーズを考慮することができ、寧夏のような地域にとって極めて重要である。
- 動的な相互作用と移動: モデルは、感受性、感染性、ワクチン接種済みの羊のパッチ間の移動率($a_{12}, a_{21}, b_{12}, b_{21}, c_{12}, c_{21}$)を明示的に組み込んでいる。これは、単一パッチモデルや、移動の影響を見落とす可能性のある統計的手法に対する重要な構造的改善である。注釈2が強調するように、移動を無視すると、「異なるパッチの基本再生産数を過大評価または過小評価する」可能性がある。
- 最適制御フレームワーク: ポントリャーギンの最大原理を用いて最適制御解($u_1$から$u_6$)を導出することの統合は、重要な質的飛躍である。これにより、異なる介入戦略(個人保護、ワクチン接種、移動監督)の定量的評価と、限られた資源の制約下でのそれらの最適配分が可能になる。これは、静的な有効性の評価だけでなく、時間依存的な実行可能な戦略を提供することで、単純なパフォーマンス指標を超えている。
- メカニズム的理解: SIV構造は、疾患伝播、回復、免疫のための明確で解釈可能なメカニズムを提供し、ブラックボックス予測モデルよりも政策策定に対してより堅牢である。基本再生産数($R_0$)のような主要な疫学的パラメータの計算を可能にし、疾患の持続性と安定性に関する洞察を提供する。
本稿では、高次元ノイズ処理やメモリ複雑性については議論していない。これらは、この種の疫学モデリングとその関連代替案(統計モデル、より単純なODEモデル)との間の主要な比較軸ではないからである。その優位性は、空間的相互作用を伴う複雑な動的システムをモデル化し、そのシステム内で介入を最適化する能力にある。
制約との整合性
選択された2パッチSIV動的モデルと最適制御理論は、問題の厳しい要件と完全に整合し、問題と解決策の堅牢な「結婚」を形成している。
- 空間的異質性: 問題は、寧夏を「顕著な時空間的異質性」を持つ高発生地域として明確に特定している。2パッチ構造(高リスクと低リスク)は、各地域で異なるパラメータとダイナミクス、およびそれらの間の相互作用を可能にすることで、これを直接的に満たす。
- 限られた保健資源: 中核的な制約は、「限られた保健資源」の下で予防および制御目標を達成する必要性である。最適制御フレームワークは、本質的にこのために設計されている。目的関数(4.2)を、累積感染個体数と制御努力に関連するコストの両方を最小化するように定義することで、モデルは希少な資源の最も効率的な配分戦略を提供する。
- 差別化された制御戦略: 「差別化された制御戦略」の要求は、両パッチにおける様々な介入(個人保護、ワクチン接種、移動監督)のための6つの異なる制御関数($u_1$から$u_6$)を定義するモデルの能力によって満たされる。最適制御解は、これらの制御の理想的な時間変化する適用を決定し、各パッチの特定の危険度プロファイルに合わせた戦略につながる。
- 介入効果の定量化: 問題は、ワクチン接種と輸送監督の予防効果を定量化することを必要とする。SIVモデルは、ワクチン接種コンパートメント($V_i$)と制御変数(ワクチン接種のための$u_2, u_5$;移動監督のための$u_3, u_6$)を明示的に含んでおり、これらはこれらのプロセスを直接調整し、最適制御フレームワーク内でのそれらの定量的評価を可能にする。
代替案の却下
本稿は、中核問題の特性に対処できないという理由で、いくつかの代替アプローチを暗黙的かつ明示的に却下している。
- 統計モデル: 最も直接的な却下は、「疫病予測のための統計モデル」である。著者らは、これらのモデルが「疫病伝播の複雑なダイナミクスを処理する上で限界があり、人間の活動や自然環境との時空間的相互作用を効果的に捉えることが困難である」と述べている。これは、動的な広がりと最適な介入のメカニズム的な理解を必要とする問題に対するそれらの不十分さを強調している。
- 単一パッチ動的モデル: 明示的に名前は挙げられていないが、本稿の「時空間的異質性」への強調と「2パッチ」モデルの構築は、単一パッチモデルを本質的に却下している。注釈2は、単一パッチモデルで移動を無視すると「異なるパッチの基本再生産数を過大評価または過小評価する可能性がある」と説明し、不正確な評価と最適化されていない戦略につながることで、これをさらに強化している。「地域間協調複合制御戦略」の必要性も、マルチパッチアプローチを必要とする。
- 確率的事象に対する決定論的モデル: 「限界」セクション(第6節)で、著者らは、決定論的モデルが「感染した羊の確率的移動のようなランダムなイベント」を記述できないことを認めている。これは、確率論が重要な役割を果たすシナリオに対して、純粋に決定論的なモデルを使用することの却下を示唆しており、将来の研究では確率的プロセスが組み込まれる可能性を示唆している。
- 一般的な機械学習モデル(例:GAN、拡散、Transformer): プロンプトではこれらを「SOTA」手法として言及している。しかし、最適制御のための疫学モデリングの文脈では、これらは直接的な代替案ではない。これらは異なるタスク(例:画像生成、自然言語処理)のために設計されており、疾患伝播ダイナミクスをモデル化し、解釈可能な制御ポリシーを導出するために必要なメカニズム構造を欠いている。本稿では、これらの特定の種類のモデルについては言及または却下していない。これらは、伝統的な疫学モデリングの比較の範囲外にあるからである。関連する代替案は、疫学および数学モデリングの領域内にある。
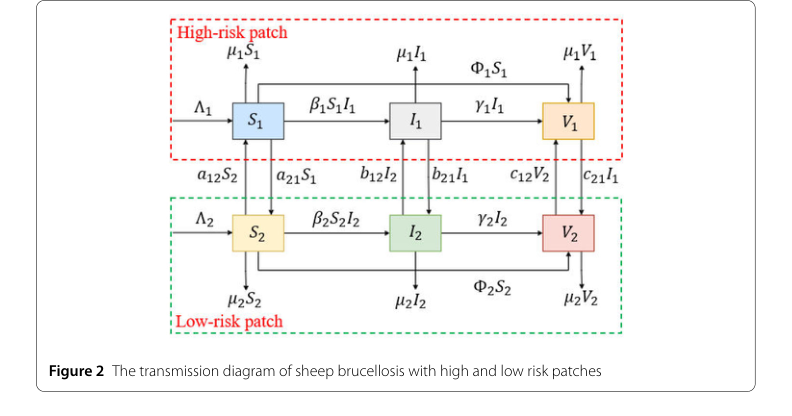 Figure 2. The transmission diagram of sheep brucellosis with high and low risk patches
Figure 2. The transmission diagram of sheep brucellosis with high and low risk patches
数学的・論理的メカニズム
マスター方程式
本稿の数学的エンジンの絶対的な核心は、ブルセラ症の疫病とそれに対する制御努力に関連する全体的なコストを定量化する目的関数である。目標は、指定された時間枠 $T$ におけるこの関数の最小化である。これは次のように表される。
$$ J = \int_0^T \left[ A_1I_1(t) + A_2I_2(t) + \frac{1}{2} \sum_{i=1}^6 B_i u_i^2(t) \right] dt $$
この方程式は、制御下にある2パッチSIV(感受性-感染性-ワクチン接種済み)モデルの羊個体群のダイナミクスを記述する常微分方程式(ODE)系と組み合わさって、完全な最適制御問題を形成する。羊個体群のダイナミクスを定義するODEは、$I_1(t)$、$I_2(t)$、および $u_i(t)$ の効果が時間とともにどのように進化するかを決定するため、暗黙的にこのメカニズムの一部である。
項ごとの解剖
マスター方程式とその構成要素、および基礎となる動的システムに影響を与える制御変数を分解してみよう。
-
$J$:
- 数学的定義: 総累積コストを表すスカラー値。
- 物理的/論理的役割: これは著者らが最小化しようとする量である。介入期間全体にわたる感染個体群(疫病の負担)と制御戦略に費やされた資源の包括的な尺度として機能する。
- なぜ積分か: システムのダイナミクスは時間とともに連続的であるため、積分は、初期時刻 $t=0$ から最終時刻 $t=T$ まで、瞬間的なコストを連続的に合計するために使用される。これにより、スナップショットではなく、合計の累積コストが得られる。
-
$\int_0^T \dots dt$:
- 数学的定義: 時間区間 $[0, T]$ における定積分。
- 物理的/論理的役割: この演算子は、制御介入の全期間にわたって、被積分関数(特定の瞬間のコスト関数)の瞬間的な値を累積する。
- なぜ積分か: 状態変数と制御アクションは時間の連続関数と見なされるため、積分は連続期間にわたるそれらの効果を合計するための自然な数学的ツールである。
-
$A_1I_1(t)$:
- 数学的定義: 正の重み係数 $A_1$ と時刻 $t$ におけるパッチ1の感染羊数 $I_1$ の積。
- 物理的/論理的役割: この項は、高リスクパッチ(パッチ1)の感染個体群に関連する瞬間的なコストまたは負担を表す。 $A_1$ が高いほど、$I_1$ を削減するための最適化が促進される。
- なぜ加算か: これは望ましくない結果(感染)を表すため、総コストに加算される。
-
$A_2I_2(t)$:
- 数学的定義: 正の重み係数 $A_2$ と時刻 $t$ におけるパッチ2の感染羊数 $I_2$ の積。
- 物理的/論理的役割: $A_1I_1(t)$ と同様に、この項は低リスクパッチ(パッチ2)の感染個体群に関連する瞬間的なコストを表す。 $A_2$ は $I_2$ を削減することの重要性を重み付けする。
- なぜ加算か: 総コストへの加算成分であり、別の負担源を反映している。
-
$A_1, A_2$:
- 数学的定義: 正の定数係数。
- 物理的/論理的役割: これらは、モデラーが各パッチでの感染個体群を削減することの相対的な重要性を割り当てることを可能にする「調整パラメータ」である。例えば、$A_1 > A_2$ の場合、パッチ1での感染を削減することがパッチ2での感染を削減することよりも重要またはコストが高いことを意味する。
- なぜ係数か: 制御戦略の目的のバランスを取る柔軟性を提供する。
-
$I_1(t), I_2(t)$:
- 数学的定義: それぞれパッチ1とパッチ2の感染羊数を時刻 $t$ で表す状態変数。これらは非負の実数である。
- 物理的/論理的役割: これらは制御戦略の主な標的である。 $J$ を最小化することは、直接これらの個体群を削減することを目的とする。それらのダイナミクスは、ODE系(4.1)によって支配される。
-
$\frac{1}{2} \sum_{i=1}^6 B_i u_i^2(t)$:
- 数学的定義: 正の係数 $B_i$ で重み付けされた6つの制御変数それぞれに対する二次項の合計の半分。
- 物理的/論理的役割: この項は、制御戦略を実施するコストの瞬間的なコストを表す。二次形式($u_i^2$)は、より強力な制御努力を適用すると、不釣り合いに高いコストがかかることを意味し、過剰または非現実的な介入を抑制する。これにより、コストは常に非負になる。
- なぜ合計か: 6つの異なる制御測定があり、それらの個々のコストが集計されて総制御コストが形成される。
- なぜ二次($u_i^2$)か: 二次形式は、いくつかの理由で最適制御における標準的な選択である。常に正のコストを保証し、より大きな制御努力をより重く罰し(最適化が「より懸命に働く」ようにする)、目的関数の凸性に寄与することが多く、一意の最適解を見つけることを容易にする。
-
$B_i$:
- 数学的定義: 各制御変数 $u_i$ に対する正の定数係数。
- 物理的/論理的役割: これらの係数は、各特定の制御測定の適用コストの相対的なコストを決定する。 $B_i$ が高いほど、制御 $u_i$ は実装するのがより高価または資源集約的になる。
- なぜ係数か: 感染の削減と特定の介入のコストとのバランスを微調整することを可能にする。
-
$u_i(t)$ ($u_1, \dots, u_6$):
- 数学的定義: $[0, 1]$ の範囲に制限された、時間依存の制御関数。
- 物理的/論理的役割: これらは、最適化プロセスが決定しようとする決定変数である。それらは、異なる制御測定の強度または有効性を表す。
- $u_1(t)$: パッチ1における個人保護行動の制御効果。ODEでは、実効伝播率 $(1-u_1)\beta_1S_1I_1$ を削減する。
- $u_2(t)$: パッチ1におけるワクチン接種の制御効果。ODEでは、感受性羊 $S_1$ をワクチン接種済みクラス $V_1$ に率 $u_2S_1$ で移動させる。
- $u_3(t)$: パッチ1からパッチ2への移動に対する制御効果。ODEでは、パッチ1からパッチ2への $S_1, I_1, V_1$ の流出を削減する。
- $u_4(t)$: パッチ2における個人保護行動の制御効果。 $u_1$ と同様に、実効伝播率 $(1-u_4)\beta_2S_2I_2$ を削減する。
- $u_5(t)$: パッチ2におけるワクチン接種の制御効果。 $u_2$ と同様に、感受性羊 $S_2$ を率 $u_5S_2$ で $V_2$ に移動させる。
- $u_6(t)$: パッチ2からパッチ1への移動に対する制御効果。 $u_3$ と同様に、パッチ2からパッチ1への $S_2, I_2, V_2$ の流出を削減する。
ステップバイステップの流れ
システムを、羊の個体群がコンパートメントとパッチ間を移動し、制御レバーの影響を受ける、複雑に相互接続された組立ラインとして想像してほしい。
- 初期状態設定: プロセスは、高リスク(パッチ1)と低リスク(パッチ2)の両方の地域における感受性($S_1(0), S_2(0)$)、感染性($I_1(0), I_2(0)$)、およびワクチン接種済み($V_1(0), V_2(0)$)羊の定義された初期数で始まる。これらの初期条件は、疫病の軌跡の開始点を設定する。
- 制御レバー調整: いずれかの瞬間 $t$ で、6つの制御レバー($u_1(t)$から$u_6(t)$)は、介入の強度を表す特定の値に設定される。例えば、$u_2(t)$ が高い場合、パッチ1で強力なワクチン接種キャンペーンが実施されていることを意味する。 $u_3(t)$ が高い場合、パッチ1からパッチ2への羊の移動を制限するために厳格な措置が講じられていることを意味する。
- 個体群ダイナミクスシミュレーション: これらの制御設定は、6つの連立ODE(4.1)で記述されるように、両パッチの各羊個体群の変動率に直接影響を与える。
- 感染削減: 制御 $u_1$ と $u_4$ は「盾」のように機能し、それぞれのパッチで感受性羊が感染する速度を削減する。
- ワクチン接種ドライブ: 制御 $u_2$ と $u_5$ は「コンベア」のように機能し、感受性羊をワクチン接種済みコンパートメントに移動させ、免疫を与える。
- 移動管理: 制御 $u_3$ と $u_6$ は「ゲートキーパー」のように機能し、両パッチ間の感受性、感染性、ワクチン接種済みの羊の移動を規制する。例えば、$u_3$ はパッチ1からパッチ2への羊の流出を削減し、$u_6$ はパッチ2からパッチ1への羊の流出を削減する。
- 自然プロセス: 出生率($A_1, A_2$)、自然死亡率($\mu_1, \mu_2$)、回復率($\gamma_1, \gamma_2$)とともに、継続的に個体群サイズに影響を与える。
- 瞬間コスト計算: 個体群が進化するにつれて、各瞬間 $t$ で2種類のコストが計算される。
- 疫病負担: 各パッチの現在の感染羊数($I_1(t)$ および $I_2(t)$)は、$A_1$ および $A_2$ で重み付けされてコストに寄与する。これは、病気の継続的な影響を測定する「メーター」のようなものである。
- 介入費用: 制御レバー($u_i(t)$)の現在の設定も、 $B_i$ および二乗で重み付けされたコストを発生させる。これは、介入によって消費されるリソース量を「燃料計」で示すようなものである。
- 総コスト累積: これらの瞬間的なコストは、積分演算子によって介入期間全体($t=0$から$t=T$まで)にわたって連続的に合計され、単一の総コスト値 $J$ が得られる。
- 最適化ループ(概念): アセンブリライン全体が、制御レバー($u_i(t)$関数)の異なる設定で繰り返し実行される。目標は、最終的な累積コスト $J$ を可能な限り小さくする特定の制御関数のセットを見つけることである。この最適制御戦略の探索が、最適化ダイナミクスの本質である。
最適化ダイナミクス
メカニズムは、最適制御理論の基本的なツールであるポントリャーギンの最大原理の適用を通じて学習、更新、収束する。この原理は、状態方程式(個体群ダイナミクス)にそれぞれコスト係数($\lambda_{ij}$)を乗じたものと、目的関数(瞬間コスト)の被積分関数を組み合わせたハミルトニアン関数を構築することから始まる。コスト係数は、各状態変数が全体的な目的関数に与える限界貢献度または「影の価格」を本質的に表す。
- ハミルトニアン定式化: 最初のステップは、ハミルトニアン関数 $H$ を、式(4.10)で定義されているように構築することである。この関数は、目的関数の被積分関数(瞬間コスト)と、状態方程式(個体群ダイナミクス)の右辺を、それぞれ対応する「コスト係数」($\lambda_{ij}$)で重み付けして組み合わせる。コスト係数は、各状態変数が全体的な目的関数に与える限界貢献度または「影の価格」を本質的に表す。
- コスト係数方程式(随伴系): 最適経路を見つけるには、コスト係数がどのように進化するかを理解する必要がある。これは、コスト係数の微分方程式系(式(4.11))を導出することによって行われる。これらの式は、ハミルトニアンの状態変数に対する偏微分を取ることによって得られる。重要なのは、状態方程式が時間方向に前進するのに対し、コスト係数方程式は通常、終端条件(ここでは、制御期間の終了時の状態に対する将来のコストがないことを意味する $\lambda_{ij}(T) = 0$)から始まって、時間方向に後方に解かれることである。
- 制御の最適性条件: 最適制御を見つける核心は、各時間点での制御変数に関するハミルトニアンの偏微分をゼロに設定すること($\frac{\partial H}{\partial u_i} = 0$)によって、ハミルトニアンを最小化することにある。これにより、最適制御 $u_i^*$ (式(4.12))の明示的な表現が得られる。これらは通常、状態変数($S_i, I_i, V_i$)とコスト係数($\lambda_{ij}$)の両方の関数として「クリップ」または実行可能な制御集合に投影される。
- 反復解法(前方-後方スイープ): 状態方程式(時間方向に前方)とコスト係数方程式(時間方向に後方)は、ハミルトニアンと制御の最適性条件を通じて結合されている。これは、直接解くことができない2点境界値問題を形成する。代わりに、しばしば前方-後方スイープと呼ばれる反復数値法が採用される。
- 初期推測: $[0, T]$ の全時間範囲にわたる制御関数 $u_i(t)$ の初期推測が行われる(例:すべてゼロまたはランダムな値)。
- 前方スイープ: 現在の制御推測を使用して、状態方程式(4.1)は初期条件とともに $t=0$ から $t=T$ まで時間方向に積分される。これにより、すべての個体群サイズ($S_i(t), I_i(t), V_i(t)$)の軌跡が得られる。
- 後方スイープ: 前方スイープから得られた状態軌跡を使用して、コスト係数方程式(4.11)は終端条件とともに $t=T$ から $t=0$ まで時間方向に積分される。これにより、すべてのコスト係数($\lambda_{ij}(t)$)の軌跡が得られる。
- 制御更新: 更新された状態とコスト係数の軌跡を使用して、最適性条件(4.12)が新しい、改善された制御関数 $u_i(t)$ のセットを計算するために使用される。
- 収束チェック: ステップ2〜4が繰り返される。制御関数、状態変数、およびコスト係数の変化が事前に定義された許容誤差を下回る場合、プロセスは収束したと見なされ、反復的な洗練によりメカニズムは最適制御戦略を「学習」できる。
- 損失ランドスケープと勾配: 目的関数 $J$ は多次元の「損失ランドスケープ」を定義する。最適化プロセスは、本質的にこのランドスケープをナビゲートする。コスト係数は、このランドスケープにおける最も急な上昇(または最小化のための下降)の方向を示す一般的な勾配と考えることができる。制御のための目的関数における二次項($B_i u_i^2$)は、このランドスケープを凸にするのに寄与し、これは一般的に反復プロセスが単一のグローバル最小値に収束することを保証するため、望ましい特性である。反復更新は、総コストを削減する方向に制御を調整し、実質的に損失ランドスケープを下って最小値に達し、感染の削減と介入コストの最小化との最適なバランスを表す。目的関数におけるコストと利益の慎重なバランスがこのランドスケープを形成し、収束を実用的な解決策に導く。
結果、限界、結論
実験デザインとベースライン
数学的主張を厳密に検証するために、著者らは包括的な実験的検証プロセスに着手した。アプローチの中核は、2010年から2019年までの中国寧夏の実際の監視データを使用して、2パッチSIV羊ブルセラ症モデル(モデル2.1)をキャリブレーションすることであった。重要な課題は、羊のブルセラ症感染に関する直接的な歴史データの欠如であった。これを克服するために、著者らは2022年から2024年にかけて寧夏で観察されたヒトブルセラ症陽性率(人口10万人あたり)から羊のブルセラ症陽性率($x$)を推定するために、巧妙に線形回帰分析を使用した。これにより、堅牢な線形回帰方程式が得られた:$y = 0.0044x + 2.5822 + \epsilon$、ここで $\epsilon \sim N(0,0.1544)$ であり、印象的な決定係数 $R^2 = 0.9962$ を誇る(図4aに示す)。この関係により、2010年から2019年までの高リスクおよび低リスクパッチにおける羊の新規感染症例を推定することができた。
この推定データを用いて、モデル(2.1)は最小二乗法によってキャリブレーションされた。モデルの初期条件は、高リスクパッチでは $S_1(0) = 1,898,000$、$I_1(0) = 42,724$、$V_1(0) = 0$、低リスクパッチでは $S_2(0) = 2,353,000$、$I_2(0) = 9091$、$V_2(0) = 0$ と設定された。出生率、伝播係数、ワクチン接種率、自然死亡率、回復率、およびパッチ間の移動率を含む様々なパラメータは、データから適合されたり、計算されたり、既存の文献から引用されたりした(表1に詳述)。
提案された最適制御戦略と比較されたベースラインモデルまたは「犠牲者」は、本質的に制御介入が適用されなかったシナリオであった。この「制御なし」の状態は、それらのコアメカニズム、すなわちポントリャーギンの最大原理から導出された差別化された最適制御戦略の有効性を明確に実証するためのベンチマークとして機能した。様々な制御の組み合わせの下での感染羊症例の累積変化をこのベースラインと比較することにより、彼らは提案された介入が疾患の有病率を大幅に削減できるという否定できない証拠を求めた。
証拠が証明すること
本稿で提示された証拠は、提案された差別化された最適制御戦略の有効性を強く支持している。第一に、モデルのキャリブレーションは非常に成功した。高リスクおよび低リスクパッチにおける新規感染羊症例の適合結果(図4bおよび4c)は、推定された歴史データと優れた一貫性を示した。この一貫性は、モデルの予測能力とそれに続く最適制御分析の強固な基盤を提供する。
特に図5に示された数値シミュレーションは、最適制御解の存在とその動的な振る舞いが時間とともに明らかになった。それらのアプローチのコアメカニズム、すなわち2パッチSIVモデルへの最適制御理論の適用は、特定の介入プロファイルを特定することによって、現実世界で機能することが示されている。
- 高リスクパッチでのワクチン接種 ($u_2$): この制御変数は、介入期間中、常に最大値を維持し、高リスク地域でのブルセラ症制御におけるその重要な役割を強調した。
- 低リスクパッチでのワクチン接種 ($u_5$): この介入は当初、かなりの影響を示したが、その後、後期段階でゼロに低下した。これは、長期にわたって低リスク地域で持続的な高ワクチン接種率が必要ではない可能性を示唆している。
- 低リスクから高リスクパッチへの輸送の制限 ($u_6$): この制御は当初、比較的高いレベルを維持したが、その後低下した。これは、高リスク地域への疾患再導入を防ぐことの重要性を示唆している。
- 高リスクパッチでの健康教育 ($u_1$) および高リスクから低リスクパッチへの輸送 ($u_3$): これらの制御は後期段階で増加し、長期的に健康教育の強化と高リスクから低リスクパッチへの羊の輸送の適度な増加が有益である可能性を示唆している。
- 低リスクパッチでの健康教育 ($u_4$): この制御は低いレベルを維持し、これらの地域での疾患制御への影響が小さいことを示唆している。
さらに、局所制御戦略の分析(図7)は、 $u_2$(高リスクでのワクチン接種)および $u_3$(高リスクから低リスクへの輸送)のような個々の介入が、高リスクパッチでの感染を大幅に削減できる一方で、$u_5$(低リスクでのワクチン接種)および $u_6$(低リスクから高リスクへの輸送の制限)が低リスクパッチで効果的であったとしても、局所戦略だけでは寧夏におけるブルセラ症の全体的な制御目標を達成するには不十分である可能性があることを明らかにした。
それらのコアメカニズムの有効性に対する決定的な証拠は、クロスパッチ複合制御戦略の評価(図8)から得られた。戦略 $S_{12}$($u_2, u_3, u_5$の組み合わせ)は、高リスクパッチで最も効果的な戦略として浮上し、感染羊の累積削減が最大になった。低リスクパッチでは、戦略 $S_{10}$($u_2, u_5, u_6$の組み合わせ)が最大の正の累積変化を生み出し、感染削減におけるその優れたパフォーマンスを示した。これは、差別化された複合アプローチが、各パッチの特定の危険度レベルに合わせて調整されることが、ブルセラ症の効果的な制御に不可欠であることを紛れもなく証明している。
限界と将来の方向性
この研究は貴重な洞察とブルセラ症制御のための堅牢なフレームワークを提供する一方で、その固有の限界を認識することが重要であり、これは自然に将来の研究への道を開く。
まず、重要な限界は、羊ブルセラ症感染率の間接的な推定に由来する。寧夏における羊の群れにおけるブルセラ症感染に関する直接的な歴史データがないため、著者らは線形回帰モデルを使用してヒトブルセラ症発生率からこれらの率を推測しなければならなかった。回帰は高い $R^2$ 値を示したものの、この間接的な推定方法はデータバイアスを導入する可能性がある[47]。プロキシデータへのこの依存は、モデルのキャリブレーションの精度、ひいては導出された最適制御戦略に影響を与える可能性がある。
第二に、現在のモデルは各パッチ内での羊個体群の均一な混合を仮定しており、個体群構造の複雑な影響を無視している。年齢、異なる繁殖タイプ、および単純な移動率を超える特定のクロスパッチ相互作用などの要因は、明示的に考慮されていない[48]。実際には、これらの構造的要素は疾患伝播ダイナミクスを大幅に変化させる可能性があり、モデルは多様な家畜個体群におけるブルセラ症の広がりを完全に捉えられない可能性がある。
第三に、決定論的モデルの使用は、ランダムなイベントを記述する能力を本質的に制限する。感染した羊の確率的移動のような現象は、疾患伝播にかなりの影響を与える可能性があるが、現在のフレームワークでは捉えることができない[49]。現実世界の疫病はしばしば予測不可能なイベントの影響を受けるため、決定論的なアプローチはこれらの重要な側面を単純化しすぎる可能性がある。
将来に向けて、これらの限界は自然に、これらの発見のさらなる開発と進化のためのいくつかの有望な方向性を示唆している。
- 個体群構造の組み込み: 将来の研究は、より詳細な個体群構造を羊ブルセラ症モデルに統合することを目指すべきである。これには、年齢構造化モデルの開発や、異なる繁殖タイプ(例:乳用羊対肉用羊)の区別が含まれる可能性がある。これにより、異なるサブ個体群が全体的な疫病にどのように貢献するか、および介入をどのようにさらに正確に調整できるかをよりニュアンス的に理解できる。
- 確率論のモデリング: 現在のモデルの決定論的な性質に対処するために、将来の研究では確率的プロセスを組み込むことができる。具体的には、環境確率論またはランダム移動イベントを描写するためにオルンシュタイン=ウーレンベックプロセスを使用することは非常に価値があるだろう。これにより、ランダム性が伝播ダイナミクスと制御戦略の堅牢性にどのように影響するかをより現実的に評価でき、より回復力のある介入計画につながる可能性がある。
- 直接的なデータ収集と検証: 長期的な目標は、羊の群れにおけるブルセラ症感染に関する直接的かつ包括的な監視データを促進し、利用することである。これにより、間接的な推定の必要性がなくなり、モデルのキャリブレーションと検証の精度が大幅に向上する。公衆衛生機関、獣医サービス、および研究者の間の協力的な取り組みは、そのようなデータ収集システムの確立に不可欠である可能性がある。
- 経済的費用便益分析: 現在の研究は感染個体群を最小化するための最適制御に焦点を当てているが、将来の研究は、異なる制御戦略の包括的な経済的費用便益分析を含むように拡張できる。これは、特に限られた保健資源を考慮して、疾患削減と資源配分効率のバランスを取る、より全体的な視点を政策立案者に提供するだろう。
これらの点を対処することにより、発見はさらに洗練され、寧夏のような地域およびそれ以降の地域における、さらに正確で堅牢で実用的なブルセラ症制御戦略につながるだろう。
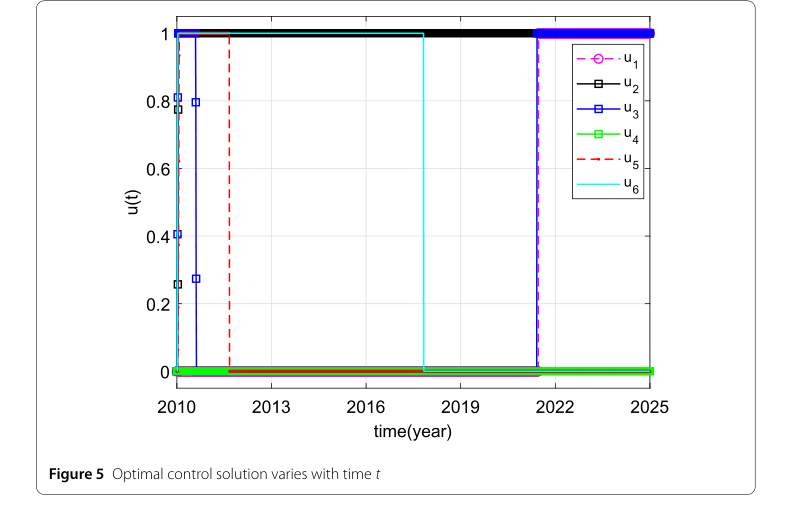 Figure 5. Optimal control solution varies with time t
Figure 5. Optimal control solution varies with time t
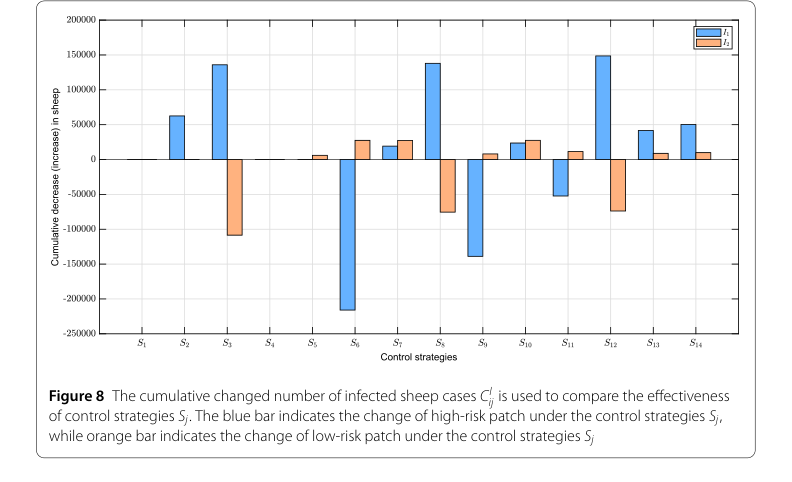 Figure 8. The cumulative changed number of infected sheep cases CI ij is used to compare the effectiveness of control strategies Sj. The blue bar indicates the change of high-risk patch under the control strategies Sj, while orange bar indicates the change of low-risk patch under the control strategies Sj
Figure 8. The cumulative changed number of infected sheep cases CI ij is used to compare the effectiveness of control strategies Sj. The blue bar indicates the change of high-risk patch under the control strategies Sj, while orange bar indicates the change of low-risk patch under the control strategies Sj
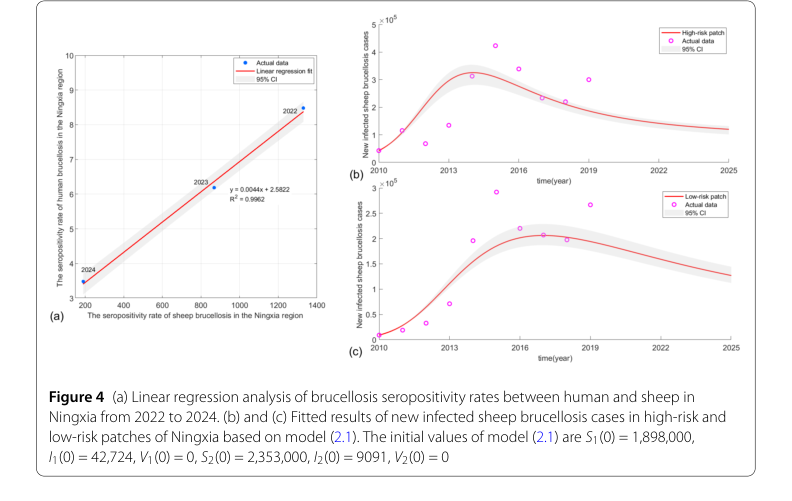 Figure 4. (a) Linear regression analysis of brucellosis seropositivity rates between human and sheep in Ningxia from 2022 to 2024. (b) and (c) Fitted results of new infected sheep brucellosis cases in high-risk and low-risk patches of Ningxia based on model (2.1). The initial values of model (2.1) are S1(0) = 1,898,000, I1(0) = 42,724, V1(0) = 0, S2(0) = 2,353,000, I2(0) = 9091, V2(0) = 0
Figure 4. (a) Linear regression analysis of brucellosis seropositivity rates between human and sheep in Ningxia from 2022 to 2024. (b) and (c) Fitted results of new infected sheep brucellosis cases in high-risk and low-risk patches of Ningxia based on model (2.1). The initial values of model (2.1) are S1(0) = 1,898,000, I1(0) = 42,724, V1(0) = 0, S2(0) = 2,353,000, I2(0) = 9091, V2(0) = 0
