残余后模式的脑连接特征精炼
New AI model RP-LGN captures subtle connectivity changes for better disease diagnosis, outperforming others with improved accuracy & noise handling.
背景与学术传承
为了理解人脑的真实本质,我们必须超越孤立的区域,研究它们如何进行交流。历史上,神经科学家使用功能性磁共振成像(fMRI)来捕捉大脑活动。随着计算神经科学领域的发展,研究人员开始将大脑表示为一个复杂的网络,或一个“图”,其中大脑区域是节点,它们的通信路径是边。这自然导致了图神经网络(GNNs)在分析这些功能连接模式后,被用于诊断自闭症谱系障碍(ASD)和注意力缺陷多动障碍(ADHD)等神经精神疾病。
然而,一个关键的瓶颈出现了。传统的GNN方法在这种特定任务上存在根本性缺陷,因为它们主要关注大脑区域本身(节点),而不是实际的通信路径(边)。在神经精神疾病中,疾病通常表现为连接的改变,而不是物理区域。此外,以前的模型面临巨大的计算障碍:如果你试图将每一个连接都视为全连接大脑图中的一个主要特征,数学计算将呈指数级增长。典型的大脑图谱可能产生一个包含数十亿参数的矩阵,使其在计算上无法处理。除此之外,医学数据集出了名地小且充满噪声,导致传统模型出现过拟合——也就是说,它们记住了训练数据,但在现实世界的临床应用中完全失效。
为了弥合这一差距,作者引入了残差后验线图网络(RP-LGN)。让我们将他们使用的专业术语分解为直观的理念:
解构术语
- 功能性磁共振成像(fMRI)与BOLD信号:在论文中,这是测量大脑血流量变化的原始数据。
- 日常类比:想象一下,卫星通过观察车头灯的密度来追踪城市夜晚的交通拥堵情况。fMRI通过血流量来做到这一点;它追踪“交通”(含氧血液)的去向,以确定哪些“交叉路口”(大脑区域)当前是活跃的,并且正在相互通信。
- 线图变换:一种将边转换为节点的数学技术。
- 日常类比:假设你正在研究一个全球航空网络。通常,你会研究城市(节点)并为航线(边)绘制线条。线图变换则颠倒过来:你将航线作为研究的主要对象(新的节点),而城市仅作为终点。这使得AI能够直接研究实际的连接。
- GNN中的过平滑:节点之间传递消息次数过多,导致所有节点看起来都相同的现象。
- 日常类比:想象一下混合颜料。如果你轻轻地将红色和蓝色漩涡状混合,你会得到美丽的纹理图案(有用的信息)。但如果你不停地搅拌,最终只会得到一种平淡、浑浊的紫色。过平滑就是AI过度搅拌数据,丢失了大脑所有独特、区分性的特征。
- 贝叶斯变分后验:模型最终层用于量化预测不确定性的一种统计方法。
- 日常类比:天气预报应用不会生硬地说“明天会下雨”(如果数据有噪声,这可能是错误的),而是采用贝叶斯方法说:“我有85%的信心会下雨,误差在5%左右。”它计算出误差范围,使得AI的医学诊断更加稳健和可信,即使患者的扫描图像有很多背景噪声。
数学蓝图
为了在数学上解释作者是如何解决这个问题的,我们需要查看定义他们宇宙的变量。他们使用 $K$-近邻(KNN)方法来稀疏化初始连接,以防止参数爆炸,然后将图映射到一个线图 $\tilde{G}$。最后,他们通过最大化证据下界(ELBO),表示为 $\mathcal{L}_{VB}$,来优化模型。
| 符号 | 描述 |
|---|---|
| $V$ | 代表大脑中感兴趣区域(ROIs)的节点集合。 |
| $E$ | 代表ROIs之间功能连接的边集合。 |
| $G = (\mathbf{A}, \mathbf{X})$ | 从fMRI数据构建的原始大脑图。 |
| $\mathbf{A} \in \mathbb{R}^{|V| \times |V|}$ | 定义大脑区域之间偏相关系数的邻接矩阵。 |
| $\mathbf{X} \in \mathbb{R}^{|V| \times |F|}$ | 基于成对BOLD信号的Pearson相关性的节点特征矩阵。 |
| $n$ | ROIs的总数,其中 $|V| = n$。 |
| $\mathcal{N}_i$ | 节点 $i$ 的 $K$ 个最近邻节点集,用于稀疏化图。 |
| $\tilde{G} = \{\tilde{\mathbf{A}}, \tilde{\mathbf{X}}\}$ | 构建的线图,其中原始边被视为节点。 |
| $\tilde{\mathbf{x}}_i$ | 新构建的线图中第 $i$ 个节点的特征向量。 |
| $\tilde{\mathbf{Z}}^{(l)}$ | 第 $l$ 个SAGEConv(GraphSAGE卷积)层的输出特征矩阵。 |
| $W$ | 最终线性分类层的权重矩阵。 |
| $\Sigma$ | 变分后验的协方差矩阵,用于建模不确定性。 |
| $\mathcal{L}_{VB}(\theta, \eta, \Sigma)$ | 作为优化模型目标函数的变分下界(ELBO)。 |
通过结合这些元素,作者彻底革新了大脑网络分析的方法。他们成功地将AI的注意力从大脑区域转移到实际的连接上,保持了计算成本低廉,并内置了一个数学“安全网”来处理小型、有噪声的医学数据集的不确定性。
问题定义与约束
为了理解本文,我们首先需要了解科学家如何看待大脑。将人脑想象成一个广阔的国家。不同的脑区是“城市”,它们之间通信的神经通路是“高速公路”。
当医生使用功能性磁共振成像 (fMRI) 时,他们实际上是在追踪这些城市之间随时间变化的交通流量(血流量和氧气)。通过计算任意两个城市之间交通流量的同步程度,科学家们创建了一个“功能连接性”(Functional Connectivity, FC) 矩阵。用数学术语来说,这是一个图 $G = (\mathbf{A}, \mathbf{X})$,其中节点(城市)具有特征 $\mathbf{X}$,边(高速公路)由邻接矩阵 $\mathbf{A}$ 表示,该矩阵显示了区域之间的相关性强度。
起点(输入)是源自 fMRI 数据的原始的、患者特异性的大脑图。期望的终点(输出)是一个高度准确、可解释的二元分类——具体来说,是确定患者是否患有自闭症谱系障碍 (ASD) 或注意力缺陷多动障碍 (ADHD) ($y_D$),或者他们是否为健康对照组 ($y_{HC}$)。
缺失的环节:节点与边
这正是本文试图弥合的根本性差距。传统的图神经网络 (GNNs) 是高度“以节点为中心”的。在其数学运算(称为消息传递)过程中,它们通过聚合邻近城市的数据来不断更新城市(脑区)的信息。高速公路(边)仅仅被当作指示数据流向的哑管道。
然而,在临床神经科学中,ADHD 和 ASD 等疾病不仅仅会改变孤立的脑区;它们会从根本上扰乱连接本身。确切的数学差距在于,传统 GNN 未能将这些连接视为主要的、可学习的特征。作者们意识到,他们需要将边提升为神经网络中的“一等公民”。
维度困境
为了解决这个问题,逻辑步骤是使用“线图”(Line Graph) 变换。在图论中,将标准图转换为线图意味着将每个原始边转换为一个新的节点。突然之间,高速公路变成了城市,允许神经网络直接分析连接。
但这引入了一个残酷而痛苦的权衡,它困扰着之前的研究人员:表示能力 vs. 计算爆炸。
如果有一个包含 $n$ 个区域的大脑图谱,一个全连接的大脑图大约有 $n^2 / 2$ 条边。如果将其转换为线图(其中每条边都变成一个新节点,而这些新节点之间的边代表共享连接),则新邻接矩阵的大小将呈指数级膨胀至:
$$(n - 1)^2 \times n^2 / 4$$
如果大脑被划分为仅 200 个区域,这种线图变换将导致矩阵包含数十亿个参数。这是一个计算上的噩梦。你获得了大脑连接性的完美表示,但完全打破了现代 GPU 的硬件内存限制。
严酷的壁垒与约束
除了计算爆炸之外,作者们还遇到了几个严酷的现实壁垒,使得这个问题异常困难:
- fMRI 数据的极端稀疏性和噪声: fMRI 扫描的噪声极大。患者会移动,扫描仪有伪影,血流量是神经活动的间接测量。此外,与巨大的特征空间相比,医学数据集出了名的小(通常只有几百名患者,如 ABIDE 或 ADHD-200 数据集)。在仅有 500 名患者的情况下,对包含数十亿参数的深度学习模型进行训练,必然会导致灾难性的过拟合。
- 过平滑的诅咒: 在 GNN 中,如果堆叠太多层来学习复杂模式,所有节点的特征最终会混合成一种均匀的糊状物——这种现象被称为过平滑。如果模型过平滑,隐藏在特定大脑连接中的独特疾病生物标志物就会被冲淡。
- 无向图的数学模糊性: 无向图中标准的皮尔逊相关性模糊了双向和单向神经激活之间的区别,使模型对大脑通信的实际流向感到困惑。
作者如何解决
为了打破这些壁垒,作者们设计了残差后验线图网络 (Residual-Posterior Line Graph Network, RP-LGN)。他们通过三个巧妙的步骤,在数学上规避了这些约束:
1. K-近邻 (KNN) 稀疏化
为了防止 $O(n^4)$ 的计算爆炸,他们没有从全连接的大脑构建线图。相反,他们在变换之前,使用 KNN 算法对原始图进行了激进的稀疏化。通过计算节点特征之间的欧氏距离:
$$d(v_i, v_j) = \|x_i - x_j\|_2$$
他们将图限制为仅包含 $K=1$ 个最近邻。该集合之外的边被强制设为零。这极大地减小了图的大小,使得线图 $\tilde{G} = \{\tilde{\mathbf{A}}, \tilde{\mathbf{X}}\}$ 能够放入内存,同时保留了最关键的神经通路。
2. 残差 GraphSAGE 架构
为了对抗过平滑的诅咒,他们使用了特定类型的图卷积(GraphSAGE)并结合了残差块。而不是让连接特征在消息传递过程中消失,他们将层的原始输入直接添加到输出:
$$\tilde{\mathbf{X}}^{(l+1)} = \tilde{\mathbf{X}}^{(l)} + \tilde{\mathbf{Z}}^{(l)}$$
这种数学上的“跳跃连接”迫使网络记住大脑连接的原始结构保真度。
3. 用于小样本偏差的贝叶斯变分推断
为了克服极端噪声和小样本量的问题,他们放弃了传统的确定性分类层。取而代之的是,他们引入了一个贝叶斯变分后验。模型不是说“这个连接权重正好是 0.8”,而是将权重 $W$ 和协方差 $\Sigma$ 视为具有高斯分布的随机变量:
$$q(\Sigma) = \prod_{k=1}^{C_y} \mathcal{N}(W_k \mid \mu_k, \Sigma_k)$$
通过这样做,模型量化了自身的不确定性。如果 fMRI 数据存在噪声或异常,模型会在数学上降低其置信度,而不是过拟合到噪声上。他们通过最大化证据下界 (ELBO) 来优化这一点:
$$S^{-1} \log p(Y \mid \mathbf{X}, \mathbf{A}, \theta) \geq \mathcal{L}_{VB}(\theta, \eta, \Sigma) - S^{-1}\text{KL}(q(W, \Sigma \mid \eta) \parallel p(W, \Sigma))$$
通过结合稀疏化的线图来靶向连接,残差层来防止平滑,以及贝叶斯概率来应对噪声和小型数据集,作者们成功地创建了一个模型,该模型不仅能猜测患者是否患有 ADHD,还能在数学上突出导致该疾病的确切故障神经通路。
为何采用此方法
为了理解作者为何构建残差后验线图网络(Residual-Posterior Line Graph Network, RP-LGN),我们必须审视传统图神经网络(GNNs)在神经影像学领域遭遇瓶颈的确切时刻。
在用于大脑分析的标准 GNNs 中,物理的大脑区域被视为“主角”(节点),而它们之间的功能连接则仅仅被当作背景关系(边)。然而,作者们认识到一个关于自闭症和注意力缺陷多动障碍(ADHD)等神经精神疾病的基本事实:疾病的实际表现恰恰发生在连接本身。传统的模型关注了错误的优先实体。
为了解决这个问题,作者们需要将这些连接提升为“一流对象”。唯一可行的数学解决方案是进行边到节点(edge-to-node)的转换,从而创建一个所谓的“线图”(line graph)。但这引入了一个灾难性的约束。一个具有 $n$ 个区域的全连接初始大脑图大约有 $n^2/2$ 条边。如果将这些边转换为节点以形成线图,新的邻接矩阵将膨胀到惊人的 $(n-1)^2 \times n^2/4$ 规模。对于拥有数百个区域的标准大脑图谱而言,这意味着需要计算包含数十亿参数的矩阵。传统的 SOTA 模型会立即耗尽内存,使得纯粹的线图方法在计算上变得不可能。
基准测试逻辑与结构优势
为了克服这种巨大的 $O(N^4)$ 内存爆炸,作者们并未仅仅投入更多的计算能力来解决问题;他们通过结构性地规避了它。他们引入了一个 K-最近邻(KNN)稀疏化步骤,在线图构建之前进行。通过设置 $K=1$,他们利用欧氏距离在数学上对图进行了剪枝:
$$ \mathcal{N}_i = \text{argmin}_j \{d(v_i, v_j) \mid j \neq i\}_{1 \leq j \leq K, i, j \in V} $$
这一巧妙的约束将密集且不可行的矩阵转化为高度稀疏、可管理的表示,仅保留了最关键的功能连接。
此外,他们必须选择合适的骨干网络来处理这个新图。为何不使用图注意力网络(GAT)等流行方法?作者们消融研究(ablation studies)明确表明,GAT 的注意力机制实际上与他们的架构产生了冲突,导致了适得其反的结果。取而代之的是,他们选择了一个残差 GraphSAGE 骨干网络。这在质量上更为优越,因为残差连接完美地保留了原始图的结构保真度,防止了“过平滑”(oversmoothing)——这是标准 GNNs 中的一个致命缺陷,即节点特征在经过几层消息传递后会模糊成无法区分的混乱状态。
严苛约束与贝叶斯解决方案的“联姻”
第二个巨大的障碍是 fMRI 数据本身的性质:它极其嘈杂,且医学数据集饱受严重的样本量不足(small-sample bias)的困扰。如果作者们像几乎所有之前的黄金标准模型那样,使用标准的全连接层作为分类器,网络将压倒性地过拟合到小数据集上。
为了解决这个问题,他们完全摒弃了确定性分类器,并将贝叶斯变分后验(Bayesian variational posterior)整合为最后一层。贝叶斯方法不输出一个僵化的、单一的预测,而是将最后一层权重 $W$ 和协方差矩阵 $\Sigma$ 作为随机变量进行建模。他们通过最大化证据下界(Evidence Lower Bound, ELBO)来近似真实的后验分布:
$$ S^{-1} \log p(Y | \mathbf{X}, \mathbf{A}, \theta) \geq \mathcal{L}_{VB}(\theta, \eta, \Sigma) - S^{-1}\text{KL}(q(W, \Sigma | \eta) \parallel p(W, \Sigma)) $$
这正是该方法与问题约束完美契合之处。通过将分类权重视为一个分布而非固定数值,模型内在地量化了不确定性。如果一个 fMRI 扫描包含异常数据或高维噪声,贝叶斯层会吸收这种不确定性,而不是被它所欺骗。这种单次通过、低方差的随机推理,使得 RP-LGN 能够抵御摧毁传统 SOTA 模型的小样本过拟合陷阱,最终能够揭示大脑真正隐藏的连接模式。
数学与逻辑机制
为了理解本文引入的深刻转变,我们首先需要确立人工智能通常如何看待人脑的背景。传统上,在分析功能性磁共振成像 (fMRI) 数据时,图神经网络 (GNNs) 将物理大脑区域视为“节点”,并将它们之间的相关性视为“边”。然而,注意力缺陷多动障碍 (ADHD) 和自闭症等神经精神疾病通常表现为通信通路本身的微妙退化。本文的动机是将这些通路——连接——提升为分析的主要对象。
为了实现这一点,作者面临着巨大的限制。如果将大脑图在数学上进行逆运算,使每个连接成为一个新的节点(“线图”),参数数量将爆炸式增长至数十亿,这将立即导致标准模型崩溃。此外,fMRI 数据以其固有的噪声而闻名,而医学数据集通常很小(通常只有几百名患者),这会导致严重的过拟合。为了克服这些限制,作者使用 K-Nearest Neighbors 对图进行稀疏化,构建了一个 Residual GraphSAGE 主干以防止信号模糊(过平滑),并用一个贝叶斯变分后验来量化不确定性。
以下是他们如何实现这一目标的数学解剖。
核心方程
Residual-Posterior Line Graph Network (RP-LGN) 的引擎由两个相互关联的数学系统驱动。
首先,残差消息传递机制,用于从线图中提取结构特征:
$$ \tilde{z}_i^{(l)} = \sigma\left(\theta_i^{(l)} \cdot \text{MEAN}\left(\{\tilde{x}_i^{(l)}\} \parallel \{\tilde{x}_j^{(l)}, \forall j \in \mathcal{N}_i\}\right)\right) $$
$$ \tilde{\mathbf{X}}^{(l+1)} = \tilde{\mathbf{X}}^{(l)} + \tilde{\mathbf{Z}}^{(l)} $$
其次,贝叶斯变分目标,作为最终的损失函数,迫使模型在预测准确性和不确定性之间取得平衡:
$$ \mathcal{L}_{VB}(\theta, \eta, \Sigma) = \frac{1}{S} \sum_{s=1}^S \left( y_s^\top W \phi_s - \log \sum_{k=1}^{C_y} \exp\left[w_k^\top \phi_s + \frac{1}{2}(\phi_s^\top \Sigma_k \phi_s + \sigma_k^2)\right] \right) $$
$$ \theta^*, \eta^*, \Sigma^* = \arg\max_{\eta, \Sigma} \left\{ \mathcal{L}_{VB}(\theta, \eta, \Sigma) + S^{-1}(\log p(\Sigma) - \text{KL}(q(W \mid \eta) \parallel p(W))) \right\} $$
解析方程
让我们来剖析这个机械装置中的每一个齿轮和弹簧:
- $\tilde{\mathbf{X}}^{(l)}$ 和 $\tilde{x}_i^{(l)}$:第 $l$ 层线图的特征矩阵和单个特征向量。在物理上,它们代表了已被提升为一等节点的实际大脑连接。
- $\parallel$ (拼接运算符):它将节点自身的特征与其邻居的平均值连接起来。为什么在这里使用拼接而不是加法?拼接保留了特定大脑连接的独立、隔离的身份,同时附加了邻域上下文。加法会将它们不可逆地混合在一起。
- $\theta_i^{(l)}$:可学习的权重矩阵。它充当几何方向盘,将特征向量旋转到更高的维度空间,在那里疾病模式和健康模式得以分离。
- $\sigma$:激活函数。它充当生物学阈值,决定哪些神经连接模式足够显著可以向前传递。
- $+$ (在 $\tilde{\mathbf{X}}^{(l)} + \tilde{\mathbf{Z}}^{(l)}$ 中):残差连接。为什么使用加法而不是乘法?加法创建了一个安全的旁路高速公路。如果图卷积提取了不必要的噪声,网络可以将权重推至零,直接传递原始数据。乘法可能会将整个信号压缩为零,破坏表示。
- $\mathcal{L}_{VB}$:变分下界。这是模型分类能力的主要评分指标。
- $S$:受试者(患者)的数量。我们使用对 $S$ 的求和 $\sum$ 而不是积分,因为患者是离散的、可数的实体,而不是连续的光谱。
- $y_s^\top W \phi_s$:正确诊断的预期 logit 分数,其中 $\phi_s$ 是患者 $s$ 的扁平化、完全处理后的大脑图谱。
- $\frac{1}{2}(\phi_s^\top \Sigma_k \phi_s + \sigma_k^2)$:方差/不确定性惩罚。$\Sigma_k$ 是协方差矩阵。这一项将计算量的 Gaussian 噪声直接注入预测。它充当数学减震器,抵消 fMRI 扫描固有的噪声。
- $\text{KL}(q \parallel p)$:Kullback-Leibler 散度。它充当橡皮筋,将学习到的后验权重分布 $q$ 拉回到安全、稳定的先验分布 $p$,以防止过拟合。
分步流程
想象一个抽象的数据点——来自一次 \$150 fMRI 扫描的前额叶皮层和基底神经节之间的功能连接。
首先,这个连接被剥离,从一个普通的“边”提升为一个新的线图中的完整“节点”。它根据原始大脑区域的相关强度被赋予一个特征向量。接下来,它进入 Residual GraphSAGE 装配线。它查看其邻居连接,平均它们的信息,并将其与自身数据捆绑在一起。
这个捆绑包与权重矩阵 $\theta$ 相乘以提取更高级别的拓扑模式,通过激活函数 $\sigma$ 进行处理以裁剪负值,然后通过残差路径加回到其原始自身。这确保了连接在处理过程中不会丢失其原始身份。
经过多层处理后,完全处理后的大脑图谱 $\phi_s$ 到达贝叶斯分类器。分类器不是通过一个刚性的、确定性的权重来获得最终答案,而是从一个概率分布中采样。它输出的不仅仅是诊断(例如,“ADHD”),还有一个置信度水平,考虑了原始医学数据的固有噪声。
优化动力学
这个架构实际上是如何学习和收敛的?模型依赖于随机变分推断来导航一个极其困难的损失景观。
在传统的 fMRI 分析中,由于数据是高维但样本量很小(小样本偏差),损失景观高度崎岖且容易出现严重的过拟合。通过引入贝叶斯后验($\Sigma$ 和 KL 散度项),损失景观被有效地平滑了。当数据模糊不清时,模型因过于自信其预测而受到主动惩罚。
在反向传播过程中,梯度从 ELBO 目标向后流动。残差连接确保这些梯度有一条清晰、无阻碍的高速公路,可以一直回溯到第一层,完全绕过梯度消失问题。通过迭代,模型更新 $\theta$ 以提取更好的结构特征,同时更新 $\eta$ 和 $\Sigma$ 以校准其不确定性。它收敛到一个稳健的状态,即使面对异常的患者数据,也能准确地区分健康和患病的大脑。
结果、局限性与结论
将人脑想象成一个广阔而繁忙的国家。大脑区域是主要城市,它们之间的神经通路是高速公路。多年来,神经科学家和人工智能研究人员一直使用功能性磁共振成像 (fMRI) 来测量这些城市中的“交通”(血流量),以诊断自闭症谱系障碍 (ASD) 和注意力缺陷多动障碍 (ADHD) 等神经精神疾病。传统的图神经网络 (GNN) 一直是首选工具,将大脑区域视为节点(城市),将连接视为边(高速公路)。
但这里存在一个根本性的缺陷:如果疾病不是破坏城市,而是扰乱了高速公路呢?传统 GNN 主要关注更新节点的特征,将连接视为次要属性。
本文的作者认识到这一盲点,并提出了一个绝妙的范式转变:残差后验线图网络 (RP-LGN)。他们决定让连接成为表演的主角。
动机与数学约束
为了聚焦于连接,作者们使用了图论中的一个概念,称为“线图”。在线图中,原始图的边成为新图的节点。
然而,他们立即遇到了巨大的数学障碍。如果一个大脑图谱将大脑划分为 $n$ 个区域,那么一个全连接图有 $(n - 1) \times n / 2$ 条边。如果将其转换为线图,新的邻接矩阵的规模将爆炸到 $(n - 1)^2 \times n^2 / 4$。对于拥有数百个区域的大脑,您将突然处理数十亿个参数。这是一个计算上的噩梦。此外,fMRI 数据出了名的嘈杂,而医学数据集通常样本量很小,这使得大型模型极易出现过拟合。
他们是如何解决的:RP-LGN 架构
为了克服这些限制,作者们设计了一个四步流程:
1. 通过 KNN 进行无情稀疏化
在构建线图之前,他们必须修剪原始图。他们使用 K-最近邻 (KNN) 方法,特别是设置 $K=1$,仅保留基于欧几里得距离的最关键连接:
$$d(v_i, v_j) = \|x_i - x_j\|_2$$
说实话,我对此部分也不是完全确定——论文并未深入论证丢弃除一阶邻居边之外的所有边的临床有效性,尽管这无疑解决了计算爆炸的问题。
2. 边到节点转换
接下来,他们构建了线图。新的节点(代表原始高速公路)需要特征。他们巧妙地通过连接两个大脑区域的特征之和与原始边权重来构建这些特征:
$$\tilde{x}_i = \text{CONCATE}(\text{SUM}(x_i, x_j), a_{ij})$$
3. 用于消息传递的残差 GraphSAGE
由于线图本身没有边权重,作者们使用 GraphSAGE 在这些新的连接节点之间传递消息。为了防止“过平滑”——一种常见的 GNN 问题,即重复的消息传递会将所有特征模糊成通用的混合体——他们添加了残差连接:
$$\tilde{\mathbf{X}}^{(l+1)} = \tilde{\mathbf{X}}^{(l)} + \tilde{\mathbf{Z}}^{(l)}$$
4. 贝叶斯变分后验
最后,为了对抗噪声和小样本过拟合,他们放弃了传统的确定性分类器。相反,他们将最后一层的权重视为具有高斯分布的随机变量。通过使用随机变分推断,模型不仅仅是做出一个僵化的猜测;它量化了自身的模型不确定性。他们通过最大化证据下界 (ELBO) 来优化这一点:
$$S^{-1} \log p(Y|\mathbf{X}, \mathbf{A}, \theta) \geq \mathcal{L}_{VB}(\theta, \eta, \Sigma) - S^{-1}\text{KL}(q(W, \Sigma|\eta) \parallel p(W, \Sigma))$$
实验架构与“牺牲者”
作者们不仅仅声称他们的数学有效;他们设计了一个严酷的考验来证明它。他们使用严格的 5 折交叉验证,在 ABIDE I(自闭症)和 ADHD-200 数据集上测试了 RP-LGN。
他们留下的“牺牲者”是标准模型和最先进模型中的佼佼者:KAN 等单分类器、标准 GNN(GAT、GIN、GraphSAGE),以及 BrainNetCNN、BrainGNN、BrainGB、FBNETGEN 和 BrainNetworkTransformer 等专用大脑网络。RP-LGN 的表现优于所有这些模型。
但决定性的、无可辩驳的证据不仅仅是更高的准确率百分比。它以两种形式出现:
1. 消融研究: 他们系统地剥离了残差连接和贝叶斯后验。当应用于 SAGE、GIN 和 GAT 等基础模型时,性能明显下降,证明了这些特定机制是模型优越性的确切原因。
- 通过 Grad-CAM 进行临床验证: 他们使用基于梯度的定位来可视化模型依赖哪些“高速公路”来诊断 ADHD。该模型独立地突出了顶叶上小叶、尾状核和梭状回之间的连接。这是确凿的证据:这些正是临床精神科医生长期以来与空间注意力、奖励处理和冲动控制相关的脑区——ADHD 的核心缺陷。数学完美地重新发现了生物学。
未来演进的讨论话题
基于这个出色的基础,以下是关于我们如何进一步推进这种大脑连接表示的几个不同视角:
- 稀疏化中的 $K=1$ 困境: 作者使用了 $K=1$ 来节省计算开销,但大脑是一个高度整合的多通路系统。我们能否探索动态稀疏化技术,例如基于注意力的修剪,以保留临床相关的长距离连接,而不是严格依赖于欧几里得最近邻?
- 时间动态与静态快照: RP-LGN 将 fMRI 数据视为部分相关性的静态图。然而,大脑连接性是高度动态的;高速公路根据认知负荷而开放和关闭。我们如何在不触发另一次参数爆炸的情况下,将滑动窗口时间动态集成到线图框架中?
- 临床中贝叶斯不确定性的解释: 贝叶斯后验提供了模型不确定性的数学量化。我们如何将这种数学方差转化为医生可操作的指标?例如,如果模型输出具有高方差的诊断,这是否可以在实际临床环境中触发特定的二级筛查方案?
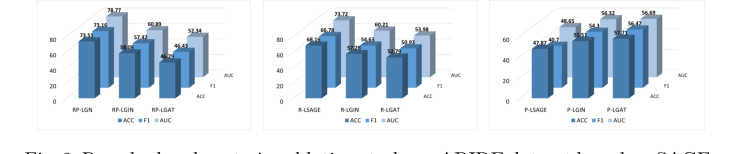 Figure 2. Resudual and posterior ablation study on ABIDE dataset based on SAGE, GIN and GAT. R: residual, P: posterior, L: line graph
Figure 2. Resudual and posterior ablation study on ABIDE dataset based on SAGE, GIN and GAT. R: residual, P: posterior, L: line graph
